para o que é indicado e para que serve?
Para que serve Nexavar é indicado para o tratamento de: Um determinado tipo de câncer nos rins que não tenha respondido ao tratamento prévio com alfainterferona ou interleucina-2 ou que não pudessem receber tal terapia.Continue lendo...
ofertas de
Nexavar - 200Mg 60 Compri...
ofertas de Nexavar - 200Mg 60 Compri...
R$ 8.260,00
R$ 8.370,00
R$ 8.490,00
R$ 8.500,00
ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
Nexavar é indicado para o tratamento de:
Um determinado tipo de câncer nos rins que não tenha respondido ao tratamento prévio com alfainterferona ou interleucina-2 ou que não pudessem receber tal terapia.
Tratamento de câncer no fígado que não possa ser removido com cirurgia.
Tratamento de pacientes com um tipo de câncer de tireoide (diferenciado - papilífero, folicular, célula de Hurthle) localmente avançado ou metastático, progressivo, que não responde à terapia com iodo radioativo.
Nexavar deve ser prescrito e controlado por um oncologista ou profissional de saúde capacitado para tratar pacientes com câncer de rim, fígado ou tireoide.
Como o Nexavar funciona?
Nexavar tem como substância ativa o sorafenibe, um inibidor de múltiplas quinases que atua diminuindo o crescimento das células cancerígenas e interrompendo o suprimento de sangue que mantém o crescimento dessas células.
As concentrações plasmáticas do sorafenibe no estado de equilíbrio são alcançadas em 7 dias, com uma relação máximo-mínimo das concentrações médias inferior a 2.
Converse com o seu médico para que ele possa lhe dar mais detalhes sobre a ação deste medicamento.
Contraindicação
Nexavar não deve ser usado se você tiver hipersensibilidade grave (alergia) ao sorafenibe ou a qualquer outro componente deste medicamento.
Como usar
Uso oral.
A dose recomendada é de 2 comprimidos de Nexavar, duas vezes ao dia, que corrresponde a 800mg por dia. Nexavar deve ser engolido inteiro, com o auxílio de um pouco de água. Pode-se tomá-lo entre as refeições ou durante refeições com pouca ou moderada quantidade de gordura. Não tome Nexavar com refeições ricas em gordura, isto pode deixá-lo menos efetivo. Se você pretende ter uma refeição rica em gordura, Nexavar deve ser tomado pelo menos 1 hora antes ou 2 horas após a refeição.
É importante tomar Nexavar aproximadamente no mesmo horário todos os dias, assim haverá uma quantidade estável do medicamento na circulação sanguínea.
Duração do tratamento e ajuste de dose:
O seu tratamento durará enquanto for benéfico. Seu médico pode interromper temporariamente o tratamento ou modificar a quantidade de comprimidos ingeridos por dia, dependendo de você estar tolerando ou não o tratamento.
Este medicamento não deve ser partido, aberto ou mastigado.
Siga a orientação do seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar o Nexavar?
Se você esquecer de tomar uma dose de Nexavar, deve tomá-la assim que se lembrar; mas se for perto do horário da próxima dose, você não deve ingerir a dose esquecida.
Você não deve ingerir duas doses para compensar a dose esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Informe seu médico se qualquer das situações a seguir se aplica a você. Você pode precisar de algum tratamento ou seu médico pode decidir alterar a dose de Nexavar ou ainda suspender o tratamento com Nexavar:
Se você apresentar reações cutâneas:
Nexavar pode causar reações na pele, principalmente nas mãos e nos pés, e o rash cutâneo. Em geral, essas reações surgem durante as primeiras 6 semanas de tratamento com sorafenibe. O médico pode controlar as reações na pele com tratamento tópico para alívio dos sintomas, interromper o tratamento temporariamente e/ou modificar a dose do medicamento, ou, em casos graves ou persistantes, interromper o tratamento permanentemente.
Se você tem hipertensão (pressão alta):
Observou-se aumento da incidência de hipertensão (pressão alta) em pacientes que receberam Nexavar. Em geral, a hipertensão foi leve a moderada, surgiu no início do tratamento e foi controlável com medicamentos habituais para pressão alta. O médico deve controlar regularmente a pressão arterial, e se necessário, iniciar tratamento de acordo com as condutas médicas padronizadas. Em caso de hipertensão grave, persistente ou de crises hipertensivas apesar do tratamento anti-hipertensivo adequado, o médico deve considerar a descontinuação permanente do tratamento com Nexavar.
Se você apresenta sangramentos ou se está tomando varfarina (um anticoagulante):
O tratamento com Nexavar pode aumentar o risco de hemorragia. A incidência de eventos hemorrágicos graves é incomum. Se ocorrer um sangramento que requeira atenção médica, poderá ser necessária a descontinuação do tratamento com Nexavar. Em pacientes com câncer de tiroide diferenciado, no caso de haver infiltração da traqueia, dos brônquios e do esôfago deve ser feita terapia localizada antes de administrar Nexavar, devido ao risco potencial de sangramento. Informe seu médico se estiver tomando varfarina, pois estes medicamentos alteram a consistência do sangue para prevenir formação de coágulo e podem aumentar o risco de hemorragia.
Se você apresentar dores no peito e problemas cardíacos:
Caso você desenvolva isquemia cardíaca e/ou infarto durante o tratamento com Nexavar, o médico deve considerar a descontinuação temporária ou permanente do tratamento.
Se você tem uma anormalidade do coração conhecida como intervalo QT prolongado:
Nexavar pode afetar o rítmo cardíaco. Caso você tenha síndrome congênita do QT longo, esteja em tratamento com altas doses cumulativas de antraciclina (outro medicamento para tratamento de câncer), esteja tomando certos medicamentos antiarrítmicos ou outros medicamentos que levem ao prolongamento do QT ou apresente distúrbios eletrolíticos como baixa concentração de potássio (hipocalemia), cálcio (hipocalcemia) ou magnésio (hipomagnesemia) no sangue, informe ao seu médico pois ele pode achar necessário solicitar exames de sangue e eletrocardiogramas, periodicamente, durante o tratamento com Nexavar.
Se você for submeter-se ou submeteu-se à cirurgia recentemente:
Nexavar pode afetar a cicatrização de feridas, então, caso necessite passar por uma cirurgia, informe ao profissional de saúde que você está tomando Nexavar. Seu médico poderá pedir para você interromper temporariamente o tratamento com Nexavar e decidirá quando reiniciá-lo.
Se você estiver tomando neomicina (um antibiótico):
A administração de Nexavar junto com neomicina pode diminuir o efeito de Nexavar.
Se você tiver alteração grave do funcionamento do fígado:
Informe seu médico se estiver com a função do fígado alterada. Você pode apresentar efeitos colaterais mais graves quando utilizar Nexavar.
Se você apresentar perfuração intestinal:
Casos de perfuração intestinal são incomuns. Em alguns casos não estava relacionada a um tumor intrabdominal evidente. O médico deverá interromper o tratamento com Nexavar.
Se você tiver câncer da tireoide:
Seu médico irá monitorar os níveis sanguíneos de cálcio e de hormônios da tireoide.
Reações Adversas
Como todo medicamento, Nexavar pode causar reações adversas, embora nem todos pacientes apresentem essas reações.
As reações adversas mais comuns foram diarreia, fadiga, queda de cabelo, infecção, reação cutânea mão-pé (desenvolvimento de vermelhidão, dor, inchaço, podendo evoluir com formação de bolhas, nas palmas das mãos ou nas solas dos pés) e vermelhidão/descamação da pele (rash).
Os eventos adversos mais comuns, que foram considerados relacionados ao Nexavar, nos pacientes com câncer renal, hepático ou de tireoide foram fadiga, perda de peso, reação cutânea mão-pé, queda de cabelo, diarreia, falta de apetite, náusea, dor abdominal, hipertensão, infecção e sangramento.
As reações adversas observadas em estudo clínico para tratamento de câncer do fígado, relatadas em pelo menos 10% dos pacientes, em ordem decrescente de frequência, foram: diarreia, fadiga, dor abdominal, perda de peso, falta de apetite, náusea, reação cutânea mão-pé, vermelhidão/descamação da pele, vômitos, constipação, queda de cabelo, coceira, distúrbios do fígado e pele seca.
As reações adversas observadas em estudo clínico para tratamento de câncer renal, relatadas em pelo menos 10% dos pacientes, em ordem decrescente de frequência, foram: diarreia, vermelhidão/descamação da pele, fadiga, reação cutânea mão-pé, queda de cabelo, náusea, coceira, hipertensão, falta de apetite, vômito, constipação, hemorragia, falta de ar, distúrbios da sensibilidade da pele, pele seca, dor abdominal, perda de peso, dor nas articulações e dor de cabeça.
As reações adversas observadas em estudo clínico para tratamento de câncer de tireoide diferenciado, relatadas em pelo menos 10% dos pacientes, em ordem decrescente de frequência, foram: reação cutânea mão-pé, diarreia, queda de cabelo, vermelhidão/descamação da pele, fadiga, perda de peso, hipertensão, infecção, falta de apetite, inflamação da mucosa da cavidade oral (mucosite), náuseas, coceira, níveis baixos de cálcio no sangue, dor de cabeça, constipação, dor nas extremidades dos membros, pele seca, dor abdominal, distúrbios da sensibilidade da pele, elevações de enzimas produziadas pelo fígado, como ALT (alanina aminotrasferase) e AST (aspartato aminotransferase), alterações na voz, dor, vômito, febre e dor de garganta/faringe/laringe.
Reações adversas de acordo com a frequência:
Reações adversas muito comuns (10% ou mais)
- Sensação de fraqueza ou cansaço;
- Dor (incluindo dor na cavidade oral, nos ossos e tumoral);
- Vermelhidão;
- Infecção;
- Hemorragia (incluindo hemorragia no intestino, no trato respiratório e casos incomuns de hemorragia cerebral);
- Febre;
- Diminuição do apetite;
- Dor nas articulações (artralgia);
- Níveis baixos de fosfato no sangue;
- Baixa contagem de leucócitos e linfócitos (tipos de células brancas) no sangue;
- Níveis aumentados de amilase e lipase no sangue (exames relacionados ao pâncreas).
Reações adversas comuns (1 a < 10%)
- Quadro clínico semelhante ao da gripe;
- Má digestão (dispepsia);
- Inflamação da mucosa do trato gastrintestinal (mucosite);
- Dificuldade para engolir (disfagia);
- Dor/queimação na língua e cavidade oral, com lesões dolorosas, incluindo boca seca e inflamada (estomatite);
- Refluxo gastroesofágico;
- Dor nos músculos (mialgia);
- Espasmos musculares;
- Depressão;
- Alteração do paladar (disgeusia);
- Problemas de ereção (impotência);
- Alteração na voz (disfonia);
- Secreção nasal persistente (rinorreia);
- Acne;
- Vermelhidão na pele (rubor facial e do pescoço);
- Pele inflamada, seca ou escamosa podendo sangrar (dermatite esfoliativa);
- Infecção dos folículos pilosos (foliculite);
- Crescimento celular localizado benigno da pele (ceratoacantomas);
- Câncer de pele (carcinoma espinocelular);
- Espessamento da camada externa da pele (hiperqueratose);
- Alteração da função cardíaca, do tipo insuficiência cardíaca congestiva*;
- Isquemia miocárdica e/ou infarto do miocárdio*;
- Alteração da função dos rins;
- Baixa contagem de células sanguíneas (células brancas, vermelhas (anemia) ou plaquetas);
- aumento temporário de enzimas produzidas pelo fígado, detectado em exames de sangue;
- Níveis baixos de cálcio no sangue (hipocalcemia);
- Níveis baixos de potássio no sangue (hipocalemia);
- Níveis baixos de sódio no sangue (hiponatremia);
- Glândula tireoide com atividade reduzida (hipotireoidismo);
- Níveis elevados de proteína na urina (proteinúria).
Reações adversas incomuns (0,1 a < 1%)
- Inflamação do revestimento do estômago (gastrite);
- Inflamação do pâncreas (pancreatite);
- Inflamação da vesícula biliar (colecistite) e/ou ductos biliares;
- Amarelamento da pele ou olhos (icterícia) causada por altos níveis de pigmentos da bile no sangue (hiperbilirrubinemia);
- Reações alérgicas (incluindo reações de pele e urticária);
- Reação anafilática (reação alérgica grave);
- Desidratação;
- Aumento do tamanho das mamas (ginecomastia);
- Eventos do tipo doença pulmonar intersticial (inflamação nos pulmões);
- Eczema;
- Eeações da pele e/ou das membranas mucosas, graves, que podem incluir bolhas dolorosas (eritema multiforme);
- Glândula tireoide com atividade anormal aumentada (hipertireoidismo);
- Crises hipertensivas* (pressão arterial exageradamente alta);
- Perfuração gastrintestinal;
- Edema reversível na parte posterior do cérebro que pode estar associado à dor de cabeça, alteração da consciência, convulsões e sintomas visuais incluindo perda da visão (leucoencefalopatia posterior reversível);
- Eumento temporário dos níveis de fosfatase alcalina no sangue;
- Alteração na RNI (exame que avalia a coagulação do sangue);
- Zumbido.
Reações adversas raras (0,01 a < 0,1%):
- Ritmo cardíaco anormal (prolongamento do QT);
- Lesão renal com perda de grande quantidade de proteína na urina (síndrome nefrótica);
- Hepatite induzida por medicamentos* (inflamação do fígado, que pode causar náuseas, vômitos, dor abdominal e icterícia).
Outros efeitos adversos, observados na experiência pós-comercialização:
A frequência desses eventos não pode ser estimada a partir dos dados disponíveis.
- Dermatite de “recall” induzida por radiação (lesão cutânea que pode ocorrer em local exposto previamente a radioterapia. Pode ser um evento grave);
- Síndrome de Stevens-Johnson e necrólise epidérmica tóxica* (condição grave que apresenta-se como vermelhidão, erupção e bolhas dolorosas na pele e nas membranas mucosas, incluindo descolamento extenso da pele);
- Vasculite leucocitoclástica (inflamação de vasos da pele que pode causar manifestações cutâneas);
- Angioedema (reação alérgica com edema (p. ex., de face e língua) que pode causar dificuldade para respirar ou engolir);
- Rabdomiólise (destruição anormal de células musculares que pode levar a problemas renais);
- Eventos do tipo doença pulmonar intersticial (inflamação dos pulmões).
*Essas reações adversas podem ser potencialmente fatais ou fatais. São incomuns ou têm incidência mais baixa que incomum.
Adicionalmente, os seguintes eventos adversos significativos foram relatados de modo infrequente durante os estudos clínicos de Nexavar:
Ataque isquêmico transitório, arritmia cardíaca (distúrbios do ritmo cardíaco) e tromboembolismo (formação de coágulos dentro dos vasos e seu desprendimento). Para esses eventos não se estabeleceu uma relação causal com Nexavar.
Alterações de exames laboratoriais:
Nexavar pode alterar os resultados de exames laboratoriais, portanto quando for realizar algum tipo de exame de laboratório, informe que está tomando Nexavar.
Atenção: este produto é um medicamento que possui nova indicação terapêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
População Especial
Gravidez e lactação
Deve-se evitar a gravidez durante o tratamento com Nexavar. Informe imediatamente seu médico em caso de suspeita de gravidez, pois este medicamento pode causar danos ao feto, que incluem malformação grave, desenvolvimento insuficiente e morte. Deve-se utilizar medidas eficazes para prevenir a gravidez durante o tratamento e por pelo menos 2 semanas após o término do tratamento. Nexavar não deve ser usado durante a gravidez.
O médico irá considerar o uso deste medicamento por mulheres grávidas quando os possíveis benefícios justificarem os possíveis riscos para o feto.
A amamentação deve ser interrompida durante o tratamento com Nexavar.
Os resultados de estudos em animais indicam que sorafenibe pode prejudicar a fertilidade masculina e feminina.
Dirigir veículos e operar máquinas
Não foram conduzidos estudos sobre o efeito de Nexavar na habilidade de dirigir veículos ou de operar máquinas.
Pacientes idosos (acima de 65 anos), gênero e peso corporal
Nenhum ajuste de dose é necessário com base na idade (acima de 65 anos), no gênero ou no peso corporal do paciente.
Uso em crianças
A segurança e a eficácia de Nexavar em pacientes pediátricos não foram estabelecidas.
Pacientes com insuficiência hepática
Não há necessidade de ajuste de dose em pacientes com insuficiência hepática Child-Pugh A ou B Não se estudou Nexavar em pacientes com insuficiência hepática Child-Pugh C.
Pacientes com insuficiência renal
Não há necessidade de ajuste de dose em pacientes com insuficiência renal leve, moderada ou grave que não requeira diálise. Nexavar não foi estudado em pacientes que estejam sendo submetidos à diálise. É recomendável que o médico monitore o equilíbrio hidroeletrolítico nos pacientes com risco de disfunção renal.
Composição
Cada comprimido de Nexavar contém:
274mg de tosilato de sorafenibe correspondente a 200mg de sorafenibe.
Excipientes: croscarmelose sódica, celulose microcristalina, hipromelose, laurilsulfato de sódio, estearato de magnésio, macrogol, dióxido de titânio e óxido férrico vermelho.
Superdosagem
Não existe tratamento específico em caso de superdose de Nexavar. A dose mais alta de Nexavar estudada clinicamente foi de 4 comprimidos (800mg) duas vezes ao dia.
A ingestão de uma quantidade maior do que a indicada de Nexavar pode tornar os efeitos adversos mais prováveis ou mais graves, especialmente diarreia e reações dermatológicas. Na suspeita de superdose, deve-se interromper o uso de Nexavar e consultar seu médico imediatamente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Indutores do CYP3A4
A administração concomitante contínua de sorafenibe e rifampicina reduziu a AUC de sorafenibe em 37%, em média. Outros indutores da atividade do CYP3A4 (por exemplo, Hypericum perforatum, conhecido como Erva de São João, fenitoína, carbamazepina, fenobarbital e dexametasona) também podem aumentar o metabolismo do sorafenibe e consequentemente reduzir suas concentrações.
Inibidores do CYP3A4
O cetoconazol, um potente inibidor do CYP3A4, administrado uma vez ao dia durante 7 dias a voluntários sadios do sexo masculino, não alterou a AUC média de uma dose única de 50 mg de sorafenibe.
Portanto, as interações farmacocinéticas clínicas de sorafenibe com os inibidores de CYP3A4 são improváveis.
Substratos do CYP2C9
Avaliou-se o possível efeito de sorafenibe sobre a varfarina (um substrato do CYP2C9) em pacientes que receberam sorafenibe em comparação com pacientes que receberam placebo. O tratamento concomitante com sorafenibe e varfarina não resultou em alterações no TP (tempo de protrombina) RNI médio em comparação com placebo. Entretanto, é necessário monitorar regularmente a RNI de pacientes que tomam varfarina.
Substratos seletivos de isoformas CYP
A administração concomitante de midazolam, dextrometorfano e omeprazol, substratos dos citocromos CYP3A4, CYP2D6 e CYP2C19 respectivamente, após 4 semanas de administração de sorafenibe, não alterou a exposição a esses agentes, indicando que o sorafenibe não inibe nem induz as isoenzimas do citocromo P450. Em um estudo clínico separado, a administração concomitante de sorafenibe e paclitaxel resultou em um aumento, ao invés de diminuição, da exposição ao 6-OH paclitaxel, metabólito ativo do paclitaxel formado pelo CYP2C8. Esses dados sugerem que o sorafenibe pode não ser um inibidor in vivo do CYP2C8. Em outro estudo clínico, a administração concomitante de sorafenibe e ciclofosfamida resultou em uma pequena diminuição na exposição à ciclofosfamida, mas não diminuiu a exposição sistêmica à 4-OH ciclofosfamida, metabólito ativo da ciclofosfamida formado principalmente pelo CYP2B6. Esses dados sugerem que o sorafenibe pode não ser um inibidor in vivo do CYP2B6.
Substratos da proteína transportadora gp-P (glicoproteína-P)
O sorafenibe demonstrou inibir a proteína transportadora glicoproteína-P (gp-P) in vitro. O aumento das concentrações plasmáticas dos substratos de gp-P, como a digoxina, não pode ser excluído com o tratamento concomitante com sorafenibe.
Combinação com outros agentes antineoplásicos
Em estudos clínicos, administrou-se sorafenibe em combinação com uma série de outros agentes antineoplásicos nas suas posologias habituais, incluindo gencitabina, cisplatina, oxaliplatina, paclitaxel, carboplatina, capecitabina, doxorrubicina, docetaxel, irinotecano e ciclofosfamida. O sorafenibe não teve efeito clinicamente relevante na farmacocinética da gencitabina, cisplatina, carboplatina, oxaliplatina ou ciclofosfamida.
Paclitaxel / carboplatina
A administração de paclitaxel (225 mg/m2) e carboplatina (AUC = 6) com sorafenibe (? 400 mg duas vezes ao dia), administrados com uma pausa de 3 dias na administração de sorafenibe para administração de paclitaxel / carboplatina, não resultou em efeito significativo na farmacocinética do paclitaxel.
A coadministração de paclitaxel (225 mg/m2, uma vez a cada 3 semanas) e carboplatina (AUC = 6) com sorafenibe (400 mg duas vezes ao dia, sem pausa na administração de sorafenibe) resultou em um aumento de 47% da exposição ao sorafenibe, 29% da exposição ao paclitaxel e 50% da exposição ao 6-OH paclitaxel.
A farmacocinética da carboplatina não foi afetada.
Esses dados indicam que não é necessário ajuste de dose quando paclitaxel e carboplatina são coadministrados com sorafenibe com pausa de 3 dias na administração de sorafenibe. A relevância clínica do aumento da exposição ao sorafenibe e paclitaxel, após a coadministração sem pausa de sorafenibe é desconhecida.
Capecitabina
A coadministração de capecitabina (750 – 1.050 mg/m2, duas vezes ao dia, dias 1 – 14 a cada 21 dias) e sorafenibe (200 ou 400 mg duas vezes ao dia, administração contínua ininterrupta) não resultou em alteração significativa na exposição ao sorafenibe, mas em um aumento de 15 – 50% na exposição da capecitabina e um aumento de 0 – 52% na exposição ao 5-FU. A relevância clínica deste aumento leve a moderado na exposição da capecitabina e 5-FU quando coadministrados com sorafenibe é desconhecida.
Doxorrubicina / irinotecano
O tratamento concomitante com sorafenibe resultou em aumento de 21% na AUC da doxorrubicina. Quando se administrou com irinotecano, cujo metabólito ativo SN-38 é adicionalmente metabolizado pela via UGT1A1, produziu-se aumento de 67 – 120% da AUC do SN-38 e aumento de 26 – 42% da AUC do irinotecano. Não se conhece a relevância clínica desses resultados.
Docetaxel
A coadministração de sorafenibe (200 mg duas vezes/dia ou 400 mg duas vezes/dia, administrados do 2° ao 19° dias de cada ciclo de 21 dias) e de docetaxel (75 ou 100 mg/m², administrado uma vez a cada 21 dias) com uma pausa de 3 dias em torno da administração de docetaxel resultou em um aumento de 36 – 80% na AUC de docetaxel e de 16–32% na Cmáx de docetaxel. Recomenda-se cautela ao administrar sorafenibe com docetaxel.
Combinação com antibióticos
Combinação com inibidores da bomba de prótons
Interação Alimentícia
Veja “Posologia e Modo de Usar”.
Ação da Substância
Resultados de eficácia
A segurança e eficácia de Tosilato de Sorafenibe (substância ativa) foram estudadas em pacientes com carcinoma hepatocelular (CHC), em pacientes com carcinoma de células renais (CCR) avançado e em pacientes com carcinoma de tireoide diferenciado (CTD).
Carcinoma hepatocelular
Carcinoma de células renais
A segurança e eficácia de Tosilato de Sorafenibe (substância ativa) no tratamento de carcinoma de células renais avançado (CCR) foram estudadas nos dois estudos clínicos controlados randomizados a seguir.
Carcinoma de Tireoide Diferenciado
O estudo 4 (14295) foi um estudo fase III, internacional, multicêntrico, randomizado, duplo cego, controlado com placebo, em 417 pacientes com carcinoma de tireoide diferenciado (CTD) localmente avançado ou metastático, refratário a iodo radioativo (RAI).
O desfecho primário do estudo foi a sobrevida livre de progressão (SLP). Os desfechos secundários incluíram a sobrevida global (SG), a taxa de resposta tumoral e a duração da resposta. Os pacientes que apresentaram progressão foram autorizados a receber Tosilato de Sorafenibe (substância ativa) em esquema aberto. Não foi permitido tratamento concomitante com iodo radioativo.
O estudo de fase III (14295) recrutou pacientes com CTD histologicamente comprovado, localmente avançado ou metastático, refratário ao tratamento com iodo radioativo que tinham progredido de acordo com RECIST nos 14 meses anteriores ao recrutamento. CTD refratário a iodo radioativo foi definido como presença de uma lesão não captante de iodo em um scan com iodo radioativo, ou utilização de doses radioativas ? 600 mCi de iodo radioativo, ou progressão após tratamento com iodo radioativo dentro de 16 meses após o início do recrutamento ou após dois tratamentos com iodo radioativo separados por intervalos de 16 meses.
As características demográficas e dos pacientes no período basal foram bem balanceadas entre os dois grupos de tratamento. Oitenta e seis por cento (86%) dos pacientes apresentavam metástases nos pulmões, 51% nos linfonodos e 27% nos ossos. Quase todos os pacientes haviam sido submetidos à tireoidectomia (99,5%) e haviam recebido radioatividade cumulativa mediana de aproximadamente 400 mCi. A maioria dos pacientes tinha carcinoma papilífero (56,8%), seguido por carcinoma folicular (25,4%) e carcinoma pouco diferenciado (9,6%). Os pacientes incluídos no estudo apresentaram “performance status” ECOG 0,1,2 sendo que aproximadamente 60% dos pacientes apresentaram “performance status” ECOG 0.
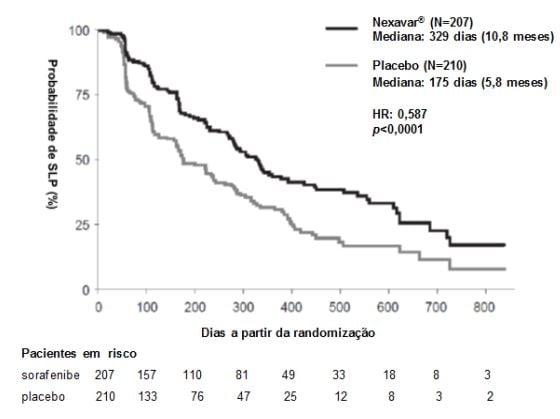
O conjunto completo para análise incluiu 207 pacientes randomizados para Tosilato de Sorafenibe (substância ativa) 400 mg duas vezes ao dia e 210 pacientes randomizados para placebo. A SLP foi avaliada por revisão radiológica independente, cega, com base nos critérios RECIST. A mediana do tempo de SLP foi de 329 dias (10,8 meses) no grupo Tosilato de Sorafenibe (substância ativa) comparada a 175 dias (5,8 meses) no grupo placebo. O risco relativo para a SLP (progressão da doença ou morte) foi reduzido em aproximadamente 41% nos pacientes que receberam sorafenibe em comparação com os indivíduos que receberam placebo (relação de risco [“Hazard Ratio” (HR)] = 0,587, Intervalo de confiança (IC) 95%: 0,454; 0,758; p unilateral <0,0001). (Tabela 2, Figura 2)
Não houve diferença estatística significamente na sobrevida global entre os grupos de tratamento (a HR foi 0,884, IC 95%: 0,633; 1,236, valor p unilateral de 0,236, Tabela 2) na análise da sobrevida global realizada 9 meses após a data de corte da análise final de SLP. A SG mediana não foi alcançada no braço sorafenibe e foi de 36,5 meses no braço placebo. Cento e cinquenta e sete (75%) pacientes randomizados para placebo e 61 (30%) randomizados para Tosilato de Sorafenibe (substância ativa) receberam Tosilato de Sorafenibe (substância ativa) em esquema aberto. A duração mediana da terapia no período duplo cego foi de 46 semanas (faixa 0,3 – 135) para pacientes recebendo sorafenibe e 28 semanas (faixa 1,7 – 132) para pacientes recebendo placebo. Não foi observada resposta completa (RC) de acordo com RECIST. A taxa de resposta global (RC + resposta parcial (RP)), por avaliação radiológica independente, foi mais alta no grupo de Tosilato de Sorafenibe (substância ativa) (24 pacientes, 12,2%) do que no grupo placebo (um paciente, 0,5%), p unilateral <0,0001. A duração mediana da resposta foi de 309 dias (IC 95%: 226, 505 dias) entre os pacientes que receberam Tosilato de Sorafenibe (substância ativa) e apresentaram RP.
Uma análise de subgrupo “post-hoc” sobre o tamanho máximo do tumor mostrou um efeito do tratamento para sobrevida livre de progressão favorecendo o sorafenibe com relação ao placebo para pacientes com tamanho máximo de tumor de 1,5 cm ou maior (HR 0,54; IC 95%: 0,41 – 0,71), enquanto um efeito numericamente menor foi relatado em pacientes com tamanho máximo de tumor menor que 1,5 cm (HR 0,87; IC 95%: 0,40 – 1,89).
Uma análise de subgrupo “post-hoc” sobre os sintomas iniciais (“baseline”) do carcinoma de tireoide mostrou um efeito do tratamento para sobrevida livre de progressão favorecendo o sorafenibe com relação ao placebo para pacientes sintomáticos e assintomáticos. O HR da sobrevida livre de progressão foi de 0,39 (IC 95%: 0,21 – 0,72) para pacientes com sintomas inciais (“baseline”) e de 0,60 (IC 95%: 0,45 – 0,81) para pacientes sem sintomas inciais (“baseline”).
Tabela 2: Resultados de eficácia do estudo 4 em carcinoma de tireoide diferenciado:
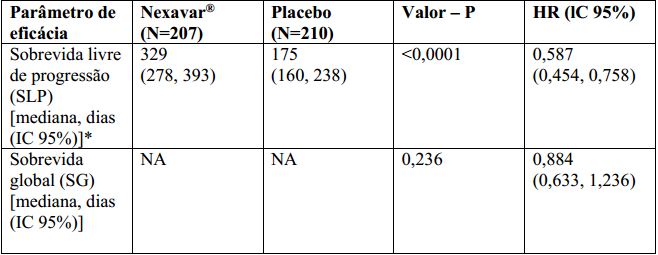 NA = Não alcançado IC = Intervalo de confiança, HR = “Hazard Ratio” (Tosilato de Sorafenibe (substância ativa) sobre placebo).
NA = Não alcançado IC = Intervalo de confiança, HR = “Hazard Ratio” (Tosilato de Sorafenibe (substância ativa) sobre placebo).
*Revisão radiológica independente.
Figura 2: Curva de Kaplan-Meier de sobrevida livre de progressão (SLP) em carcinoma de tireoide no estudo 4 (Conjunto completo para análise):
Características Farmacológicas
Farmacodinâmica
O sorafenibe é um inibidor de proteínas quinases.
Farmacocinética
Informações adicionais para populações especiais
Dados de segurança pré-clínicos
O perfil de segurança pré-clínico de sorafenibe foi avaliado em camundongos, ratos, cães e coelhos.
Cuidados de Armazenamento
Nexavar deve ser guardado na sua embalagem original protegido da umidade e à temperatura ambiente (entre 15°C e 30°C).
Características organolépticas
Nexavar apresenta-se na forma de comprimido redondo de cor vermelha, sem cheiro característico.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Dizeres Legais
MS-1.7056.0029
Farm. Resp.:
Dra. Dirce Eiko Mimura
CRF-SP n° 16532
Fabricado por:
Bayer Pharma AG
Leverkusen - Alemanha
Importado por:
Bayer S.A.
Rua Domingos Jorge, 1.100
04779-900 - Socorro – São Paulo - SP
C.N.P.J. nº 18.459.628/0001-15
Venda sob prescrição médica.
informações complementares
| Fabricante |
| BAYER |
| Princípio ativo |
| Tosilato De Sorafenibe |
| Categoria do medicamento |
| Medicamentos Especiais |
