- Home
- Medicamentos
- Medicamentos Especiais
- Zytiga - 250Mg 120 Comprimidos...
- Bula de Zytiga - 250Mg 120 Comprimidos...
para o que é indicado e para que serve?
Para que serve Zytiga, em combinação com os medicamentos prednisona ou prednisolona, é indicado para:Continue lendo...
ofertas de Zytiga - 250Mg 120 Comprimidos

ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
Zytiga, em combinação com os medicamentos prednisona ou prednisolona, é indicado para:
- O tratamento de pacientes com câncer de próstata que se espalhou para outras partes do corpo, que não apresentam sintomas ou apresentam sintomas leves, após falha à terapia de privação de androgênios (um hormônio sexual);
- O tratamento de pacientes com câncer de próstata que se espalhou para outras partes do corpo e que já receberam quimioterapia com o medicamento docetaxel.
Como Zytiga funciona?
Zytiga inibe seletivamente uma enzima necessária para a produção de androgênios (hormônios sexuais) pelos testículos, glândulas suprarrenais e tumores da próstata. Assim, Zytiga diminui consideravelmente os níveis destes hormônios, os quais levam à progressão da doença.
A concentração de testosterona (um hormônio sexual) no sangue é reduzida dentro de 12 horas após o primeiro uso do medicamento.
Contraindicação
Não tome Zytiga se você estiver grávida ou se houver suspeita de gravidez.
Como usar
A dose recomendada de Zytiga é de quatro comprimidos de 250 mg ao dia, em uma única tomada. Não exceder a dose máxima diária de 1000 mg (quatro comprimidos de 250 mg).
Não tome Zytiga com as refeições. Zytiga deve ser tomado pelo menos 2 horas após a refeição e nenhum alimento deve ser ingerido durante pelo menos 1 hora após a tomada.
A tomada de Zytiga com alimentos provoca absorção maior do que a necessária pelo corpo e isto pode provocar efeitos colaterais.
Os comprimidos de Zytiga devem ser ingeridos inteiros, com água. Não quebre os comprimidos.
O tratamento com Zytiga é realizado em combinação com prednisona ou prednisolona.
A dose usual de prednisona ou prednisolona é 5 mg duas vezes ao dia, utilizados conforme a orientação do seu médico. Recomenda-se que os pacientes sejam mantidos em tratamento até que haja a progressão dos valores de PSA (Antígeno Prostático Específico) no sangue associada à progressão radiográfica e sintomática ou clínica. Converse com seu médico.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Este medicamento não deve ser partido, aberto ou mastigado.
Precauções
Zytiga pode provocar aumento da pressão arterial sanguínea ou insuficiência do coração ou diminuição dos níveis de potássio no sangue ou piorar estas condições clínicas pré-existentes.
A tomada da prednisona ou prednisolona com Zytiga ajuda a evitar a piora destas condições. Se você tiver alguma das condições mencionadas ou outros problemas do coração ou de vasos sanguíneos, converse com seu médico.
Se você tiver relações sexuais com uma mulher grávida, você precisa usar preservativo (camisinha). Se você tiver relações sexuais com uma mulher que pode ficar grávida, você deve usar preservativo e outro método contraceptivo eficaz para evitar a gravidez.
Zytiga pode afetar o fígado. Informe seu médico se você tiver problemas no fígado. Enquanto você estiver tomando Zytiga, seu médico solicitará exames de sangue para verificar os efeitos do medicamento sobre o seu fígado. Caso isso aconteça pode haver a necessidade de interromper o tratamento e/ou reduzir a dose.
Siga sempre a orientação do seu médico quanto à dose a ser tomada.
Gravidez e amamentação
Zytiga não deve ser tomado por mulheres grávidas ou amamentando ou que possam ficar grávidas, uma vez que Zytiga pode afetar o bebê.
Se você estiver grávida ou suspeitar que possa estar grávida, use luvas se for preciso tocar ou manusear os comprimidos de Zytiga.
Doença renal
Zytiga pode ser usado caso você tenha alguma doença renal.
Doença hepática
Você não deve tomar Zytiga caso apresente doença moderada ou grave do fígado. Se o seu problema no fígado for leve, o médico decidirá se você pode tomar este medicamento.
Efeitos sobre a capacidade de dirigir veículos e operar máquinas
Não é esperado que Zytiga afete sua capacidade de dirigir ou operar máquinas.
Interações medicamentosas
Para reduzir a chance de você apresentar pressão alta ou efeitos no coração ou nível baixo de potássio no sangue, seu médico irá prescrever prednisona ou prednisolona. Você deve tomar um destes medicamentos diariamente enquanto estiver tomando Zytiga.
Não interrompa a tomada de prednisona ou prednisolona a não ser que seu médico recomende. Durante uma emergência médica, pode ser necessário aumentar a dose de prednisona ou prednisolona. Se isto ocorrer, seu médico irá observá-lo e orientá-lo sobre como proceder.
Seu médico poderá solicitar que você continue com outros tratamentos durante o tratamento com Zytiga e prednisona ou prednisolona.
A tomada de Zytiga com outros medicamentos pode resultar em efeitos maiores ou menores ou até mesmo em reações adversas a estes medicamentos. Alguns medicamentos como fenitoína, carbamazepina, rifampicina, rifabutina, rifapentina, fenobarbital, devem ser evitados ou usados com cautela durante o tratamento com Zytiga.
Informe ao seu médico sobre qualquer outro medicamento que você esteja utilizando, para que ele possa orientá-lo se você poderá continuar a usá-los ou se a dose deverá ser reduzida.
Interações com alimentos
Não tome Zytiga com alimentos. Zytiga deve ser tomado pelo menos 2 horas após a refeição e nenhum alimento deve ser ingerido durante pelo menos 1 hora após a tomada de Zytiga.
Os comprimidos de Zytiga devem ser ingeridos inteiros, com água. Se você tomar Zytiga com alimentos, uma quantidade maior do que a necessária do medicamento será absorvida pelo seu organismo e isto pode provocar o aparecimento de efeitos colaterais.
Interações com álcool e nicotina
Não há dados disponíveis sobre a interação de acetato de abiraterona e álcool ou nicotina.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Interrompa a tomada de Zytiga e procure atendimento médico imediatamente se você notar sinais de níveis baixos de potássio no sangue, tais como:
Fraqueza muscular, câimbras musculares e batidas rápidas ou irregulares do coração.
As reações adversas mais comuns a Zytiga são:
Inchaço nas pernas e pés, nível baixo de potássio no sangue, infecção urinária, pressão alta, aumentos nos níveis das transaminases do fígado (alanina aminotransferase e aspartato aminotransferase) – testes de função do fígado; indigestão (dispepsia), sangue na urina (hematúria) e fraturas ósseas.
Outros efeitos colaterais observados durante o tratamento com Zytiga são:
Níveis altos de gordura no sangue, dor no peito, distúrbios no batimento do coração, insuficiência do coração, batimento rápido do coração e problemas nas glândulas suprarrenais.
Outros efeitos adversos clinicamente relevantes, reportados foram uma irritação nos pulmões (também denominada alveolite alérgica), ruptura do tecido muscular (também denominada rabdomiólise) e fraqueza muscular e/ou dor muscular (também denominada miopatia).
Se estes ou outros eventos adversos ocorrerem, converse imediatamente com seu médico.
Composição
Cada comprimido contém:
250 mg de acetato de abiraterona, que corresponde a 223 mg de abiraterona.
Excipientes: lactose monoidratada, celulose microcristalina, croscarmelose sódica, povidona, laurilsulfato de sódio, estearato de magnésio, dióxido de silício coloidal.
Superdosagem
Durante os estudos clínicos conduzidos com Zytiga não foram observados casos de ingestão de dose excessiva do medicamento.
Não há antídoto específico para o acetato de abiraterona.
Se, acidentalmente, você tomar uma quantidade maior que a dose usual, a administração de Zytiga deve ser interrompida e você deve conversar com o médico. Se necessário, ele irá adotar medidas gerais, incluindo o monitoramento dos batimentos do coração e avaliará o funcionamento do seu fígado.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Potencial de outras drogas para afetar a exposição à abiraterona
Em um estudo clínico de interação farmacocinética em indivíduos saudáveis tratados previamente com um indutor forte de CYP3A4 (rifampicina, dose diária de 600 mg, por 6 dias), seguido de uma dose única de 1000 mg de acetato de abiraterona, houve redução de 55% na AUC? plasmática média de abiraterona.
Indutores fortes da CYP3A4 (por exemplo, fenitoína, carbamazepina, rifampicina, rifabutina, rifapentina e fenobarbital) devem ser evitados durante o tratamento com Acetato de Abiraterona (substância ativa), ou utilizados acompanhados de uma avaliação cuidadosa da eficácia clínica.
Em um estudo clínico de interação farmacocinética em indivíduos saudáveis, a coadministração de cetoconazol, um forte inibidor da CYP3A4, não teve efeito clínico significativo na farmacocinética da abiraterona.
Potencial do Zytiga para afetar a exposição a outras drogas
Interação Alimentícia
A administração de Acetato de Abiraterona (substância ativa) com alimentos aumenta significantemente a absorção do acetato de abiraterona. A eficácia e a segurança de Acetato de Abiraterona (substância ativa) administrado com alimento não foram estabelecidas. Acetato de Abiraterona (substância ativa) não deve ser tomado com alimentos.
Não há dados disponíveis sobre a interação de acetato de abiraterona e álcool.
Ação da Substância
Resultados de eficácia
A eficácia de Acetato de Abiraterona (substância ativa) foi estabelecida em dois estudos clínicos fase 3 (estudos 301 e 302), multicêntricos, randomizados, controlados com placebo em pacientes com câncer de próstata metastático e resistente à castração.
O estudo 302 incluiu pacientes que não haviam recebido quimioterapia prévia e eram assintomáticos ou levemente sintomáticos, enquanto que o estudo 301 incluiu pacientes que já tinham recebido quimioterapia prévia contendo docetaxel. Em ambos os estudos os pacientes estavam em uso de agonistas de LHRH (hormônio liberador do hormônio luteinizante) ou haviam sido submetidos previamente à orquiectomia. Nos braços experimentais, Acetato de Abiraterona (substância ativa) foi administrado na dose de 1000 mg ao dia, associado a uma dose baixa de prednisona ou prednisolona de 5 mg duas vezes ao dia. Os pacientes do grupo controle receberam placebo e dose baixa de prednisona ou prednisolona de 5 mg duas vezes ao dia.
Devido ao fato de que as alterações na concentração sérica do Antígeno Prostático Específico (PSA) nem sempre podem prever um benefício clínico, em ambos os estudos os pacientes foram mantidos em tratamento com Acetato de Abiraterona (substância ativa) até atingirem critério para descontinuação, conforme especificado para cada estudo abaixo.
Estudo 302 (pacientes assintomáticos ou levemente sintomáticos que não receberam quimioterapia prévia)
No estudo 302, (n = 1.088) a mediana de idade dos pacientes incluídos foi de 71 anos para os pacientes tratados com Acetato de Abiraterona (substância ativa) associado à prednisona ou prednisolona e 70 anos para os pacientes tratados com placebo mais prednisona ou prednisolona. O “performance status ECOG” (Eastern Cooperative Oncology Group) era de 0 em 76% dos pacientes e de 1 em 24% dos pacientes em ambos braços. Os pacientes com metástase visceral foram excluídos. Os desfechos de eficácia co-primários foram sobrevida global e sobrevida livre de progressão radiográfica (rPFS). Uma avaliação de dor na linha de base foi de 0-1 (assintomático) em 66% pacientes e 2-3 (levemente sintomático) em 26% dos pacientes, conforme definido pelo Formulário Abreviado da Dor (Brief Pain Inventory-Short Form) (pior dor ao longo das últimas 24 horas). Além da avaliação dos desfechos co-primários, a eficácia também foi avaliada observando-se o tempo até o uso de opiáceos para o controle da dor oncológica, o tempo para início de quimioterapia citotóxica, o tempo para queda no escore de “performance status ECOG” em ? 1 ponto e o tempo para progressão do PSA conforme os critérios do “Prostate Cancer Working Group-2” (PCWG2).
No estudo 302, os tratamentos foram descontinuados no momento de progressão clínica inquestionável. Os tratamentos também podiam ser descontinuados no momento de progressão radiográfica confirmada, a critério do investigador.
A sobrevida livre de progressão radiográfica (rPFS) foi avaliada empregando-se exames de imagens sequenciais, definidas pelos critérios de PCWG2 (para lesões ósseas) e “Response Evaluation Criteria In Solid Tumors” (RECIST) modificado (para lesões em partes moles). A análise da rPFS utilizou uma avaliação da progressão radiográfica revisada em laboratório central.
Na análise de rPFS planejada houveram 401 eventos; 150 (28%) em pacientes tratados com Acetato de Abiraterona (substância ativa) e 251 (46%) dos pacientes tratados com placebo tiveram evidência radiográfica de progressão ou vieram a óbito. Uma diferença significativa na rPFS entre os grupos de tratamento foi observada (ver Tabela 1 e Figura 1).
Tabela 1 Estudo 302 - Sobrevida Livre de Progressão Radiográfica em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia:
| ZYTIGA (n= 546) | Placebo (n= 542) | |
| Sobrevida Livre de Progressão Radiográfica (rPFS) | ||
| Progressão ou óbito | 150 (28%) | 251 (46%) |
| rPFS (mediana em meses) | Não atingido | 8,3 |
| (IC de 95%) | 11,66; NE | (8,12; 8,54) |
| Valor de p* | <0,0001 | |
| Razão de risco** | 0,425 | |
| (IC de 95%) | (0,347; 0,522) | |
NE = Não Estimado.
* O valor de p é derivado de um teste de log-rank estratificado pelo escore ECOG basal (0 ou 1).
** Razão de risco <1 favorece Acetato de Abiraterona (substância ativa).
Figura 1: Curvas de sobrevida livre de progressão radiográfica pelo método de Kaplan-Meier em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associado a agonistas de LHRH ou orquiectomia prévia:
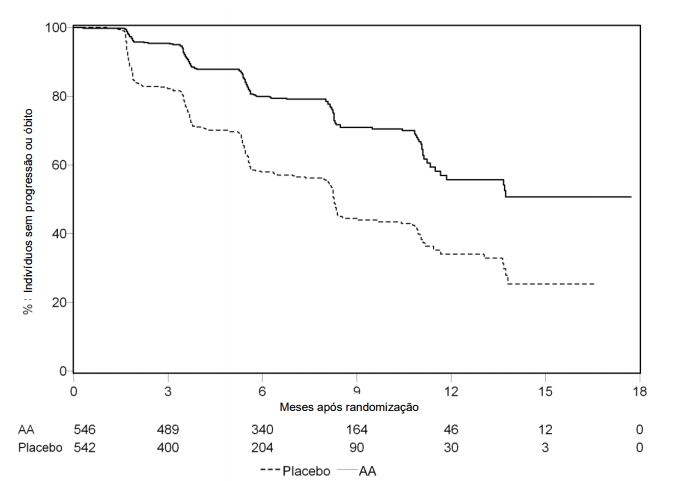
Tabela 2: Estudo 302 - Sobrevida Livre de Progressão Radiográfica em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia (no momento da segunda análise interina de sobrevida global – revisão do investigador):
| ZYTIGA (n= 546) | Placebo (n= 542) | |
| Sobrevida Livre de Progressão Radiográfica (rPFS) | ||
| Progressão ou óbito | 271 (50%) | 336 (62%) |
| rPFS (mediana em meses) | 16,5 | 8,3 |
| (IC de 95%) | (13,80; 16,79) | (8,05; 9,43) |
| Valor de p* | <0,0001 | |
| Razão de risco** | 0,530 | |
| (IC de 95%) | (0,451; 0,623) | |
* O valor de p é derivado de um teste de log-rank estratificado pelo escore ECOG basal (0 ou 1);
** Razão de risco <1 favorece Acetato de Abiraterona (substância ativa).
Figura 2: Curvas de sobrevida livre de progressão radiográfica pelo método de Kaplan-Meier em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associado a agonistas de LHRH ou orquiectomia prévia (no momento da segunda análise interina de sobrevida global – revisão do investigador):
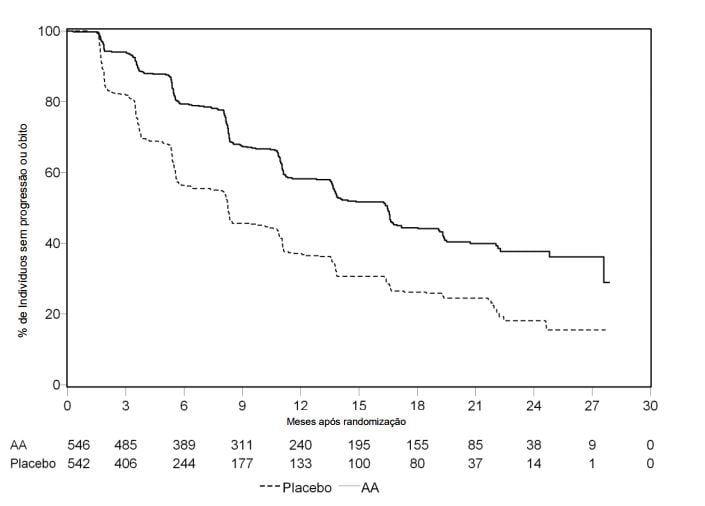
AA=Acetato de Abiraterona (substância ativa)
Foi realizada uma análise da sobrevida global planejada após a ocorrência de 333 óbitos. O estudo foi aberto com base na magnitude do benefício clínico observado. Vinte e sete por cento (147 de 546) dos pacientes tratados com Acetato de Abiraterona (substância ativa) foram a óbito, comparado com 34% (186 de 542) dos pacientes tratados com placebo. A sobrevida global foi maior para Acetato de Abiraterona (substância ativa) do que para o placebo, com uma redução no risco de morte de 25% (Razão de risco = 0,752; IC 95%: 0,606 – 0,934). O valor de p foi de 0,0097, que não atingiu o valor pré-especificado para significância estatística (ver Tabela 3 e Figura 3).
Tabela 3: Estudo 302 - Sobrevida Global em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia:
| ZYTIGA (n= 546) | Placebo (n= 542) | |
| Sobrevida Livre de Progressão Radiográfica (rPFS) | ||
| Progressão ou óbito | 147 (27%) | 186 (34%) |
| rPFS (mediana em meses) | Não atingido | 27,2 |
| (IC de 95%) | (NE; NE) | (25,95; NE) |
| Valor de p* | 0,0097 | |
| Razão de risco** | 0,752 | |
| (IC de 95%) | (0,606; 0,934) | |
NE = Não Estimado;
* O valor de p é derivado de um teste de log-rank estratificado pelo escore ECOG basal (0 ou 1);
** Razão de risco <1 favorece Acetato de Abiraterona (substância ativa).
Figura 3: Curvas de sobrevida pelo método de Kaplan-Meier em pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia:
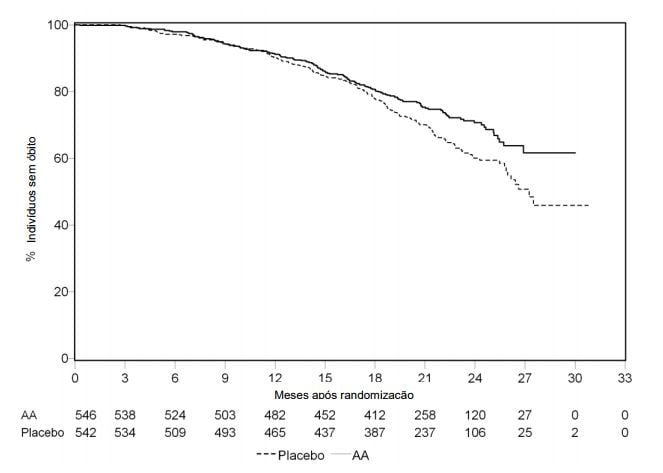
AA = Acetato de Abiraterona (substância ativa).
Além das melhoras observadas na sobrevida global e rPFS foram observados benefícios do tratamento com Acetato de Abiraterona (substância ativa) quando comparado ao placebo em todas as medidas de desfechos secundários prospectivamente definidas, como segue:
Os seguintes desfechos do estudo demonstraram uma vantagem estatisticamente significativa em favor do tratamento com Acetato de Abiraterona (substância ativa)
Estudo 301 (pacientes que receberam quimioterapia prévia)
Onze por cento (11%) dos pacientes incluídos no estudo 301 tinham “performance status ECOG” (Eastern Cooperative Oncology Group) igual a 2; 70% tinham evidência radiográfica de progressão da doença com ou sem progressão do PSA; 70% haviam recebido um esquema de quimioterapia citotóxica anteriormente e 30% haviam recebido dois. Metástase hepática estava presente em 11% dos pacientes tratados com Acetato de Abiraterona (substância ativa).
Foi recomendado que os pacientes continuassem recebendo os respectivos medicamentos do estudo até que houvesse progressão do PSA (25% de aumento confirmado em relação ao nível basal/nadir do paciente), em conjunto com a progressão radiográfica definida no protocolo e a progressão sintomática ou clínica. O desfecho primário de eficácia foi a sobrevida global.
Em uma análise planejada conduzida após a ocorrência de 552 óbitos, 42% (333 de 797) dos pacientes tratados com Acetato de Abiraterona (substância ativa) morreram em comparação com 55% (219 de 398) dos pacientes tratados com placebo. Uma melhora estatisticamente significativa na mediana da sobrevida global foi observada em pacientes tratados com Acetato de Abiraterona (substância ativa) (veja Tabela 4 e Figura 4). Uma análise de sobrevida atualizada foi conduzida quando 775 óbitos foram observados (97% do número planejado de óbitos para a análise final). Os resultados desta análise de sobrevida atualizada foram consistentes com a primeira análise de sobrevida (ver Tabela 4).
Tabela 4: Estudo 301 - Sobrevida global de pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia:
| ZYTIGA (n= 797) | Placebo (n= 398) | ||
| Análise de Sobrevida Primária | |||
| Óbito | 333 (42%) | 219 (55%) | |
| Sobrevida global mediana em meses (IC de 95%) | 14,8 (14,1; 15,4) | 10,9 (10,2; 12,0) | |
| Valor de p | <0,0001 | ||
| Razão de risco* | 0,646 (0,543; 0,768) | ||
| Análise de Sobrevida Atualizada | |||
| Óbito | 501 (63%) | 274 (69%) | |
| Sobrevida global mediana em meses (IC de 95%) | 15,8 (14,8; 17,0) | 11,2 (10,4; 13,1) | |
| Razão de risco*(IC de 95%) | 0,740 (0,638; 0,859) | ||
* Razão de risco <1 favorece Acetato de Abiraterona (substância ativa).
Em todos os pontos de avaliação após os primeiros meses de tratamento, uma proporção maior de pacientes tratados com Acetato de Abiraterona (substância ativa) continuava viva em comparação com a proporção de pacientes tratados com placebo (veja Figura 4).
Figura 4: Curvas de sobrevida pelo método de Kaplan-Meier de pacientes tratados com Acetato de Abiraterona (substância ativa) ou placebo em combinação com prednisona ou prednisolona associados a agonistas de LHRH ou orquiectomia prévia:
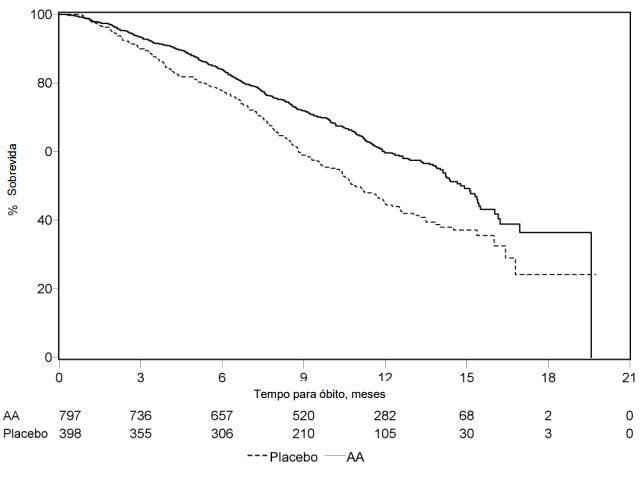
AA = Acetato de Abiraterona (substância ativa).
As análises de sobrevida por subgrupo mostraram um benefício consistente de sobrevida para o tratamento com Acetato de Abiraterona (substância ativa) (veja figura 5).
Figura 5: Sobrevida global por subgrupo: Razão de risco e intervalo de confiança de 95%:
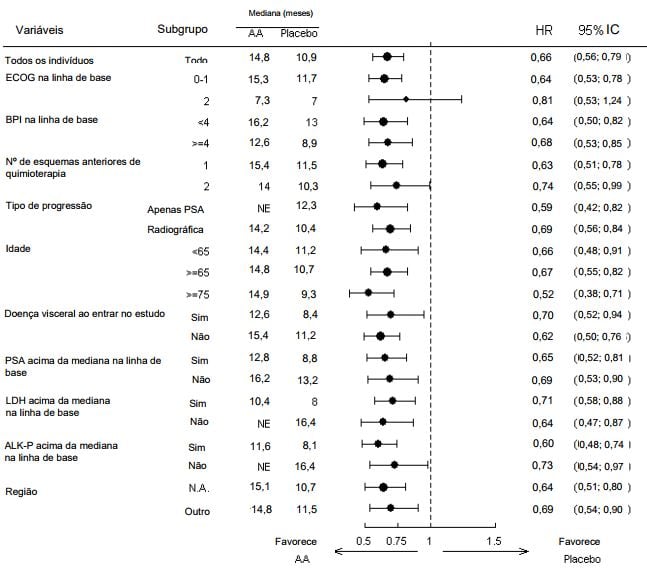
AA = Acetato de Abiraterona (substância ativa); ALK-P = fosfatase alcalina; BPI = Inventário Breve da Dor; IC = intervalo de confiança; ECOG = escore de desempenho do “Eastern Cooperative Oncology Group”; HR = razão de risco (do inglês Hazard Ratio).
LDH = desidrogenase lática.
NA = América do Norte.
NE = Não avaliável.
Além do aumento observado na sobrevida global, todos os desfechos secundários do estudo favoreceram Acetato de Abiraterona (substância ativa) e foram estatisticamente significativos depois do ajuste para multiplicidade.
Os pacientes que receberam Acetato de Abiraterona (substância ativa) demonstraram uma taxa de resposta do PSA total significativamente maior (definida como redução > 50% em relação à linha de base) em comparação com os pacientes que receberam o placebo: 38% versus 10%, p<0,0001.
O tempo mediano para progressão do PSA foi 10,2 meses para os pacientes tratados com Acetato de Abiraterona (substância ativa) e 6,6 meses para os pacientes tratados com placebo (Razão de risco = 0,580; IC 95%: [0,462; 0,728], p<0,0001).
A mediana de sobrevida livre de progressão radiográfica foi 5,6 meses para os pacientes tratados com Acetato de Abiraterona (substância ativa) e 3,6 meses para os pacientes que receberam placebo (Razão de risco = 0,673; IC 95%: [0,585; 0,776], p<0,0001).
Características farmacológicas
Propriedades Farmacodinâmicas
Propriedades Farmacocinéticas
Cuidados de Armazenamento
Você deve conservar Zytiga em temperatura ambiente (entre 15oC e 30oC).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Característica física
Os comprimidos de Zytiga têm formato oval e são brancos a quase brancos.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
MS- 1.1236.3401
Farm. Resp.:
Marcos R. Pereira – CRF/SP nº 12.304
Registrado por:
Janssen-Cilag Farmacêutica Ltda.
Avenida Presidente Juscelino Kubitschek, 2041, São Paulo – SP
CNPJ 51.780.468/0001-87
Fabricado por:
Patheon, Inc.,
Mississauga– Canadá
Importado e Embalado (emb. secundária) por:
Janssen-Cilag Farmacêutica Ltda.
Rodovia Presidente Dutra, km 154
São José dos Campos - SP
CNPJ 51.780.468/0002-68
Indústria Brasileira
Sac: 0800 701 1181
Venda sob prescrição médica.
informações complementares
| Fabricante |
| JANSSEN-CILAG |
| Princípio ativo |
| Acetato De Abiraterona |
| Categoria do medicamento |
| Medicamentos Especiais |
ZYTIGA - 250MG 120 COMPRIMIDOS É UM MEDICAMENTO, NÃO USE SEM PRESCRIÇÃO MÉDICA E ORIENTAÇÃO DO FARMACÊUTICO. AO PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
