- Home
- Medicamentos
- Medicamentos de A-Z
- Brilinta - 90Mg 60 Comprimidos...
- Bula de Brilinta - 90Mg 60 Comprimidos...
para o que é indicado e para que serve?
Para que serve Brilinta é indicado para a prevenção de eventos cardiovasculares caracterizados por trombose (coágulo dentro de um vaso sanguíneo), em pacientes que tiveram infarto do miocárdio (infarto) ou angina instável (dor no peito que ocorre no repouso).Continue lendo...
ofertas de Brilinta - 90Mg 60 Comprimidos

ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
Brilinta é indicado para a prevenção de eventos cardiovasculares caracterizados por trombose (coágulo dentro de um vaso sanguíneo), em pacientes que tiveram infarto do miocárdio (infarto) ou angina instável (dor no peito que ocorre no repouso).
Como o Brilinta funciona?
Brilinta ajuda a impedir o acúmulo de plaquetas (células muito pequenas presentes no sangue), reduzindo a possibilidade de formação de coágulos que podem bloquear um vaso sanguíneo. Isto significa que Brilinta reduz as chances de você ter outro infarto ou angina instável.
Brilinta demonstra um rápido início de ação. Ocorre inibição de quase metade da capacidade de formação do coágulo cerca de 30 minutos após dose inicial, atingindo efeito máximo entre 2-4 horas pósdose.
Contraindicação
Você não deve tomar Brilinta se tiver hipersensibilidade (alergia) ao ticagrelor ou a qualquer componente da fórmula.
Você não deve tomar este medicamento se tiver sangramento ativo, por exemplo, sangramento no estômago ou intestino devido a uma úlcera, histórico de sangramento intracraniano (dentro da cabeça) e/ou alterações graves no fígado.
Como usar
Você deve tomar os comprimidos de Brilinta com água, por via oral, com ou sem a ingestão de alimentos.
O tratamento de Brilinta deve ser iniciado com uma dose única de 180 mg (dois comprimidos de 90 mg) e então continuada com a dose de 90 mg duas vezes ao dia.
Os pacientes que estiverem utilizando Brilinta devem também tomar ácido acetilsalicílico diariamente, a menos que especificamente contraindicado. Após uma dose inicial de ácido acetilsalicílico, Brilinta deve ser utilizado com uma dose de manutenção de 75-150 mg de ácido acetilsalicílico.
Os médicos que desejam alterar a terapia dos pacientes de clopidogrel para Brilinta devem administrar a primeira dose de 90 mg de Brilinta 24 horas após a última dose do clopidogrel.
O tratamento é recomendado por pelo menos 12 meses, exceto se a interrupção do Brilinta for clinicamente indicada. Em pacientes com Síndrome Coronariana Aguda (SCA), a interrupção prematura com qualquer terapia antiplaquetária, incluindo Brilinta, poderia resultar em um aumento do risco de morte cardiovascular ou infarto do miocárdio devido a doença subjacente do paciente.
Posologia para populações especiais
Pacientes pediátricos:
A segurança e a eficácia em crianças abaixo de 18 anos de idade não foram estabelecidas.
Idosos:
Não é necessário ajuste de dose.
Pacientes com insuficiência renal (alterações nos rins):
Não é necessário ajuste de dose para pacientes com insuficiência renal. Não há informações disponíveis referente ao tratamento de pacientes em diálise renal (dos rins).
Pacientes com insuficiência hepática (alterações no fígado):
Não é necessário ajuste de dose para pacientes com insuficiência hepática leve. Brilinta não foi estudado em pacientes com insuficiência hepática moderada ou grave.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Os comprimidos de Brilinta não devem ser partidos ou mastigados.
O que devo fazer quando eu me esquecer de usar o Brilinta?
Se você esquecer de tomar uma dose de Brilinta, tome a dose seguinte no horário habitual.
Não tome uma dose em dobro (duas doses ao mesmo tempo) para compensar a dose esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico.
Precauções
Antes de usar Brilinta verifique com seu médico se você tem um risco aumentado de sangramento devido a:
- Um trauma recente, cirurgia recente (incluindo procedimentos odontológicos), sangramento gastrointestinal ativo ou recente, ou alterações moderadas no fígado O uso de BRILINTA é contraindicado se você estiver com sangramento ativo ou recente causado por alguma doença e se tiver histórico de sangramento intracraniano e alterações graves no fígado.
- Administração concomitante de medicamentos que podem aumentar o risco de sangramento (por exemplo, anti-inflamatórios não esteroidais, anticoagulantes orais e/ou fibrinolíticos dentro de 24 horas da dose de Brilinta).
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
As seguintes reações adversas foram identificadas nos estudos com Brilinta.
Reação muito comum (ocorre em 10% ou mais dos pacientes que utilizam este medicamento):
Alteração (aumento) no resultado de exame laboratorial referente aos níveis de ácido úrico, dispneia (ou falta de ar – sintoma no qual a pessoa tem desconforto ou dificuldade para respirar).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento):
Dor de cabeça, tontura, vertigem, epistaxe (sangramento nasal, pelas narinas), dor no abdômen, prisão de ventre, diarreia, dispepsia (indigestão – dificuldade na digestão dos alimentos), hemorragias gastrointestinais (sangramento no estômago ou intestino), náusea, vômito, sangramento na pele (dérmico ou subcutâneo), rash (erupção na pele com aspecto avermelhado), prurido (coceira no corpo), alteração (aumento) no resultado de exame laboratorial referente aos níveis de creatinina sanguínea, hemorragia pós-procedimento, sangramento do trato urinário.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
Confusão, hemorragia intracraniana, parestesia (sensação de formigamento/queimação na pele), hemorragia ocular (sangramento nos olhos), hemoptise (tosse com sangue), hemorragia retroperitoneal (sangramento no abdômen), gastrite (inflamação da mucosa do estômago).
Reação rara (ocorre em entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
Hemartrose (sangramento nas “juntas”).
As seguintes reações adversas foram identificadas no uso pós-comercialização de Brilinta:
Distúrbios do sistema imunológico, reações de hipersensibilidade (alergia), incluindo angioedema (inchaço) e distúrbios de pele e tecidos subcutâneos (rash). Uma vez que estas reações são reportadas voluntariamente, não é possível estimar com exatidão suas frequências.
Informe ao seu médico ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe a empresa sobre o aparecimento de reações indesejáveis e problemas com este medicamento, entrando em contato através do Sistema de Atendimento ao Consumidor (SAC).
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer reações adversas imprevisíveis ou desconhecidas. Nesse caso, informe seu médico ou cirurgião-dentista.
População Especial
Recomenda-se precaução em pacientes com risco aumentado de eventos bradicárdicos (frequência cardíaca baixa), sem marcapasso, ou síncope (perda abrupta da consciência).
Caso você sinta falta de ar durante o tratamento com Brilinta avise seu médico.
Efeito sobre a capacidade de dirigir veículos e operar máquinas
Não é esperado que Brilinta afete a capacidade de dirigir veículos e operar máquinas. Durante o tratamento do infarto ou da angina instável, pode ocorrer tontura e confusão. Se você tem esses sintomas, você deve ter cuidado ao dirigir veículos e operar máquinas.
Gravidez
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Antes de tomar Brilinta, fale com seu médico se você estiver grávida, tentando engravidar ou se estiver amamentando. O seu médico discutirá com você os riscos de tomar Brilinta durante este período.
Portadores de diabetes
Atenção: este medicamento contém manitol (126 mg/comprimido), portanto, deve ser usado com cautela e a critério médico em pacientes portadores de diabetes.
Brilinta contém manitol, que pode ter um leve efeito laxativo.
Composição
Cada comprimido revestido contém:
Ticagrelor: 90 mg.
Excipientes: manitol, fosfato de cálcio dibásico, amidoglicolato de sódio, hiprolose, estearato de magnésio, hipromelose, dióxido de titânio, talco, macrogol e óxido férrico amarelo.
Superdosagem
Tratamento
Em caso de ingestão de uma quantidade maior do medicamento que a prescrita pelo seu médico, você deve imediatamente entrar em contato com o seu médico e/ou ir a um hospital, levando a embalagem do medicamento com você.
Sintomas
Pode ocorrer um risco aumentado de sangramento, falta de ar e anormalidade dos batimentos cardíacos.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações sobre como proceder.
Interação Medicamentosa
Efeitos de outros medicamentos em Ticagrelor (substância ativa)
Efeitos de Ticagrelor (substância ativa) em outros medicamentos
Ação da Substância
Resultados de eficácia
Evidências clínicas
A eficácia de Ticagrelor (substância ativa) é procedente do estudo PLATO (PLATelet Inhibition and Patient Outcomes), um estudo comparativo de Ticagrelor (substância ativa) e clopidogrel, ambos administrados em combinação com ácido acetilsalicílico e outras terapias padrão.
O estudo PLATO foi um estudo randomizado, duplo-cego, de grupos paralelos, fase III, com 18.624 pacientes, que avaliou eficácia e segurança de Ticagrelor (substância ativa) comparado com clopidogrel para prevenção de eventos vasculares em pacientes com Síndrome Coronariana Aguda (angina instável, infarto agudo do miocárdio sem elevação do segmento ST [IAMSST] ou infarto agudo do miocárdio com elevação do segmento ST [IAMCST]).
O estudo foi composto de pacientes que se apresentaram no prazo de 24 horas do início do episódio mais recente da dor no peito ou sintomas relacionados. Os pacientes foram randomizados para receber clopidogrel (75 mg uma vez ao dia, com uma dose de ataque inicial de 300 mg se a terapia com tienopiridina não houvesse sido administrada anteriormente.
Uma dose de ataque adicional de 300 mg foi permitida, a critério do investigador), ou uma dose de ataque de 180 mg de Ticagrelor (substância ativa) seguido por uma dose de manutenção de 90 mg de Ticagrelor (substância ativa) duas vezes ao dia. Os pacientes poderiam ser controlados clinicamente, tratados com intervenção coronária percutânea (ICP) ou cirurgia de revascularização do miocárdio (RM).
Figura. Mostra a estimativa do risco para a primeira ocorrência de qualquer evento no desfecho composto de eficácia
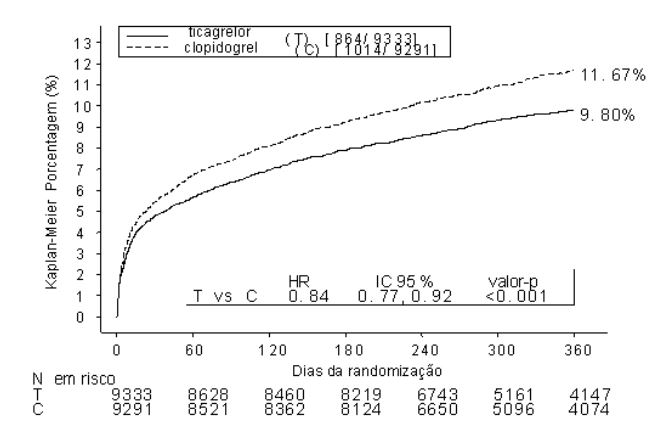
Ticagrelor (substância ativa) reduziu a ocorrência do desfecho composto primário comparado ao clopidogrel em ambas as populações AI/ IAMCST e IAMSST.
Tabela. Eventos de desfecho no estudo PLATO
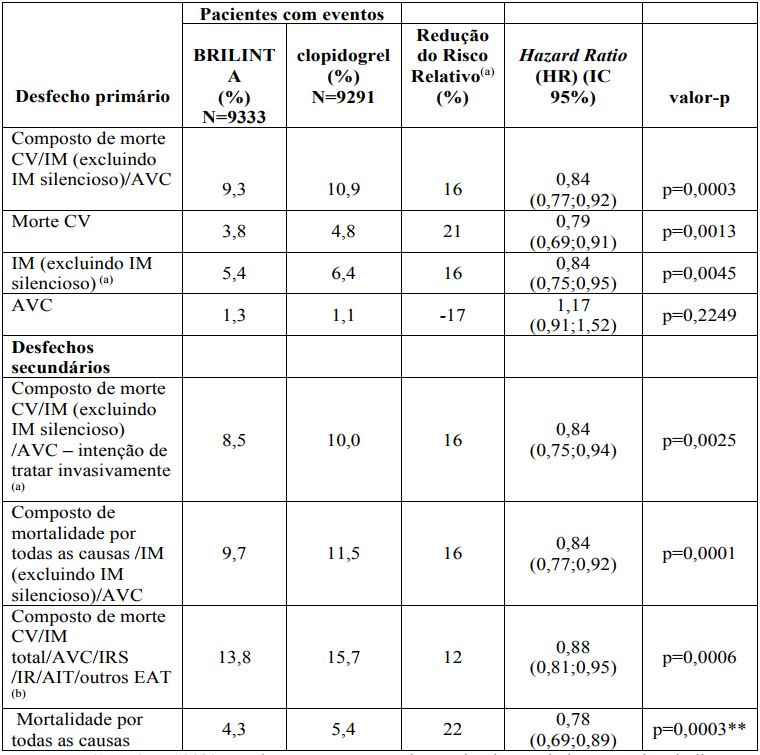
(a) RRR= (1-HR) x 100%. Valores com uma redução do risco relativo negativo indicam um aumento do risco relativo.
(b) IRS = isquemia recorrente severa / IR = isquemia recorrente / AIT= acidente isquêmico transitório / EAT= evento arterial trombótico.
** valor-p nominal.
Ticagrelor (substância ativa) é superior ao clopidogrel na prevenção de eventos trombóticos (RRR 16%; RRA 1,9%; NNT =54) no desfecho composto de eficácia (morte CV, IM e AVC) em 12 meses. A diferença nos tratamentos foi determinada pela morte cardiovascular e infarto do miocárdio sem diferença nos acidentes vasculares cerebrais.
Ticagrelor (substância ativa) demonstrou uma redução do risco relativo estatisticamente significativo de 16% (RRA 1,1%) para IM e uma redução do risco relativo de 21% (RRA 1,1%) para morte CV. Tratar 91 pacientes com Ticagrelor (substância ativa) ao invés de clopidogrel prevenirá 1 morte CV.
Ticagrelor (substância ativa) demonstrou superioridade em relação ao clopidogrel na prevenção do desfecho composto (morte CV, IM ou AVC). Os resultados foram precoces (redução de risco absoluto [RRA] de 0,6% e Redução do Risco Relativo [RRR] de 12% em 30 dias), com efeitos observados no tratamento mantidos durante o período de 12 meses, resultando em uma RRA de 1,9% ao ano com RRR de 16%. Isto sugere que o tratamento é apropriado por pelo menos 12 meses.
No estudo PLATO um grande número de comparações de subgrupos foram conduzidas do desfecho de eficácia primário para avaliar a robustez e consistência do benefício global. O efeito do tratamento de Ticagrelor (substância ativa) em comparação ao clopidogrel parece consistente entre os múltiplos subgrupos de pacientes pelas características demográficas, incluindo peso, sexo, antecedentes clínicos, terapia concomitante e pelo diagnóstico final do evento (IAMSST, IAMCST e AI).
Uma fraca, mas significativa interação do tratamento foi observada por região em que o HR para o desfecho primário favorece Ticagrelor (substância ativa) no resto do mundo, mas favorece o clopidogrel na América do Norte, que representou aproximadamente 10% do total da população estudada (valor-p da interação = 0,045).
Essa aparente interação de tratamento por região observada no PLATO pode plausivelmente ser atribuída ao acaso, pelo menos em parte. Análises adicionais sugerem que a eficácia de Ticagrelor (substância ativa) em relação ao clopidogrel está associada à dose de ácido acetilsalicílico durante a terapia de manutenção. Os dados mostram uma maior eficácia de Ticagrelor (substância ativa) em relação ao clopidogrel, quando utilizados em associação com uma dose baixa de ácido acetilsalicílico (75-150 mg).
A eficácia relativa de Ticagrelor (substância ativa) versus clopidogrel, quando utilizado com altas doses de ácido acetilsalicílico (> 300 mg) é menos evidente. Baseado nessas observações da relação entre a dose de manutenção do ácido acetilsalicílico e a eficácia relativa de Ticagrelor (substância ativa) em comparação ao clopidogrel, é recomendado que Ticagrelor (substância ativa) seja utilizado com uma dose baixa de ácido acetilsalicílico de 75-150 mg.
Os benefícios associados com Ticagrelor (substância ativa) também foram independentes do uso de outras terapias cardiovasculares indicadas na fase aguda e de longo-prazo, incluindo heparina, heparina de baixo peso molecular (HBPM), inibidores GpIIb/IIIa por via intravenosa, medicamentos hipolipemiantes, betabloqueadores, inibidores da enzima conversora da angiotensina (ECA), antagonistas dos receptores da angiotensina II e inibidores da bomba de prótons.
Ticagrelor (substância ativa) demonstrou uma redução do risco relativo (RRR) estatisticamente significativa no desfecho composto de morte cardiovascular (CV), infarto do miocárdio (IM) e acidente vascular cerebral (AVC) em pacientes com SCA com intenção de tratamento invasivo (RRR 16%; RRA 1,7%; p = 0,0025). Em uma análise exploratória, Ticagrelor (substância ativa) demonstrou uma redução do risco relativo do desfecho composto primário em pacientes com SCA com intenção de tratamento clínico (RRR 15%; RRA 2,3%; p nominal = 0,0444).
Consistente com o desfecho primário do estudo, o efeito nesses dois grupos foi determinado pela morte CV e IM, sem efeito em AVC. Em pacientes recebendo stents houve numericamente menos trombose definitiva de stent entre pacientes tratados com Ticagrelor (substância ativa) comparado com o clopidogrel (73 versus 107; RRR 32%; RRA 0,6%; p nominal = 0,0123).
Ticagrelor (substância ativa) demonstrou uma RRR estatisticamente significativa de 16% (RRA 2,1%) para o composto de mortalidade por todas as causas, IM e AVC comparado com o clopidogrel.
O desfecho secundário final (mortalidade por todas as causas) foi avaliado. Ticagrelor (substância ativa) demonstrou uma RRR de 22% de mortalidade por todas as causas comparado com o clopidogrel com um nível de significância de p = 0,0003 e uma RRA de 1,4%.
Características farmacológicas
Propriedades Farmacodinâmicas
Efeitos farmacodinâmicos
Propriedades Farmacocinéticas
Populações especiais
Dados de segurança pré-clínica
Dados pré-clínicos para o Ticagrelor (substância ativa) e o principal metabólito não demonstraram risco inaceitável para efeitos adversos para humanos baseado em estudos convencionais de farmacologia de segurança, toxicidade de dose única e repetida e potencial genotóxico.
Reações adversas não observadas em estudos clínicos, mas observadas em animais com níveis de exposição similar ou superior aos níveis de exposição clínica e com possível relevância para o uso clínico foram: GI (gastrointestinais) e irritação gastrointestinal.
Não foram observados tumores relacionados ao composto em um estudo de 2 anos com camundongos em doses orais até 250 mg/kg/dia (> 18 vezes a exposição terapêutica humana). Não houve aumento nos tumores em ratos machos em doses orais até 120 mg/kg/dia (> 15 vezes a exposição terapêutica humana). Houve um aumento de adenocarcinomas uterinos e adenomas hepatocelulares mais adenocarcinomas e uma redução nos adenomas hipofisários e fibroadenomas mamários em ratas expostas somente a altas doses (> 25 vezes a exposição terapêutica humana).
Não foi observada alteração na incidência de tumores em doses de 60 mg/kg/dia (diferença > 8 vezes para a dose terapêutica humana.). Os tumores uterinos observados apenas em ratos foram achados ser o resultado de um efeito endócrino não-genotóxico do desequilíbrio hormonal presente em ratos que receberam altas doses de Ticagrelor (substância ativa).
Os tumores benignos do fígado são considerados secundários a resposta pelo fígado para a carga metabólica localizada no fígado a partir de doses elevadas de Ticagrelor (substância ativa).
O Ticagrelor (substância ativa) foi testado em uma faixa de testes in vitro e in vivo e não foi mostrado ser genotóxico.
O Ticagrelor (substância ativa) não demonstrou ter efeito na fertilidade de ratas fêmeas em doses orais até 200 mg/kg por dia (aproximadamente 20 vezes a exposição terapêutica humana) e não teve efeito sobre a fertilidade de ratos machos em doses até 180 mg/kg/dia (15,7 vezes a exposição terapêutica humana).
O Ticagrelor (substância ativa) não teve efeito no desenvolvimento fetal em doses orais até 100 mg/kg por dia em ratos (5,1 vezes a exposição terapêutica humana) e até 42 mg/kg/dia em coelhos (equivalente à exposição terapêutica humana). O Ticagrelor (substância ativa) não teve efeitos no parto ou no desenvolvimento pós-natal em ratos com doses até 60 mg/kg/dia (4,6 vezes a exposição terapêutica humana).
Cuidados de Armazenamento
Você deve conservar Brilinta em temperatura ambiente (15ºC a 30ºC).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Para sua segurança, mantenha o medicamento na embalagem original.
Os comprimidos de Brilinta são apresentados da seguinte maneira:
Comprimidos revestidos, redondos, biconvexos e de cor amarela, com a impressão 90 T de um lado e liso do outro.
Antes de usar, observe o aspecto do medicamento. Caso você observe alguma mudança no aspecto do medicamento que ainda esteja no prazo de validade, consulte o médico ou o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Venda sob prescrição médica.
MS - 1.1618.0238
Farm. Resp.:
Dra. Gisele H. V. C. Teixeira - CRF-SP nº 19.825
Fabricado por:
AstraZeneca AB (Gärtunavägen) – Södertälje – Suécia
Importado e embalado por:
AstraZeneca do Brasil Ltda.
Rod. Raposo Tavares, km 26,9 - Cotia - SP - CEP 06707-000
CNPJ 60.318.797/0001-00
Indústria Brasileira
informações complementares
| Fabricante |
| ASTRAZENECA |
| Princípio ativo |
| Ticagrelor |
| Categoria do medicamento |
| Medicamentos de A-Z |
BRILINTA - 90MG 60 COMPRIMIDOS É UM MEDICAMENTO, NÃO USE SEM PRESCRIÇÃO MÉDICA E ORIENTAÇÃO DO FARMACÊUTICO. AO PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
