- Medicamentos
- Medicamentos Especiais
- Gazyva - 1000 Mg Solução Diluente Infs Intravenosa Frasco-Ampola 40 Ml
Menor preço para Gazyva - 1000 Mg Solução Diluente Infs Intravenosa Frasco-Ampola 40 Ml, você encontra no CliqueFarma
Gazyva - 1000 Mg Solução Diluente Infs Intravenosa Frasco-Ampola 40 Ml

Menor Preço
R$ 26.300,00
- CATEGORIA: Medicamentos Especiais
- PRINCÍPIO ATIVO: Obinutuzumabe
- FABRICANTE: ROCHE
PARA QUE SERVE?
Para que serve Leucemia Linfocítica Crônica (LLC): Gazyva está indicado, juntamente com outro medicamento chamado clorambucil, para tratar pacientes adultos portadores de leucemia linfocítica crônica, que não tenham recebido outro medicamento anteriormente e que apresentem comorbidades (ocorrência simultânea de dois ou mais problemas de saúde em um mesmo indivíduo), tornando-os não elegíveis ao tratamento baseado na dose plena do medicamento fludarabina.
R
Referência
12
ofertasMelhores preços a partir de R$ 26.300,00 até R$ 43.888,00
Menor preço
Frete Grátis para SP e MG em Compras Acima de R$ 149,90.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Frete Grátis para SP e MG em Compras Acima de R$ 149,90.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Farmácia de medicamentos oncológicos. Parcelamos em até 6 x sem juros.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Para que serve
Leucemia Linfocítica Crônica (LLC):
Gazyva está indicado, juntamente com outro medicamento chamado clorambucil, para tratar pacientes adultos portadores de leucemia linfocítica crônica, que não tenham recebido outro medicamento anteriormente e que apresentem comorbidades (ocorrência simultânea de dois ou mais problemas de saúde em um mesmo indivíduo), tornando-os não elegíveis ao tratamento baseado na dose plena do medicamento fludarabina.
Linfoma Folicular:
Gazyva está indicado, juntamente com outro medicamento chamado bendamustina e depois tomado sozinho, em terapia de manutenção, para tratamento de portadores de linfoma folicular que não tenham respondido ou que tenham recaído durante ou depois do tratamento com rituximabe ou com um esquema de tratamento contendo rituximabe.
Como Gazyva funciona?
Gazyva é um anticorpo do tipo IgG1 fabricado por glicoengenharia. Ele atinge um antígeno que fica na superfície de algumas células brancas do sangue chamadas de linfócitos que podem ser não malignas ou malignas, mas não atinge as células-tronco do sistema formador de células do sangue nem outras células de tecidos normais. Por serem produzidos por glicoengenharia, esses anticorpos apresentam uma atividade mais potente.
Em estudos não clínicos, isto é, que não foram realizados em seres humanos, Gazyva provocou a morte direta das células e colaborou na toxicidade celular e fagocitose (englobamento de células pelo sistema de defesa) que dependem de anticorpos recrutando células imunoefetoras (células com atividade imunológica). Também atuou na toxicidade que depende de complemento. Isso se traduz em uma redução maior das células do tipo B e maior eficácia antitumoral em animais.
Em um estudo clínico realizado com pacientes tratados com Gazyva, houve redução de células B (número de células B CD19+ < 0,07 x 109/L) no final do período de tratamento e o número continuou baixo durante o período de recuperação dos primeiros 6 meses. A recuperação de células B foi observada entre 12 a 18 meses de acompanhamento em 35% (14 de 40) pacientes sem doença progressiva e 13% (5 de 40) com doença progressiva.
Contraindicação
Você não deve utilizar este medicamento se souber que tem alergia ao obinutuzumabe ou a qualquer um dos outros componentes de Gazyva.
Como usar
Gazyva deve ser administrado por infusão intravenosa por meio de um acesso venoso exclusivo, em um ambiente onde meios de reanimação estejam imediatamente disponíveis e sob a supervisão rigorosa de um médico experiente. Infusões de Gazyva não devem ser administradas em injeção direta ou em bolus. Deve-se utilizar solução isotônica de cloreto de sódio 0,9% (soro fisiológico) como veículo de infusão.
Pré-medicação, consistindo de analgésico/antipirético, anti-histamínico e glicocorticoide, deverá ser sempre administrada antes de cada infusão de Gazyva.
O profissional da saúde saberá como preparar o medicamento.
Leucemia linfocítica crônica - Dose de Gazyva em combinação com clorambucil
A dose recomendada de Gazyva é de 1000 mg administrados nos Dias 1-2 (100 + 900 mg), 8 e 15 do primeiro ciclo de tratamento de 28 dias, seguido por 1000 mg administrados apenas no Dia 1 para cada ciclo de tratamento subsequente (Ciclos 2 a 6).
Linfoma Folicular
A dose recomendada de Gazyva é de 1000 mg administrados no Dia 1, Dia 8 e dia 15 do primeiro ciclo de tratamento de 28 dias, seguidos por 1000 mg administrados apenas no Dia 1 de cada ciclo de tratamento de 28 dias subsequente (Ciclos 2 a 6).
Pacientes que responderem ao tratamento (resposta completa ou resposta parcial) ou apresentem doença estável devem continuar a receber Gazyva 1000 mg isoladamente como terapia de manutenção uma vez a cada 2 meses até a progressão da doença ou por até dois anos.
Duração do Tratamento
Seis ciclos de tratamento, com duração de 28 dias cada.
Modificações de dose durante o tratamento
Não são recomendadas reduções de dose de Gazyva.
Ajustes de dose para populações especiais
Crianças
A segurança e a eficácia de Gazyva em crianças abaixo dos 18 anos de idade não foram estabelecidas.
Idosos
Não é necessário ajuste de dose para pacientes idosos.
Insuficiência Renal
Não é necessário ajuste de dose em pacientes com insuficiência renal leve ou moderada. Gazyva não foi estudado em pacientes com CrCl < 30 mL/min.
Insuficiência Hepática
A segurança e a eficácia de Gazyva em pacientes com insuficiência hepática não foram estabelecidas.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar Gazyva?
Caso uma dose programada de Gazyva seja perdida, a mesma deve ser administrada assim que possível. Não omita e nem espere até a próxima dose planejada.
Seu médico saberá quando deverá ser aplicada a próxima dose de Gazyva.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
A substituição de Gazyva por qualquer outro medicamento biológico exige o consentimento do médico prescritor.
Gerais
Infusões de Gazyva não devem ser administradas em injeção direta ou em bolus.
Reações relacionadas a infusão (RRI)
As reações que foram observadas com maior frequência em pacientes recebendo Gazyva são relacionadas à infusão, principalmente durante a infusão dos primeiros 1000 mg.
Em pacientes com leucemia linfocítica crônica que receberam as medidas para a prevenção de reações infusionais, as quais devem ser seguidas, observou-se uma menor ocorrência de reações infusionais de todos os graus. Notou-se, ainda, redução substancial da incidência e da intensidade dos sintomas relacionadas às infusões após os primeiros 1000 mg, sendo que a maioria dos pacientes não apresentou nenhuma reação durante as aplicações subsequentes de Gazyva.
Na maioria dos pacientes com leucemia linfocítica crônica ou linfoma folicular, as reações foram leves a moderadas e puderam ser controladas diminuindo a velocidade da primeira infusão ou suspendendo temporariamente, mas também foram descritas reações mais intensas, com necessidade de tratamento. Essas reações podem ser muito semelhantes às reações alérgicas tipo anafiláticas. Pacientes com carga tumoral elevada [isto é, número elevado de linfócitos no sangue na LLC (> 25 x 109/L)] podem ter um risco mais elevado de reações graves.
Se você apresentar uma reação, a infusão deve ser controlada de acordo com o grau da reação. O seu médico saberá como tratar as reações à infusão e também vai determinar se você poderá ou não continuar recebendo a medicação.
Caso você apresente sintomas respiratórios agudos e/ou reações infusionais graves Grau 4, ou ainda uma segunda ocorrência de reação infusional de Grau 3, o tratamento deve ser interrompido.
Se você apresentar problemas cardíacos ou pulmonares antes do tratamento, haverá necessidade de um acompanhamento mais rigoroso, durante e depois da infusão. Pode ocorrer hipotensão (queda da pressão arterial) durante a infusão. Por isso, às vezes é preciso suspender os tratamentos anti-hipertensivos para reduzir a pressão arterial durante 12 horas antes e durante toda a infusão de Gazyva. Esta suspensão deve ser mantida durante a primeira hora depois da infusão. Pacientes com risco de crise hipertensiva deverão ser avaliados quanto aos benefícios e riscos de suspensão da medicação anti-hipertensiva.
Reações de hipersensibilidade
As reações de hipersensibilidade (tipo alérgicas) com início imediato (por exemplo: anafilaxia) e início tardio (por exemplo: doença do soro) foram reportados em pacientes tratados com Gazyva. Se houver suspeita de uma reação de hipersensibilidade durante ou após a infusão (geralmente depois de uma exposição prévia e, muito raramente, na primeira infusão), a infusão deverá ser interrompida e o tratamento, definitivamente descontinuado. Pacientes com hipersensibilidade a Gazyva não devem ser tratados. A hipersensibilidade pode ser clinicamente difícil de distinguir de uma reação relacionada à infusão.
Síndrome de Lise Tumoral
Esta síndrome foi relatada com Gazyva. Pacientes considerados de risco (p.ex., aqueles com elevada carga tumoral e/ou grande número de linfócitos no sangue e/ou insuficiência renal) devem receber medidas de prevenção. Essas medidas consistem de hidratação adequada e administração de medicamentos uricostáticos ou uma alternativa adequada, como a urato oxidase, antes da infusão de Gazyva. Todos os pacientes considerados como de risco devem ser cuidadosamente monitorados durante os dias iniciais de tratamento, com especial foco para a função renal, valores de potássio e ácido úrico. Qualquer orientação adicional de acordo com a prática clínica deve ser seguida. Seu médico saberá como tratar essa síndrome caso você apresente os sintomas característicos.
Neutropenia
Neutropenia (número baixo de um dos tipos de células brancas do sangue) grave e potencialmente fatal, incluindo neutropenia febril, foi relatada com Gazyva. Seu médico saberá como tratar esse problema, caso ele ocorra. É preciso estar atento ao aparecimento de infecções, porque as defesas do organismo ficam prejudicadas quando há neutropenia. Neutropenia tardia (28 dias após o término do tratamento) ou prolongada também podem ocorrer.
Trombocitopenia
Pode ocorrer redução grave e potencialmente fatal do número de plaquetas (ou trombócitos, elementos do sangue relacionados à coagulação) dentro de 24 horas após a infusão durante o tratamento com Gazyva. Seu médico saberá como tratar a trombocitopenia, caso venha a ocorrer. É importante que você informe ao seu médico todos os medicamentos que estiver tomando, porque alguns podem aumentar esse efeito de reduzir as plaquetas, principalmente no primeiro ciclo. Eventos hemorrágicos fatais também foram observados no Ciclo 1 em pacientes que receberam Gazyva. Uma relação clara entre trombocitopenia e eventos hemorrágicos não foi estabelecida.
Piora de Problemas Cardíacos Preexistentes
Em pacientes portadores de problemas cardíacos prévios, ocorreram arritmias, dor no peito, problemas das artérias coronárias, infarto do miocárdio e insuficiência cardíaca durante o tratamento com Gazyva. Esses eventos podem ocorrer como parte da reação à infusão e podem ser fatais. Portanto, se você tiver uma doença cardíaca conhecida, precisará de acompanhamento especial e a hidratação deve ser feita com cautela, para retenção de líquidos.
Infecções
Gazyva não deve ser administrado na presença de infecção ativa e deve-se ter cuidado com pacientes com história de infecções repetidas ou crônicas. Infecções graves, bacterianas, fúngicas e virais, podem ocorrer durante e depois do tratamento com Gazyva. Infecções fatais foram observadas.
Uma alta incidência de infecções foi observada em todas as fases dos estudos clínicos em linfoma folicular, incluindo a fase de acompanhamento, com maior incidência vista na manutenção. Durante a fase de acompanhamento, infeções grau 3-5 foram mais observadas em pacientes que receberam Gazyva + bendamustina na fase de indução.
Reativação de Hepatite B
A reativação do vírus da hepatite B (HBV), em alguns casos, resultando em hepatite fulminante, insuficiência hepática e óbito, pode ocorrer em pacientes tratados com medicamentos biológicos anti-CD20, incluindo Gazyva. Deve ser sempre exame prévio para identificar infecção pelo vírus da hepatite B em todos os pacientes antes de iniciar o tratamento com Gazyva. Pacientes com doença ativa não devem receber Gazyva. Se a sua sorologia for positiva para hepatite B, será encaminhado a um especialista em doenças do fígado antes do início do tratamento. Seu médico saberá como orientar seu tratamento.
Leucoencefalopatia Multifocal Progressiva (LEMP)
Foram relatados casos desta doença durante tratamento com Gazyva. É uma doença neurológica. Os sintomas são manifestações neurológicas, mas são inespecíficos e dependem da área do cérebro que foi afetada. Podem aparecer fraqueza muscular, paralisia, distúrbio da sensibilidade, sintomas de desequilíbrio e alteração da visão. Também podem ocorrer incapacidade para falar e desorientação espacial. Se houver suspeita dessa doença, o paciente precisa ser encaminhado ao neurologista para investigação com exames (coleta de líquido cefalorraquidiano, exame de ressonância magnética etc.) e a terapia com Gazyva deverá ser suspensa. Caso o diagnóstico seja confirmado, a terapia será definitivamente interrompida.
Imunização
A segurança da imunização com vacinas virais vivas ou atenuadas não foi estudada e não se recomenda o uso de vacinas com vírus vivo (como a tríplice viral ou a de febre amarela) durante o tratamento com Gazyva e até a recuperação dos linfócitos B.
Exposição no útero a Gazyva e vacinação de crianças com vacinas de vírus vivo
Por causa da potencial diminuição das células B em crianças de mães que receberam Gazyva durante a gravidez, a segurança e o tempo de vacinação com vírus vivo deve ser discutido com o pediatra. A prorrogação da vacinação com vacinas de vírus vivo deve ser considerada para crianças nascidas de mães que receberam Gazyva durante a gravidez até o nível de células B da criança estar dentro da faixa de normalidade.
Capacidade para Dirigir e Operar Máquinas
Não foram feitos estudos sobre os efeitos de Gazyva sobre a capacidade de dirigir ou operar máquinas. Se você apresentar sintomas relacionados à infusão, deverá ser orientado a não dirigir nem operar máquinas até que os sintomas desapareçam.
Uso em Crianças
A segurança e a eficácia de Gazyva não estão estabelecidas em crianças abaixo de 18 anos de idade.
Uso em Idosos
Leucemia Linfocítica Crônica
Em um dos estudos, 46% (156 de 336) dos pacientes com leucemia linfocítica crônica tratados com Gazyva mais clorambucil, tinham 75 anos de idade ou mais. Esses pacientes apresentaram mais eventos adversos e eventos adversos graves (até levando ao óbito) do que pacientes com menos de 75 anos. Não foram notadas diferenças na eficácia.
Linfoma Não-Hodgkin
Nos estudos em Linfoma Não-Hodgkin, pacientes com 65 anos de idade ou mais apresentaram mais eventos adversos graves e eventos adversos que levaram a descontinuação ou óbito que pacientes < 65. Não foi observada nenhuma diferença significativa clinicamente na eficácia.
Insuficiência Renal
Leucemia Linfocítica Crônica
Em um dos estudos, 27% (90 de 336) dos pacientes com leucemia linfocítica crônica tratados com Gazyva mais clorambucil, apresentavam grau moderado de insuficiência renal (ou seja, de mau funcionamento dos rins).
Esses pacientes apresentaram mais eventos adversos graves e levando ao óbito do que pacientes sem insuficiência renal, mas não houve diferença na eficácia.
Linfoma Não-Hodgkin
Nos estudos em pacientes portadores de linfoma Não-Hodgkin, 7,7% (GAO4753g:15 de 194) dos tratados com Gazyva mais bendamustina apresentavam insuficiência renal moderada. Eles apresentaram mais eventos adversos graves, eventos levando a óbito e a descontinuação do tratamento do que os pacientes sem insuficiência renal. Não foram testados pacientes com insuficiência renal muito grave.
Insuficiência Hepática
A segurança e a eficácia de Gazyva em pacientes com insuficiência hepática não foram estabelecidas.
Gravidez
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Gazyva deve ser evitado durante a gravidez, a menos que o potencial benefício para a mãe supere o risco para o feto.
Se você é mulher com possibilidade de gravidez, deve usar um contraceptivo eficaz enquanto estiver fazendo tratamento com Gazyva e durante 18 meses após o término do tratamento. A prorrogação da vacinação com vacinas de vírus vivo deve ser considerada para crianças nascidas de mães que receberam Gazyva durante a gravidez até que os níveis de linfócitos B da criança estejam dentro da faixa de normalidade.
Não foram feitos estudos em gestantes. Um estudo em macacos não mostrou evidências de toxicidade embrionária ou fetal ou efeitos teratogênicos (de malformação fetal), mas resultou em falta completa de linfócitos B (tipo de célula branca do sangue, ligada à defesa contra infecções) nos filhotes.
O número dessas células voltou ao normal e as defesas do organismo foram restauradas dentro de 6 meses após o parto. Não obstante, as concentrações séricas de Gazyva nos filhotes foram similares àqueles nas mães no dia 28º dia pós-parto, enquanto as concentrações encontradas no leite no mesmo dia foram muito baixas, sugerindo que Gazyva atravesse a placenta.
Lactação
Como o tipo de anticorpo IgG (que é o mesmo do obinutuzumabe) é secretado no leite materno e não se conhece a possibilidade de absorção pela criança, se você estiver amamentando, será orientada a descontinuar o aleitamento durante a terapia com Gazyva e até 18 meses após a última dose. Estudos em animais de laboratório mostraram excreção de Gazyva no leite materno.
Interações com Outros Produtos Medicinais e Outras Formas de Interação
Não foram realizados estudos formais de interação medicamentosa. Foram feitos estudos limitados com bendamustina, CHOP (associação de medicamentos quimioterápicos), FC (fludarabina e ciclofosfamida) e clorambucil.
A administração de Gazyva não teve efeito sobre a ação desses medicamentos e estes também não tiveram efeito sobre a ação do Gazyva. O risco de interações com produtos medicinais usados ao mesmo tempo não pode ser afastado.
Até o momento, não há informações de que obinutuzumabe possa causar doping. Em caso de dúvida, consulte o seu médico.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
?Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Leucemia Linfocítica Crônica
As reações que este medicamento pode provocar foram identificadas durante o tratamento e acompanhamento em estudos clínicos, em que Gazyva foi administrado juntamente com clorambucil e a comparação foi feita com o uso de clorambucil sem Gazyva (Estágio 1) ou rituximabe mais clorambucil (Estágio 2). Oitenta e um por cento (81%) dos pacientes tratados com Gazyva com clorambucil receberam os 6 ciclos completos de tratamento, em comparação com 89% dos pacientes no braço do estudo que receberam rituximabe mais clorambucil e 67% dos pacientes no braço do estudo que receberam apenas clorambucil.
As Tabelas 1 e 2 resumem as reações adversas que ocorreram com maior frequência (diferença ? 2%) em pacientes que receberam Gazyva com clorambucil em comparação com clorambucil apenas ou rituximabe mais clorambucil, respectivamente.
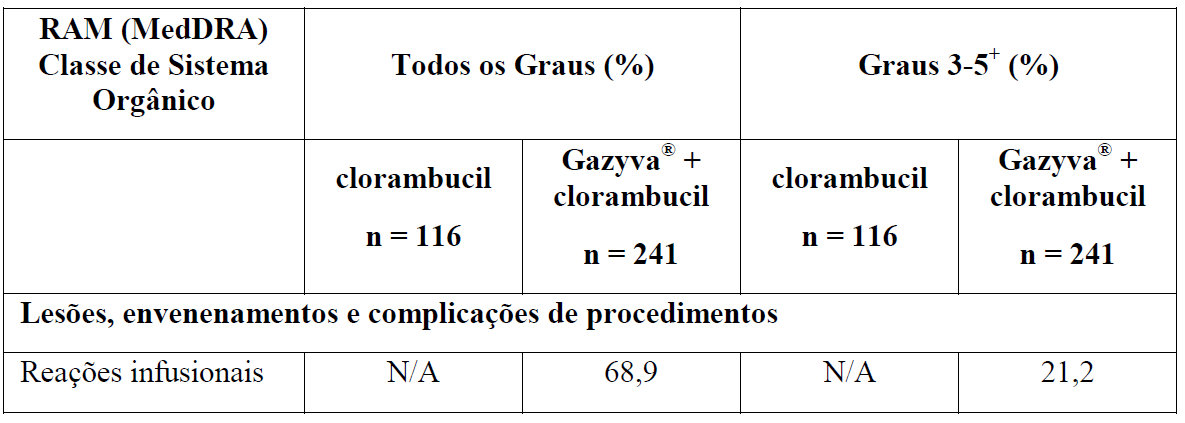
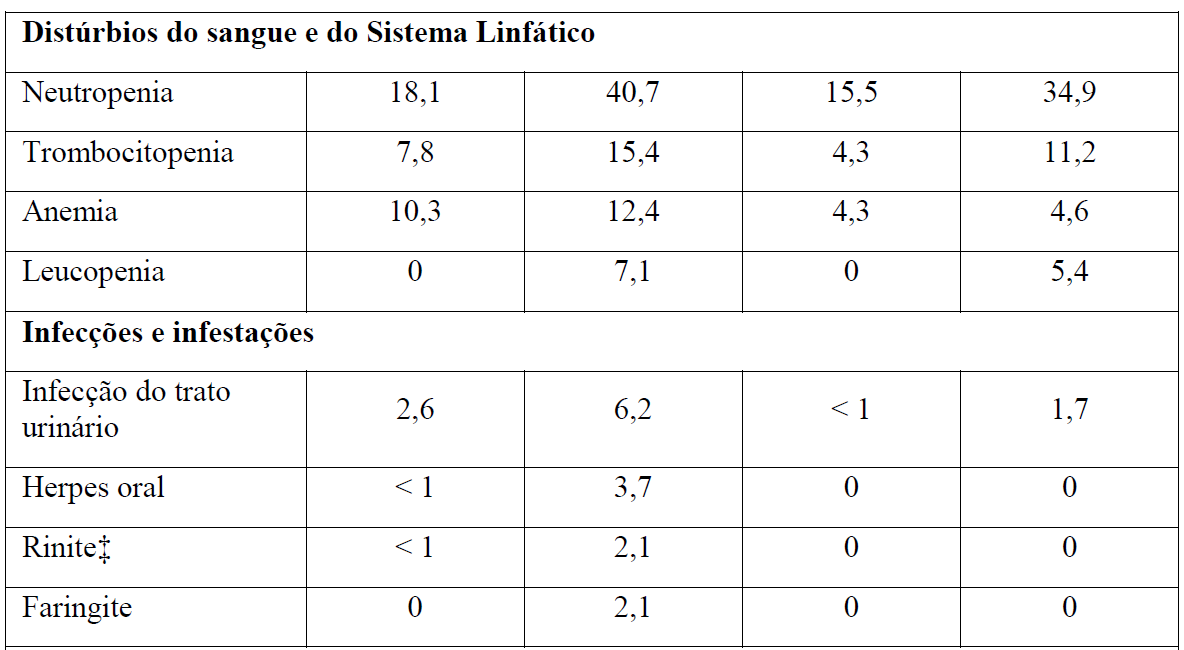
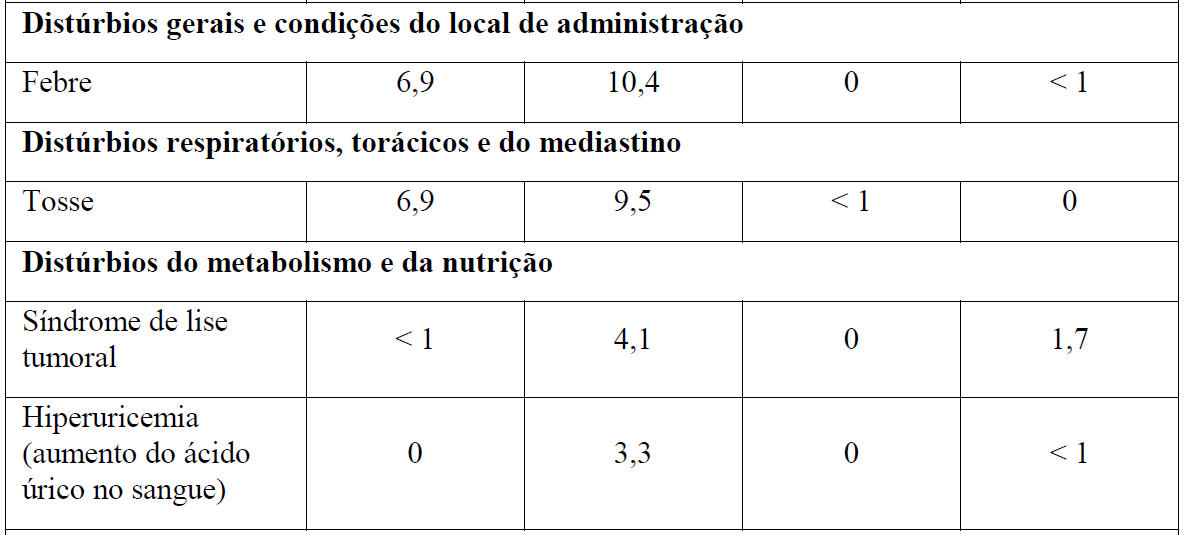
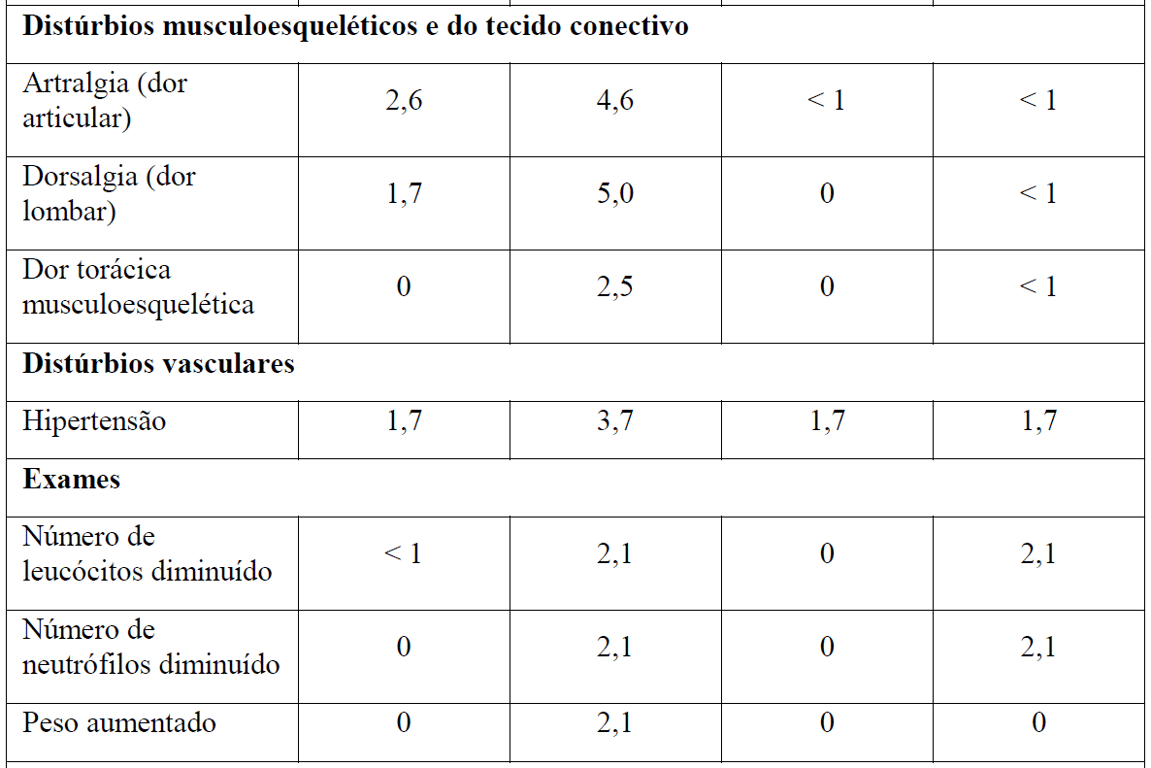

*Em todos os graus ou Graus 3-5.
+ Nenhuma reação adversa Grau 5 foi observada com uma diferença ? 2% entre os braços de tratamento.
‡ Com a atualização dos dados do Estágio 1 e Estágio 2, esse evento não foi mais reportado com uma diferença de ? 2% entre os braços de tratamento.
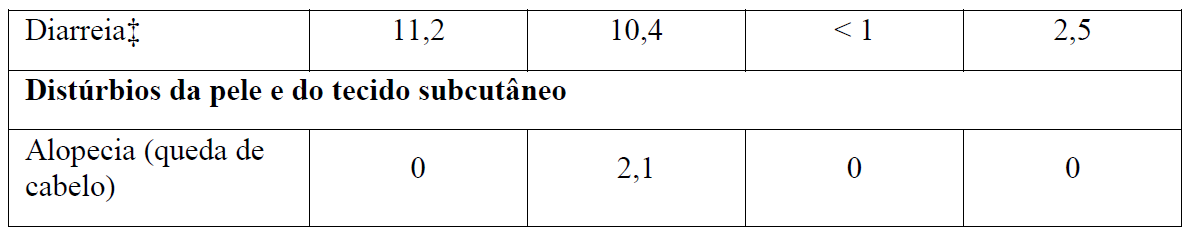
Tabela 2 Reações adversas reportadas com maior incidência (diferença ? 2%) em pacientes recebendo Gazyva mais clorambucil em comparação com rituximabe mais clorambucil (Estágio 2)
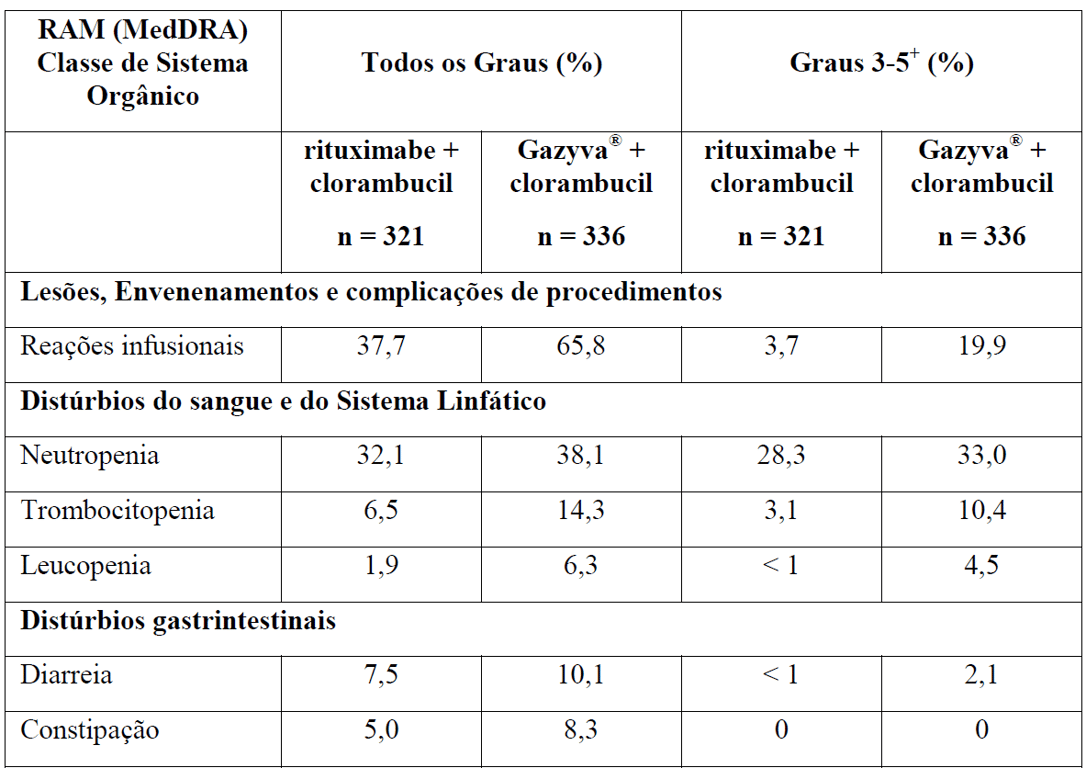
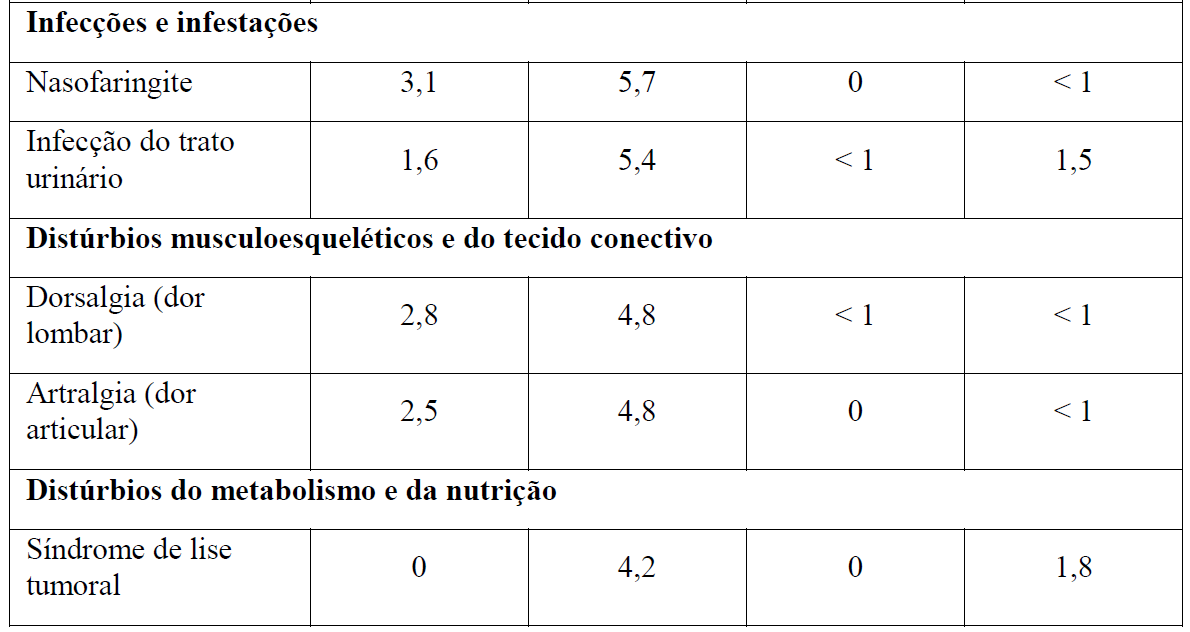
* Em todos os graus ou Graus 3-5.
+ Nenhuma reação adversa Grau 5 foi observada com uma diferença ? 2% entre os braços de tratamento.
Linfoma Não-Hodgkin
No subgrupo de pacientes com linfoma folicular, o perfil das reações adversas foi compatível com a população total de pacientes com linfoma Não-Hodgkin (LNH).
As reações adversas à medicamentos (RAMs) descritas nesta seção (baseadas em uma população de segurança de 392 pacientes com LNH indolente, dos quais 81% tinham LF) foram identificadas durante a indução, a manutenção e o acompanhamento do estudo clínico, em que Gazyva foi administrado em combinação com bendamustina (G+B) durante a indução e em monoterapia na manutenção e comparadas com bendamustina durante a indução apenas (B).
Em pacientes tratados com G+B, 79,4% receberam os 6 ciclos de tratamento com Gazyva e 75,6% receberam os 6 ciclos de B em comparação com 66,7% dos pacientes no braço B.
A Tabela 3 resume as RAMs que ocorreram com maior incidência (diferença > 2%) em pacientes que receberam G+B durante a indução seguidos por manutenção com Gazyva em comparação com B durante a indução apenas.
Tabela 3 Reações Adversas reportadas com maior incidência (diferença > 2%) em pacientes recebendo Gazyva mais bendamustina (indução) seguidos por manutenção com Gazyva em relação a bendamustina (indução) apenas
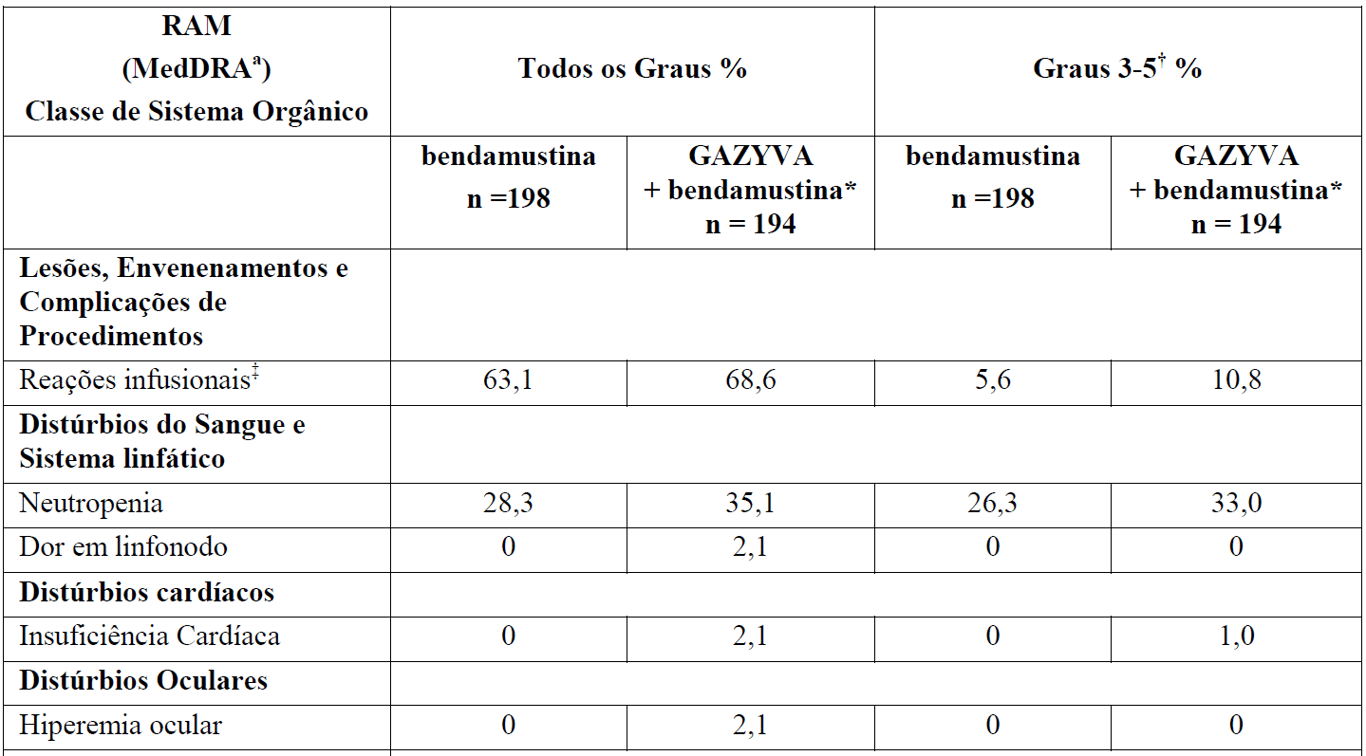
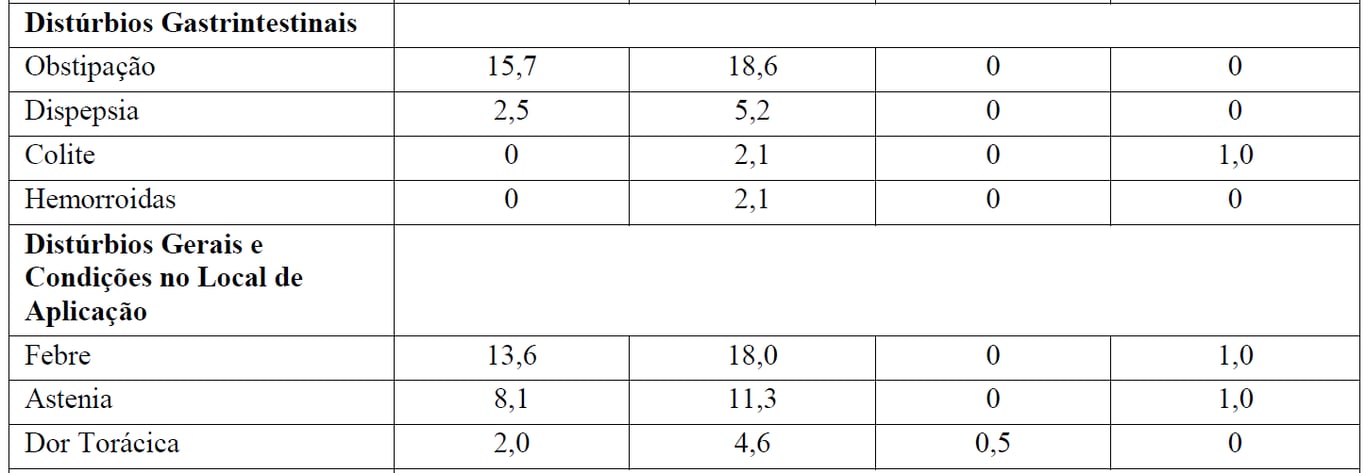
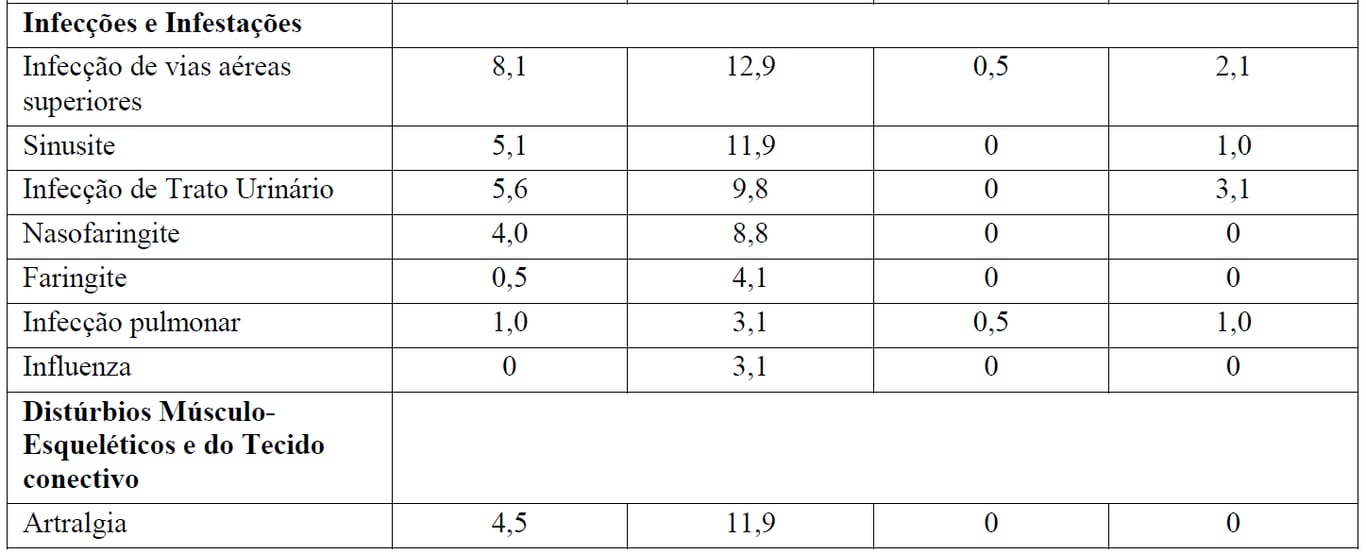
*Seguido por Gazyva manutenção.
aReações adversas codificadas pelo MedDRA conforme relato dos investigadores (excluindo as reações infusionais).
† Não foi observada nenhuma reação adversa Grau 5 com uma diferença > 2% entre os braços de tratamento.
‡ definido como qualquer evento adverso relacionado que tenha ocorrido durante ou no prazo de 24 horas da infusão.
Pacientes no braço B receberam 6 meses de tratamento de indução apenas, enquanto que depois do período de indução os pacientes no braço G+B continuaram com tratamento de manutenção com Gazyva. Durante o período de manutenção com Gazyva, as reações adversas mais comuns foram tosse (14,7%), infecções de vias aéreas superiores (11,9%), neutropenia (10,5%), sinusite (9,8%), diarreia (8,4%), reações infusionais (8,4%), náuseas (7,7%), fadiga (7,7%), bronquite (7,0%), artralgia (7,0%), nasofaringite (6,3%), infecções de trato urinário (6,3%) e febre (5,6%).
As reações adversas graus 3-5 mais comuns foram neutropenia (9,8%) e anemia, neutropenia febril, trombocitopenia, sepse, infecção de vias aéreas superiores e infecção de trato urinário (todas com 1,4%).
Informações adicionais sobre algumas reações adversas ao obinutuzumabe
Reações relacionadas à infusão:
Os sintomas mais frequentemente reportados (?5%) associados com uma reação infusional foram náuseas, fadiga, calafrios, hipotensão, febre, vômitos, dispneia, rubor, hipertensão, cefaleia, taquicardia, tontura e diarreia. Sintomas respiratórios e cardíacos como broncoespasmo, irritação de laringe e garganta, sibilos, edema de laringe e fibrilação atrial também foram reportados.
Leucemia Linfocítica Crônica
A incidência dessas reações foi de 65% com a infusão dos primeiros 1000 mg de Gazyva (20% dos pacientes com reação infusional de Graus 3-4. No geral, 7% dos pacientes apresentaram uma reação infusional que levou à descontinuação do tratamento com Gazyva. A incidência de reações infusionais com infusões subsequentes foi de 3% com a segunda dose de 1000 mg e 1%, por conseguinte. Nenhuma reação infusional Graus 3-5 foi reportada além dos primeiros 1000 mg infusionais do Ciclo 1.
Em pacientes que receberam as medidas para a prevenção de reações infusionais, observou-se uma redução da incidência de reações infusionais de todos os graus. As taxas de reações infusionais Graus 3-4 (as quais foram baseadas em um número relativamente pequeno de pacientes) foram similares antes e depois que as medidas para a redução de reações foram implementadas.
Linfoma Não-Hodgkin
No Ciclo 1, a incidência total de reações infusionais foi maior em pacientes recebendo G+B (55%) em comparação com pacientes recebendo apenas B (42%) (com reações infusionais Graus 3-5 reportadas em 9% e 2%, respectivamente e nenhum evento fatal). Em pacientes recebendo G+B, a incidência de reações infusionais foi maior no Dia 1 (38%) e diminuiu gradualmente nos Dias 2, 8 e 15 (25%, 7% e 4%, respectivamente).
Durante o ciclo 2, a incidência de reações infusionais foi menor em pacientes recebendo G+B (24%) em comparação com pacientes recebendo apenas B (32%). A incidência de reações infusionais em infusões subsequentes foi comparável nos dois braços e diminuiu com cada ciclo. As reações infusionais também foram observadas em 8% dos pacientes durante o período de manutenção com Gazyva. No total, 3% dos pacientes apresentaram uma reação infusional levando à descontinuação de Gazyva.
Neutropenia e infecções:
Leucemia Linfocítica Crônica:
A incidência de neutropenia foi maior no braço tratado com Gazyva mais clorambucil em comparação com o braço tratado com rituximabe mais clorambucil, com a resolução espontânea da neutropenia ou com o uso de fatores estimulantes de colônias de granulócitos (injeção que aumenta o número de glóbulos brancos).
A incidência de infecção foi de 38% no braço tratado com Gazyva mais clorambucil e 37% no braço tratado com rituximabe mais clorambucil (com eventos de Graus 3-5 reportados em 12% e 14%, respectivamente, e eventos fatais reportados em < 1% em ambos os braços de tratamento). Casos de neutropenia prolongada (2% no braço tratado com Gazyva mais clorambucil e 4% no braço com rituximabe mais clorambucil) e neutropenia de início tardio (16% no braço tratado com Gazyva mais clorambucil e 12% no braço com rituximabe mais clorambucil) também foram relatados.
Linfoma Não-Hodgkin
A incidência de neutropenia foi maior no braço G+B em comparação com o braço tratado apenas com B. A incidência de infecção foi de 66% no braço G+B e 57% no braço B (com eventos Graus 3-5 reportados em 18% e 17%, respectivamente, e eventos fatais reportados em 3% e 4%, respectivamente). Os casos de neutropenia prolongada (3% no G+B) e neutropenia de início tardio (7% no G+B) também foram reportados.
Trombocitopenia:
Leucemia Linfocítica Crônica:
A incidência de plaquetas baixas foi maior no braço com Gazyva mais clorambucil em comparação com o braço querecebeu rituximabe mais clorambucil, especialmente durante o primeiro ciclo do tratamento. Quatro por cento dos pacientes no braço com Gazyva mais clorambucil apresentaram trombocitopenia aguda (ocorrendo em 24 horas depois da infusão).
A incidência geral de eventos hemorrágicos foi similar no braço tratado com Gazyvae o braço tratado com rituximabe. O número de eventos hemorrágicos fatais foi equilibrado entre os braços de tratamento; no entanto, todos os eventos em pacientes tratados com Gazyva foram reportados no Ciclo 1. Uma relação clara entre trombocitopenia e eventos hemorrágicos não foi estabelecida.
Linfoma Não-Hodgkin
A incidência de trombocitopenia foi menor no braço G+B (15%) em comparação com o braço tratado apenas com (24%). A incidência de eventos hemorrágicos (11% G+B, 10% B) e eventos hemorrágicos Graus 3-5 (5% G+B, 3% B) foi similar nos dois braços de tratamento sem nenhum evento fatal reportado.
Leucoencefalopatia Multifocal Progressiva (LEMP) foi relatada em pacientes tratados com Gazyva.
Foram relatados casos de reativação da hepatite B e eventos cardíacos fatais em pacientes tratados com Gazyva.
Casos de perfuração gastrintestinal foram reportados em pacientes recebendo Gazyva, principalmente em LNH.
Elevações transitórias das enzimas hepáticas (AST, ALT, ALP) foram observadas logo após a primeira infusão de Gazyva.
Atenção: Este produto é um medicamento que possui nova indicação terapêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos imprevisíveis ou desconhecidos.
Nesse caso, notifique os eventos adversos pelo Sistema de Notificação em Vigilância Sanitária – NOTIVISA disponível em http://www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
Composição
Cada frasco-ampola de dose única com 40 mL contém:
Obinutuzumabe - 1000 mg (25 mg/mL).
Excipientes: Histidina, cloridrato de histidina monoidratado, trealose di-hidratada, Poloxamer 188 e água para injetáveis.
Superdosagem
Não existe nenhuma experiência com administração de dose excessiva (superdose) em estudos clínicos em seres humanos. Em estudos clínicos, foram administradas doses de Gazyva variando de 50 mg até 2000 mg por infusão. A frequência e a intensidade das reações adversas não parecem depender da dose.
Pacientes que apresentarem uma superdose devem ter sua infusão imediatamente interrompida ou reduzida e devem ser monitorados cuidadosamente. Deve-se considerar o monitoramento regular do número de linfócitos por meio de exames de sangue regulares e o risco aumentado de infecções pela redução das defesas naturais do organismo.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Não foram realizados estudos formais de interação droga-droga. O risco de interações com outros medicamentos usados concomitantemente não pode ser descartado.
Ação da Substância
Resultados de Eficácia
Estudo clínico fase III, internacional, multicêntrico, aberto, randomizado, realizado em dois estágios, com três braços (BO21004/CLL11) para investigar o perfil de segurança e eficácia de Obinutuzumabe (substância ativa) mais clorambucil (G-Clb) em comparação com rituximabe mais clorambucil ou clorambucil (Clb) isolado foi conduzido incluindo pacientes com leucemia linfocítica crônica não tratados previamente com comorbidades.
Antes da inclusão, os pacientes precisavam apresentar LLC, CD20 positivo e uma ou ambas das seguintes medidas de condições clínicas coexistentes: escore de comorbidade (escala CIRS) maior que 6 ou função renal reduzida mensurada pela depuração de creatinina (CrCl) < 70 mL/min. Pacientes com função hepática [NCICTC Grau 3 para testes de função hepática (AST, ALT > 5 x ULN por mais de 2 semanas; bilirrubina > 3 x ULN)] e função renal (CrCl < 30 mL/min) não adequadas foram excluídos.
Um total de 781 pacientes foi randomizado na proporção de 2:2:1 para receber Obinutuzumabe (substância ativa) mais clorambucil, rituximabe mais clorambucil ou clorambucil isolado. O Estágio 1 comparou Obinutuzumabe (substância ativa) mais clorambucil com clorambucil isolado em 356 pacientes e o Estágio 2 comparou Obinutuzumabe (substância ativa) mais clorambucil com rituximabe mais clorambucil em 663 pacientes. Os resultados de eficácia estão resumidos na Tabela 1 e nas Figuras 1-3.
Na maioria dos pacientes, Obinutuzumabe (substância ativa) foi administrado por via intravenosa na dose inicial de 1000 mg nos Dias 1, 8 e 15 do primeiro ciclo de tratamento. Para reduzir a porcentagem de reações infusionais nos pacientes, 140 deles receberam a primeira dose de Obinutuzumabe (substância ativa) administrada em dois dias [Dia 1 (100 mg) e o Dia 2 (900 mg)]. Para cada ciclo de tratamento subsequente (Ciclos 2 a 6), os pacientes receberam 1000 mg de Obinutuzumabe (substância ativa) no Dia 1 apenas. O clorambucil foi administrado oralmente na dose de 0,5 mg/kg de peso corporal nos dias 1 e 15 de todos os ciclos de tratamento (1 a 6).
Os dados demográficos e as características basais foram bem equilibrados entre os grupos de tratamento. A maioria dos pacientes incluídos era caucasiana (95%) e do sexo masculino (61%). A mediana de idade foi de 73 anos, sendo que 44% tinham 75 anos de idade ou mais. No período basal, 22% dos pacientes apresentavam estadio A de Binet, 42% apresentavam estadio B e 36%, estadio C. O escore mediano de comorbidade foi 8 e 76% dos pacientes incluídos apresentavam escore de comorbidade acima de 6. A mediana estimada de CrCl foi de 62 mL/min e 66% de todos os pacientes apresentavam CrCl < 70 mL/min. Quarenta e dois por cento dos pacientes incluídos apresentavam tanto CrCl < 70 mL/min como um escore de comorbidade > 6. Trinta e quatro por cento dos pacientes foram incluídos no escore de comorbidade isolado e 23% com função renal comprometida somente.
As condições clínicas coexistentes mais frequentemente reportadas (usando um corte de 30% ou mais) no sistema MedDRA são: distúrbios vasculares (73%), distúrbios cardíacos (46%), distúrbios gastrintestinais (38%), distúrbios do metabolismo e nutrição (40%), distúrbios renais e urinário (38%) e distúrbios musculoesqueléticos e do tecido conectivo (33%).
O desfecho primário do estudo foi a sobrevida livre de progressão (SLP) avaliada pelo investigador (SLP-INV). Além disso, uma comissão de revisão independente (IRC) avaliou todos os pacientes com relação à progressão e avaliou a SLP (SLP-IRC).
Os principais desfechos secundários de eficácia foram o percentual de resposta no final do tratamento, a remissão molecular no final do tratamento (doença residual mínima) e o tempo até desfechos (sobrevida livre de evento, nova terapia antileucêmica). A sobrevida global para o Estágio 1 é apresentada na Figura 2. A sobrevida global para o Estágio 2 continuará sendo acompanhada e os dados são ainda imaturos.
Tabela 1. Resumo de eficácia do estudo BO21004/CLL11
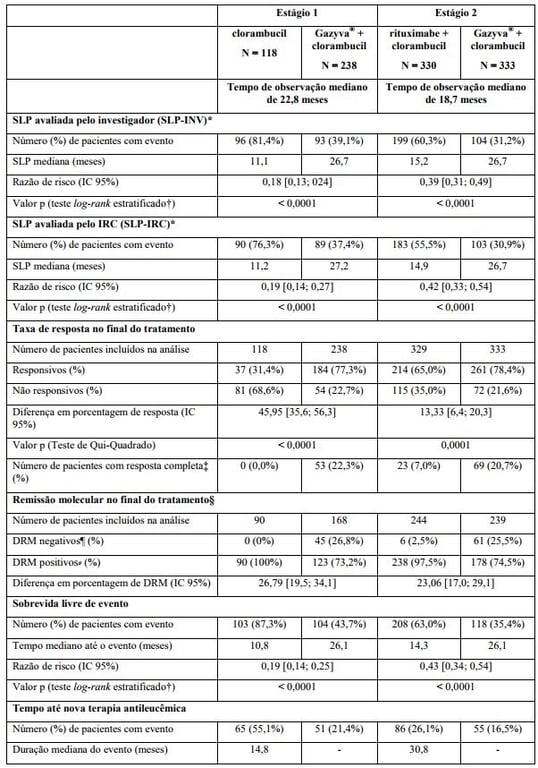
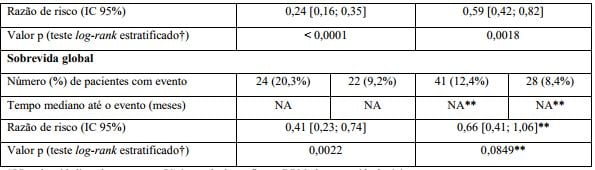
SLP: sobrevida livre de progressão; IC: intervalo de confiança; DRM: doença residual mínima.
* Definida como o tempo desde a randomização até a primeira ocorrência de progressão, recidiva ou óbito por qualquer causa conforme avaliação do investigador.
† Estratificado por estágio Binet no período basal.
‡ Inclui 11 pacientes no braço G-Clb com uma resposta completa e recuperação incompleta da medula.
§ Sangue e medula óssea combinados.
¶ Negatividade DRM definida como resultado abaixo de 0,0001.
? Inclui pacientes DRM positivos e pacientes que progrediram ou morreram antes do final do tratamento NA = não alcançado.
** Dado ainda imaturo.
Resultados da análise de SLP do subgrupo (sexo, idade, estágios de Binet, CrCl, escore CIRS, beta2-microglobulina, estado mutacional do IgVH, anormalidades cromossômicas, contagem de linfócitos no período basal) foram compatíveis com os resultados observados no total da população com intenção de tratamento (ITT). O risco de progressão da doença ou óbito (SLP) foi reduzido no braço Obinutuzumabe (substância ativa) mais clorambucil (GClb), em comparação com o braço que recebeu rituximabe mais clorambucil (RClb) e clorambucil isolado (Clb) em todos os subgrupos. A razão de risco variou de 0,08 a 0,42 para GClb vs. Clb e 0,28 a 0,71 para GClb vs. RClb.
Figura 1. Curva de Kaplan-Meier de Sobrevida Livre de Progressão do Estágio 1 Avaliada pelo Investigador
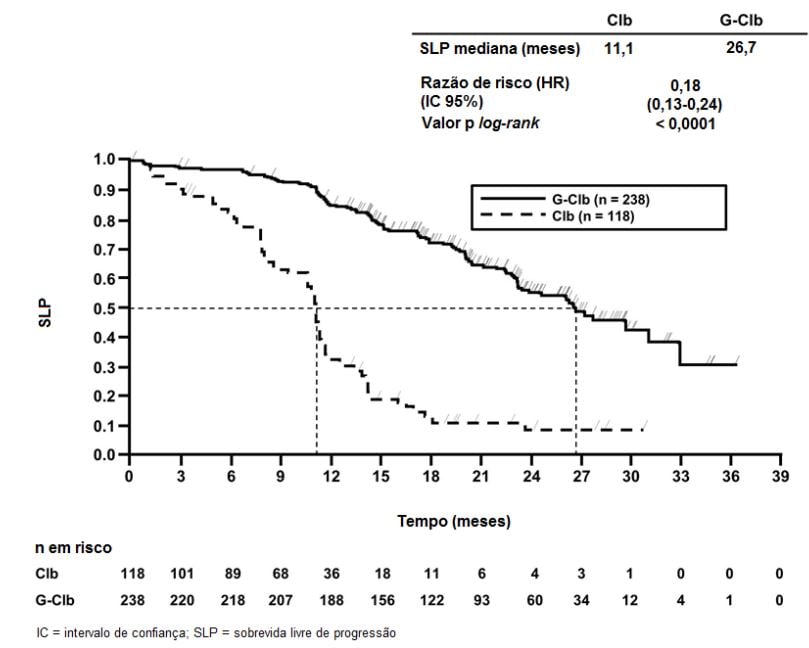
Figura 2. Curva de Kaplan-Meier de Sobrevida Global do Estágio 1
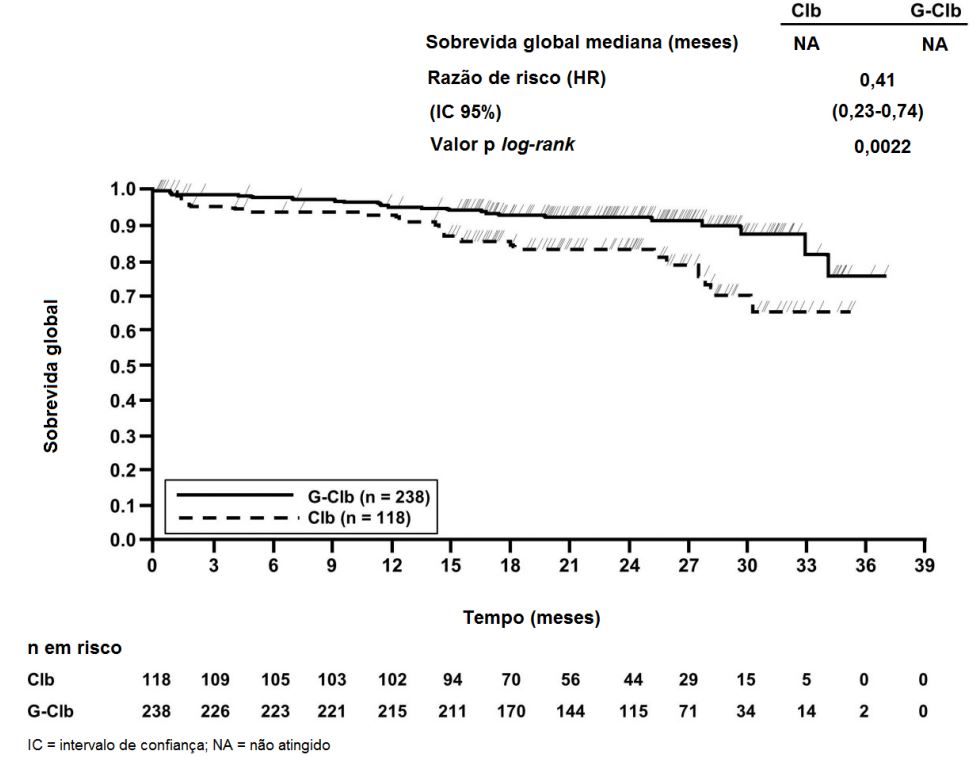
Figura 3. Curva de Kaplan-Meier de Sobrevida Livre de Progressão do Estágio 2 Avaliada pelo Investigador
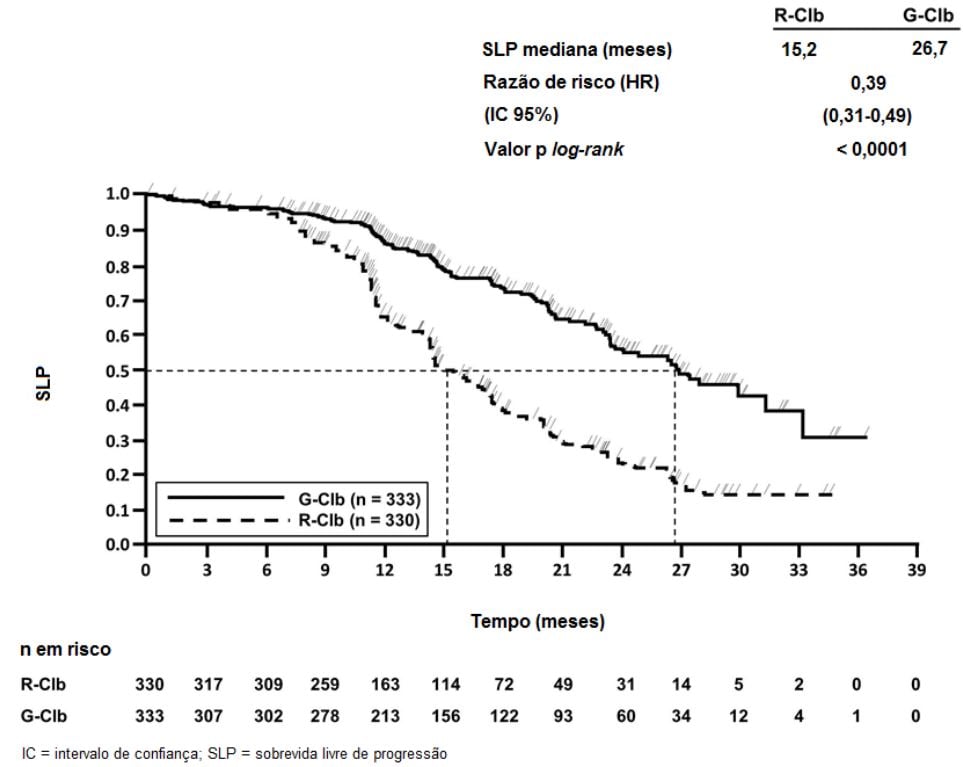
Resultados Reportados pelos Pacientes
Nos questionários QLQC30 e QLQ-CLL-16, conduzidos durante o período de tratamento, não foi observada nenhuma diferença substancial em nenhuma das subescalas. Dados durante o acompanhamento, especialmente para o braço clorambucil isolado, são limitados. No entanto, nenhuma diferença notável foi identificada até o momento durante o acompanhamento do parâmetro qualidade de vida.
Avaliações de qualidade de vida relacionada à saúde, específicas para fadiga durante o período de tratamento, não mostram diferença estatisticamente significativa sugerindo que a adição de Obinutuzumabe (substância ativa) ao regime de tratamento com clorambucil não aumenta a sensação de fadiga para os pacientes.
Imunogenicidade
Pacientes no estudo pivotal BO21004/CLL11 foram testados em vários momentos para anticorpos antidrogas (ATA) contra Obinutuzumabe (substância ativa) . Nos pacientes tratados com Obinutuzumabe (substância ativa) , 8 de 140 na fase randomizada e 2 em 6 na fase de inclusão tiveram testes positivos para ATA em 12 meses de acompanhamento. Desses pacientes, nenhum apresentou reações anafiláticas ou de hipersensibilidade consideradas relacionadas aos ATA, tampouco a resposta clínica foi afetada.
Resultados de ensaio de imunogenicidade são altamente dependentes de diversos fatores, incluindo sensibilidade e especificidade do ensaio, sua metodologia, robustez a quantidade de Obinutuzumabe (substância ativa) circulante, manipulação de amostras, cronograma de coleta de amostras, medicações concomitantes e doença subjacente. Por essas razões, a comparação da incidência de anticorpos contra Obinutuzumabe (substância ativa) com a incidência de anticorpos contra outros medicamentos pode estar equivocada.
Características Farmacológicas
Propriedades Farmacodinâmicas
Mecanismo de ação
Obinutuzumabe (substância ativa) é um anticorpo monoclonal humanizado recombinante Tipo II anti-CD20 do isotipo IgG1 e produzido por glicoengenharia. É especificamente direcionado à alça extracelular do antígeno transmembrana CD20 na superfície de linfócitos pré-B e B maduros não malignos e malignos, mas não sobre células-tronco hematopoiéticas, células pro-B, plasmócitos normais ou outros tecidos normais. A glicoengenharia da porção Fc de Obinutuzumabe (substância ativa) resulta em maior afinidade por receptores Fc?RIII sobre células imunoefetoras, como células NK (Natural Killer) e macrófagos e monócitos em comparação com anticorpos não produzidos por glicoengenharia.
Em estudos não clínicos, Obinutuzumabe (substância ativa) induz morte celular direta e é mediador de citotoxicidade celular dependente de anticorpos (CCDA) e fagocitose celular dependente de anticorpos (FCDA) por meio do recrutamento de células imunoefetoras positivas Fc?RIII. Além disso, Obinutuzumabe (substância ativa) apresenta baixo grau de citotoxicidade dependente do complemento (CDC). Em modelos animais, Obinutuzumabe (substância ativa) induz depleção potente de células B com eficácia antitumoral. Em comparação com anticorpos CD20 Tipo I, Obinutuzumabe (substância ativa) , um anticorpo Tipo II, é caracterizado por uma indução aumentada de morte celular direta com redução concomitante de CDC. Comparado a anticorpos anti-CD20 não produzidos por glicoengenharia, Obinutuzumabe (substância ativa) se caracteriza por aumento da citotoxicidade celular dependente de anticorpos (CCDA) como consequência da glicoengenharia. Isso se traduz em depleção de células B e eficácia antitumoral superiores em modelos animais.
Efeitos farmacodinâmicos
No estudo clínico pivotal BO21004/CLL11, 91% (40 em 44) dos pacientes passíveis de avaliação tratados com Obinutuzumabe (substância ativa) apresentaram depleção de células B (definido como número de células B CD19+ < 0,07 x 109 /L) no final do período de tratamento e permaneceram depletados durante os primeiros 6 meses de acompanhamento. A recuperação das células B foi observada dentro de 12 a 18 meses de acompanhamento em 35% (14 de 40) dos pacientes sem doença progressiva e 13% (5 de 40) com doença progressiva.
Propriedades Farmacocinéticas
Foi desenvolvido um modelo farmacocinético populacional para analisar dados farmacocinéticos de 678 pacientes com LNH (linfoma não Hodgkin) ou LLC que receberam Obinutuzumabe (substância ativa) nos estudos Fase I, II e III, o qual foi utilizado para descrever as características farmacocinéticas de obinutuzumabe em pacientes com LLC.
Absorção
Obinutuzumabe (substância ativa) é administrado por via intravenosa, portanto a absorção não se aplica nesse caso. Não foram realizados estudos clínicos com outras vias de administração. A partir do modelo farmacocinético populacional, após infusão do Dia 1 do Ciclo 6 em pacientes com LLC, o valor mediano estimado de Cmax foi 473,2 µg/mL e o valor de AUC(T) foi 9516 µg.d/mL.
Distribuição
Depois da administração intravenosa, o volume de distribuição do compartimento central (2,76 L) se aproxima ao volume do soro, o que indica que a distribuição é, em grande parte, restrita ao plasma e ao líquido intersticial.
Metabolismo
O metabolismo de Obinutuzumabe (substância ativa) não foi estudado diretamente. A maior parte dos anticorpos é eliminada por catabolismo.
Eliminação
A depuração de Obinutuzumabe (substância ativa) no Ciclo 6 em pacientes com LLC é de aproximadamente 0,083 L/dia com uma t ½ de eliminação mediana de 30,3 dias. A depuração de Obinutuzumabe (substância ativa) compreende um modelo de depuração com tempo variável com duas vias paralelas que a descrevem: uma via de depuração linear e uma não linear que se altera em função do tempo.
Durante o início do tratamento, a via de depuração não linear variável com o tempo é dominante e responde pela principal via de depuração. À medida que o tratamento progride, o impacto dessa via diminui e a via de depuração linear predomina.
Esse é um indicativo de target mediated drug disposition (TMDD), em que a abundância inicial de células CD20 causa uma depleção rápida de Obinutuzumabe (substância ativa) . No entanto, quando a maior parte das células CD20 fica ligada a Obinutuzumabe (substância ativa) , existe uma redução do impacto de TMDD sobre a farmacocinética.
Farmacocinética em populações especiais
Na análise de farmacocinética populacional, o sexo se revelou uma covariável que justifica algumas das variabilidades entre os pacientes, com uma depuração em estado de equilíbrio dinâmico (CLss) 22% maior e um volume de distribuição (V) 18% maior no sexo masculino. No entanto, os resultados da análise populacional mostraram que as diferenças em exposição não são significativas (com uma mediana estimada de AUC e Cmax de 11282 µg*d/mL e 578,9 µg/mL no sexo feminino e 8451 µg*d/mL e 432,5 µg/mL no sexo masculino, respectivamente, no Ciclo 6), indicando que não existe a necessidade de ajuste de dose baseado no sexo.
Pacientes Idosos
A análise farmacocinética populacional de Obinutuzumabe (substância ativa) mostrou que a idade não afeta a sua farmacocinética. Nenhuma diferença significativa foi observada na farmacocinética de Obinutuzumabe (substância ativa) entre pacientes < 65 anos (n = 265), pacientes entre 65 e 75 anos (n = 197) e pacientes > 75 anos (n = 128).
Pacientes Pediátricos
Não foram conduzidos estudos para investigar a farmacocinética de Obinutuzumabe (substância ativa) em crianças.
Insuficiência renal
A análise farmacocinética populacional de Obinutuzumabe (substância ativa) mostrou que a depuração de creatinina não afeta a farmacocinética do produto. A farmacocinética de Obinutuzumabe (substância ativa) em pacientes com depuração de creatinina levemente diminuída (CrCl 50-89 mL/min, n = 306) ou moderadamente diminuída (CrCl 30 a 49 mL/min, n = 72) foi semelhante à de pacientes com função renal normal (CrCl ? 90 mL/min, n = 207). Dados farmacocinéticos em pacientes com insuficiência renal grave (CrCl 15-29 mL/min) são limitados (n = 5), portanto, não é possível fazer nenhuma recomendação específica de dose.
Insuficiência Hepática
Não foram conduzidos estudos formais de farmacocinética e nenhum dado de farmacocinética populacional foi coletado em pacientes com insuficiência hepática.
Segurança pré-clínica
Carcinogenicidade
Não foram realizados estudos de carcinogenicidade para estabelecer o potencial carcinogênico de Obinutuzumabe (substância ativa).
Mutagenicidade
Não foram realizados estudos para estabelecer o potencial mutagênico de Obinutuzumabe (substância ativa).
Comprometimento da Fertilidade
Não foram realizados estudos específicos em animais para avaliar o efeito de Obinutuzumabe (substância ativa) sobre a fertilidade. Nenhum evento adverso sobre órgãos reprodutores masculinos e femininos foi observado em estudos de toxicidade de dose repetida em macacos cynomolgus.
Teratogenicidade
Um estudo de toxicidade sobre o desenvolvimento pré e pós-natal foi realizado em macacas cynomolgus prenhes. Os animais receberam doses intravenosas semanais de Obinutuzumabe (substância ativa) [médias de AUC0-168h em estado de equilíbrio (no Dia 139 p.c.) foram de 125.000 e 250.000 (µg.h)/mL com 25 e 50 mg/kg, respectivamente; a Cmax média foi 1.220 e 2.470 µg/mL com 25 e 50 mg/kg, respectivamente] durante a gestação (período de organogênese; Dia 20 pós-coito até o parto).
Os filhotes expostos não apresentaram nenhum efeito teratogênico, mas as células B estavam completamente depletadas no Dia 28 pós-parto. As exposições dos filhotes no Dia 28 pós parto sugerem que Obinutuzumabe (substância ativa) pode atravessar a barreira hematoplacentária. As concentrações no soro do filhote no Dia 28 pós-parto estavam na faixa das concentrações do soro materno, enquanto que as concentrações no leite no mesmo dia eram muito baixas (menos que 0,5% dos níveis séricos maternos correspondentes), sugerindo que a exposição dos filhotes deve ter ocorrido dentro do útero. O número de células B retornou a níveis normais e a função imunológica foi restaurada dentro de 6 meses a partir do parto.
Outros
Em um estudo de 26 semanas com macacos cynomolgus, reações de hipersensibilidade foram notadas e atribuídas ao reconhecimento do anticorpo humanizado como estranho nesses macacos (Cmax e AUC0-168h em estado de equilíbrio - Dia 176 - depois da administração semanal de 5, 25 e 50 mg/kg foram 377, 1530 e 2920 µg/mL e 39.800, 183.000 e 344.000 (µg.h)/mL, respectivamente).
Os achados incluíram reações anafiláticas ou anafilactoides agudas e aumento da prevalência de inflamação sistêmica e infiltrados compatíveis com reações de hipersensibilidade mediadas por imunocomplexos, como arterite/periarterite, glomerulonefrite e inflamação serosa/adventícia.
Essas reações levaram à exclusão não programada de 6/36 animais tratados com Obinutuzumabe (substância ativa) durante as fases de administração e recuperação; essas alterações foram parcialmente reversíveis. Não se observou nenhuma toxicidade renal de relação causal com Obinutuzumabe (substância ativa) em seres humanos.
Cuidados de Armazenamento
Antes de aberto, Gazyva deve ser conservado sob refrigeração (entre 2°C e 8°C).
O produto deve ser mantido na embalagem original, de forma a protegê-lo da luz. Não congelar. Não agitar.
O profissional da saúde saberá como armazenar a solução para infusão contendo Gazyva.
Número de lote e datas de fabricação e validade: Vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Característica física
Gazyva é um líquido límpido, incolor a levemente castanho, fornecido em dose única de 1000 mg em um frasco- ampola de vidro estéril, isento de conservantes, não pirogênico, contendo 40 mL de líquido concentrado (25 mg/mL).
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Descarte de medicamentos não utilizados e/ou com data de validade vencida
O descarte de medicamentos no meio ambiente deve ser minimizado. Os medicamentos não devem ser descartados no esgoto, e o descarte em lixo doméstico deve ser evitado. Utilize o sistema de coleta local estabelecido, se disponível.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Dizeres Legais
MS-1.0100.0660
Farm. Resp.:
Tatiana Tsiomis Díaz - CRF-RJ n°. 6942
Fabricado para:
F. Hoffmann-La Roche Ltd, Basileia, Suíça
Por Roche Diagnostics GmbH, Mannheim, Alemanha
Embalado por:
F. Hoffmann-La Roche Ltd, Kaiseraugst, Suíça
Registrado, importado e distribuído no Brasil por:
Produtos Roche Químicos e Farmacêuticos S.A.
Est. dos Bandeirantes, 2020
CEP 22775-109 - Rio de Janeiro - RJ CNPJ 33.009.945/0023-39
Serviço Gratuito de Informações – 0800 7720 289
Uso retrito a hospitais.
Venda sob prescrição médica.
Comparar preços de remédios e medicamentos no CliqueFarma é rápido e simples.
O CliqueFarma, é uma ferramenta para comparativo de preços de produtos farmacêuticos. Não comercializamos, não indicamos, não receitamos, nenhum tipo de medicamento essa função cabe exclusivamente a médicos e farmacêuticos. Não consuma qualquer tipo de medicamento sem consultar seu médico.
SE PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO. PROCURE UM MÉDICO E O FARMACÊUTICO. LEIA A BULA.
Conheça nossos Termos de Uso