para o que é indicado e para que serve?
Cancidas é indicado para tratar um dos vários tipos de infecções fúngicas descritos a seguir: Uma infecção fúngica grave chamada candidíase invasiva: Essa infecção é causada por células fúngicas (leveduras) chamadas Candida.Continue lendo...
ofertas de
Cancidas - 50Mg 1 Ampola
ofertas de Cancidas - 50Mg 1 Ampola
R$ 1.100,00
R$ 2.960,00
R$ 3.271,00
R$ 3.280,00
ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
Cancidas é indicado para tratar um dos vários tipos de infecções fúngicas descritos a seguir:
Como o Cancidas funciona?
Cancidas é um antifúngico que interfere na produção de um componente (polissacarídeo glucana) da parede da célula fúngica, essencial à vida e ao crescimento do fungo. As células fúngicas expostas a Cancidas apresentam paredes celulares incompletas ou defeituosas, o que as torna frágeis e incapazes de se desenvolver.
Contraindicação
Cancidas é contraindicado para pacientes com hipersensibilidade a qualquer componente do produto.
Como usar
Cancidas deve ser administrado em dose única diária por infusão intravenosa lenta de aproximadamente 1 hora. O médico irá determinar a duração do tratamento e a quantidade diária de Cancidas a ser administrada.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar o Cancidas?
O esquema terapêutico e a dose serão determinados pelo seu médico, que irá monitorar a sua resposta e condição clínica. Se você estiver preocupado(a) com a possibilidade de ter deixado de receber uma dose, fale com seu médico imediatamente.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Durante a administração de Cancidas, reações alérgicas com risco de morte foram relatadas raramente. Foram relatados sinais ou sintomas possivelmente mediados pela histamina, incluindo erupção cutânea, inchaço do rosto e/ou dos lábios, prurido, sensação de calor ou dificuldade respiratória. Cancidas também pode causar reações adversas graves à pele, incluindo descamação da pele, úlceras na membrana mucosa, urticária ou descamação de grandes áreas da pele. Informe o seu médico ou farmacêutico imediatamente sobre esses ou quaisquer outros sinais ou sintomas incomuns que apresentar.
Informe o seu médico sobre qualquer condição médica e sobre qualquer tipo de alergia que esteja apresentando ou tenha apresentado.
Reações Adversas
Qualquer medicamento pode apresentar efeitos adversos ou indesejados, denominados reações adversas.
As reações adversas relacionadas a Cancidas mais comuns (ocorrem em 10% dos pacientes que utilizam este medicamento) em adultos são febre e irritações na veia no local da infusão (prurido, vermelhidão, inchaço ou formação de coágulos).
Outros efeitos indesejáveis relatados relacionados a este medicamento em adultos incluem:
Dor de cabeça; dor; calafrios; batimentos cardíacos acelerados; sudorese; náusea; diarreia; vômito; rubor da face e do pescoço; erupção cutânea; coceira; dificuldade para respirar; inchaço nas mãos, tornozelos ou pés; prejuízo da função hepática e alterações de alguns testes laboratoriais de sangue.
As reações adversas relacionadas a Cancidas mais comuns (ocorrem em 10% dos pacientes que utilizam este medicamento) em crianças e adolescentes são febre, erupção cutânea e dor de cabeça.
Outros efeitos indesejáveis relatados relacionados a este medicamento em crianças e adolescentes incluem:
Dor no local da infusão calafrios, batimentos cardíacos rápidos, rubor da face e do pescoço, coceira, baixa pressão arterial e alterações em alguns testes laboratoriais.
Raramente (ocorrem entre 0,01% e 0,1% dos pacientes que utilizam este medicamento) foram relatadas reações alérgicas potencialmente fatais durante a administração de Cancidas.
Foram relatados sinais ou sintomas possivelmente mediados pela histamina, incluindo erupções cutâneas, inchaço da face e/ou lábios, coceira, sensação de calor ou dificuldade para respirar; além disso, podem ocorrer raramente outros efeitos além dos citados e, a exemplo do que ocorrem com qualquer medicação obtida somente com prescrição médica, alguns podem ser graves. Peça mais informações ao seu médico ou farmacêutico.
Adicionalmente, durante a comercialização do medicamento, as seguintes reações foram reportadas:
Erupção cutânea, descamação da pele, feridas nas membranas mucosas, urticária, grandes áreas de descamação da pele.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
População Especial
Gravidez e amamentação:
Informe imediatamente o seu médico em caso de suspeita de gravidez. Não há experiência clínica envolvendo mulheres grávidas. Em estudos com animais, demonstrou-se que a caspofungina ultrapassa a barreira placentária.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Não se sabe se essa medicação é excretada no leite humano, portanto, mulheres que estejam recebendo Cancidas não devem amamentar.
Crianças:
Cancidas foi aprovado para uso em crianças e adolescentes (de 3 meses até 17 anos de idade) para todos os tipos de infecção descritos anteriormente. A dose utilizada em pacientes pediátricos pode diferir da dose utilizada em pacientes adultos. Cancidas não foi estudado adequadamente em bebês com menos de 3 meses de idade.
Idosos:
Não é necessário ajuste da dose para pacientes idosos.
Uso em pacientes com insuficiência renal:
Não é necessário ajuste posológico para pacientes com insuficiência renal.
Uso em pacientes com insuficiência hepática:
Alguns pacientes com problemas hepáticos podem necessitar de ajuste de dose. Informe o seu médico se apresenta ou já apresentou problemas hepáticos.
Dirigir ou operar máquinas:
Não existem informações sugestivas de que Cancidas afete a capacidade de conduzir veículos ou operar máquinas
Composição
Cada frasco-ampola de Cancidas 50 mg contém:
55,5 mg de acetato de caspofungina, que equivale a 50 mg de base anidra livre de caspofungina.
Cada frasco-ampola de Cancidas 70 mg contém:
77,7 mg de acetato de caspofungina, que equivale a 70 mg de base anidra livre de caspofungina.
Excipientes: sacarose, manitol, ácido acético e hidróxido de sódio (para ajustar o pH).
Superdosagem
O esquema terapêutico e a dose serão determinados pelo seu médico, que irá monitorar as suas condições clínicas e a resposta ao tratamento. Caso tenha recebido uma quantidade muito alta de Cancidas, fale com seu médico imediatamente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Estudos in vitro mostram que o Acetato de Caspofungina (substância ativa) não é um inibidor de nenhuma enzima do sistema do citocromo P450 (CYP). Em estudos clínicos, a caspofungina não induziu o metabolismo pela via do CYP3A4 de outras medicações. A caspofungina não é um substrato para a glicoproteína-P e é um substrato fraco para as enzimas do citocromo P450.
Em dois estudos clínicos, a ciclosporina (uma dose de 4 mg/kg ou duas doses de 3 mg/kg) aumentou a AUC da caspofungina em aproximadamente 35%. Esses aumentos da AUC são provavelmente devidos à captação reduzida de caspofungina pelo fígado.
Acetato de Caspofungina (substância ativa) não aumentou os níveis plasmáticos de ciclosporina.
Ocorreram aumentos transitórios de ALT e AST quando Acetato de Caspofungina (substância ativa) e ciclosporina foram administrados concomitantemente. Em um estudo retrospectivo que envolveu 40 pacientes tratados durante o período de comercialização com Acetato de Caspofungina (substância ativa) e/ou ciclosporina por 1 a 290 dias (mediana de 17,5 dias), não foram observados eventos adversos hepáticos graves.
Estudos clínicos com voluntários saudáveis mostram que a farmacocinética de Acetato de Caspofungina (substância ativa) não é alterada por itraconazol, anfotericina B, micofenolato, nelfinavir ou tacrolimo. Acetato de Caspofungina (substância ativa) não exerce efeito na farmacocinética de itraconazol, anfotericina B, rifampicina ou do metabólito ativo do micofenolato.
Acetato de Caspofungina (substância ativa) reduziu em 26% a concentração sanguínea de 12 horas (C12h) de tacrolimo (FK-506) em voluntários adultos saudáveis. Para os pacientes que estejam recebendo as duas terapias, recomenda-se a monitoração padrão das concentrações sanguíneas do tacrolimo e seu ajuste posológico adequado.
Os resultados de dois estudos clínicos de interação medicamentosa em voluntários adultos saudáveis indicaram que a rifampicina tanto induz como inibe a disposição da caspofungina com indução líquida no estado de equilíbrio.
Em um dos estudos, o tratamento tanto com rifampicina como com caspofungina foi iniciado simultaneamente e ambos os fármacos foram administrados concomitantemente durante 14 dias; no segundo estudo, a rifampicina foi administrada isoladamente durante 14 dias para permitir ao efeito de indução alcançar o estado de equilíbrio até que, por fim, a rifampicina e a caspofungina foram coadministradas durante mais 14 dias.
Quando o efeito de indução da rifampicina estava no estado de equilíbrio, houve pequena alteração na AUC da caspofungina ou na concentração no final da infusão, mas as concentrações de caspofungina no vale foram reduzidas em aproximadamente 30%.
Demonstrou-se o efeito inibitório da rifampicina quando o tratamento com a rifampicina e o Acetato de Caspofungina (substância ativa) foram iniciados simultaneamente; a elevação transiente nas concentrações plasmáticas de caspofungina ocorreu no primeiro dia (aumento de aproximadamente 60% na AUC).
Esse efeito inibitório não foi observado quando a caspofungina foi adicionada à terapia preexistente com rifampicina e não ocorreu elevação das concentrações de caspofungina. Além disso, os resultados da triagem da população farmacocinética em adultos sugerem que a administração concomitante de outros indutores da depuração de medicamentos (efavirenz, nevirapina, fenitoína, dexametasona ou carbamazepina) com Acetato de Caspofungina (substância ativa) pode também resultar em reduções clinicamente significativas das concentrações de caspofungina.
Os dados disponíveis sugerem que o mecanismo indutível de depuração de medicamentos envolvido na disposição da caspofungina é provavelmente um processo de transporte de captação e não de metabolismo; portanto, quando Acetato de Caspofungina (substância ativa) é administrado em pacientes adultos concomitantemente com indutores da depuração de medicamentos, como efavirenz, nevirapina, rifampicina, dexametasona, fenitoína ou carbamazepina, deve-se considerar a administração da dose diária de 70 mg de Acetato de Caspofungina (substância ativa).
Em pacientes pediátricos, os resultados das análises de regressão dos dados farmacocinéticos sugerem que a coadministração de dexametasona e Acetato de Caspofungina (substância ativa) pode resultar em reduções clinicamente significativas nas concentrações de vale da caspofungina. Esse achado pode indicar que pacientes pediátricos terão reduções similares com indutores conforme observado em adultos. Quando Acetato de Caspofungina (substância ativa) é coadministrado em pacientes pediátricos com indutores de depuração do fármaco, como rifampicina, efavirenz, nevirapina, fenitoína, dexametasona, ou carbamazepina, deve-se considerar uma dose de Acetato de Caspofungina (substância ativa) de 70 mg/m2 diariamente (sem exceder uma dose diária real de 70 mg).
Estudos in vitro e in vivo com Acetato de Caspofungina (substância ativa) em combinação com anfotericina B não demonstram antagonismo da atividade antifúngica contra A. fumigatus ou C. albicans. Os resultados dos estudos in vitro sugerem alguma evidência de atividade aditiva/indiferente ou sinérgica contra A. fumigatus e atividade aditiva/indiferente contra C. albicans. A significância clínica desses resultados é desconhecida.
Ação da Substância
Resultados de eficácia
Os resultados dos estudos clínicos que incluíram adultos são apresentados por cada indicação abaixo, seguidos dos resultados dos estudos clínicos pediátricos.
Tratamento empírico em paciente neutropênico febril
Um estudo duplo-cego e multicêntrico envolveu 1.111 pacientes neutropênicos febris distribuídos de forma randômica para receber doses diárias de Acetato de Caspofungina (substância ativa) (50 mg/dia após uma dose de ataque de 70 mg no 1º dia) ou de anfotericina B lipossomal injetável (3,0 mg/kg/dia).
Os pacientes elegíveis haviam recebido quimioterapia para tumores malignos ou sido submetidos a transplante de células-tronco hematopoiéticas (TCTH) e apresentavam neutropenia (< 500 células/mm3 durante 96 horas) e febre (> 38,0ºC) que não respondiam ao tratamento antibacteriano; pacientes com infecção fúngica documentada foram excluídos do estudo. Os pacientes foram tratados até a resolução da neutropenia, por no máximo 28 dias, e aqueles que apresentavam infecção fúngica documentada puderam ser tratados durante mais tempo.
Se o medicamento fosse bem tolerado, mas a febre persistisse e a condição clínica piorasse após 5 dias de tratamento, a dose poderia ser aumentada para 70 mg/dia de Acetato de Caspofungina (substância ativa) (13,3% dos pacientes tratados) ou 5,0 mg/kg/dia de anfotericina B lipossomal injetável (14,3% dos pacientes tratados).
Os pacientes foram estratificados com base na categoria de risco (pacientes de alto risco haviam sido submetidos a TCTH alogênico ou apresentavam leucemia aguda recidivante) e no recebimento prévio de profilaxia antifúngica. A porcentagem de pacientes na categoria de alto risco no início do estudo foi de 26,6% no grupo que recebeu Acetato de Caspofungina (substância ativa) e de 22,9% entre aqueles que foram tratados com anfotericina B lipossomal injetável.
Uma porcentagem similar de pacientes nos dois grupos recebeu profilaxia antifúngica. Os diagnósticos mais frequentes foram leucemia mielogênica aguda, leucemia linfocítica aguda e linfoma não Hodgkin.
Os pacientes que se enquadraram nos critérios de inclusão do estudo e receberam pelo menos uma dose do tratamento foram incluídos na população de intenção de tratamento modificada (ITM) (556 tratados com Acetato de Caspofungina (substância ativa) e 539 tratados com anfotericina B lipossomal injetável). Uma resposta global favorável requeria cada um dos 5 critérios:
- Tratamento bem-sucedido de qualquer infecção fúngica presente no período basal;
- Ausência de novas infecções fúngicas manifestadas durante a administração da medicação de estudo ou até 7 dias após a conclusão do tratamento;
- Sobrevida durante 7 dias após a conclusão da medicação de estudo;
- Desaparecimento da febre durante o período de neutropenia.
Um comitê independente de especialistas analisou os dados cegos de todos os pacientes com suspeita de infecção fúngica invasiva. O comitê avaliou a presença de infecção fúngica invasiva, tempo do início do resultado (período basal ou nova infecção), patógeno responsável e, para infecções no período basal, resposta ao tratamento.
As únicas infecções fúngicas consideradas para a proposta da análise estatística foram aquelas classificadas pelos especialistas como prováveis ou comprovadas. Aproximadamente 5% dos pacientes apresentaram infecções fúngicas no período basal, a maioria causada por espécies de Aspergillus ou de Candida. Os percentuais de pacientes da população de ITM com resposta favorável global e respostas favoráveis aos critérios individuais são demonstrados na Tabela 1.
Tabela 1: Resposta favorável de pacientes com febre persistente e neutropenia:
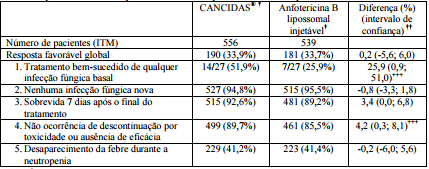 †Acetato de Caspofungina (substância ativa): 70 mg no 1º dia, seguidos de 50 mg diariamente durante o restante do tratamento (dose aumentada para 70 mg para 73 pacientes); anfotericina B lipossomal: 3,0 mg/kg/dia (dose aumentada para 5,0 mg/kg/dia para 74 pacientes).
†Acetato de Caspofungina (substância ativa): 70 mg no 1º dia, seguidos de 50 mg diariamente durante o restante do tratamento (dose aumentada para 70 mg para 73 pacientes); anfotericina B lipossomal: 3,0 mg/kg/dia (dose aumentada para 5,0 mg/kg/dia para 74 pacientes).
†† Resposta global: diferença percentual estimada ajustada por estrato e expressa como Acetato de Caspofungina (substância ativa) – anfotericina B lipossomal injetável (IC 95,2%). Critérios individuais: diferença percentual calculada como Acetato de Caspofungina (substância ativa) – anfotericina B lipossomal injetável (IC 95%).
†††Diferença estatisticamente significativa.
Com base nas taxas de resposta favorável global, Acetato de Caspofungina (substância ativa) foi tão eficaz quanto a anfotericina B lipossomal injetável no tratamento empírico da neutropenia febril persistente. Acetato de Caspofungina (substância ativa) apresentou taxas significativamente maiores que a anfotericina B lipossomal injetável para os seguintes critérios: tratamento bem-sucedido de qualquer infecção fúngica presente no período basal (Acetato de Caspofungina (substância ativa), 51,9%; anfotericina B lipossomal injetável, 25,9%) e inexistência de descontinuação prematura da medicação em estudo por toxicidade ou ausência de eficácia (Acetato de Caspofungina (substância ativa), 89,7%; anfotericina B lipossomal injetável, 85,5%). Acetato de Caspofungina (substância ativa) foi comparável à anfotericina B lipossomal injetável em outros critérios (ausência de infecções fúngicas manifestadas durante a administração da medicação de estudo ou até 7 dias e após a conclusão do tratamento e desaparecimento da febre durante o período de neutropenia).
A taxa de resposta favorável global foi comparável em pacientes de alto risco (Acetato de Caspofungina (substância ativa), 43,2%; anfotericina B lipossomal injetável, 37,7%) e de baixo risco (Acetato de Caspofungina (substância ativa), 31,0%; anfotericina B lipossomal injetável, 32,4%). As taxas também foram comparáveis em pacientes que receberam profilaxia antifúngica prévia (Acetato de Caspofungina (substância ativa), 33,5%; anfotericina B lipossomal injetável, 32,9%) e naqueles que não receberam profilaxia antifúngica prévia (Acetato de Caspofungina (substância ativa), 35,0%; anfotericina B lipossomal injetável, 34,5%).
A maioria das infecções do período basal foi causada por espécies de Aspergillus ou de Candida. As taxas de resposta a Acetato de Caspofungina (substância ativa) e à anfotericina B lipossomal injetável para infecções no período basal causadas por espécies de Aspergillus foram de 41,7% (5/12) e 8,3% (1/12), respectivamente; para infecções do período basal causadas por espécies de Candida, essas taxas foram de 66,7% (8/12) e 41,7% (5/12) para Acetato de Caspofungina (substância ativa) e anfotericina B lipossomal injetável, respectivamente.
Candidíase invasiva
Em um estudo duplo-cego, randômico e de fase III, pacientes com diagnóstico comprovado de candidíase invasiva receberam doses diárias de Acetato de Caspofungina (substância ativa) (50 mg/dia após uma dose de ataque de 70 mg no 1º dia) ou de anfotericina B deoxicolato (0,6 a 0,7 mg/kg/dia para pacientes não neutropênicos e 0,7 a 1,0 mg/kg/dia para pacientes neutropênicos); os pacientes foram estratificados tanto pelo status neutropênico como pela escala APACHE II.
Os pacientes que atendiam aos critérios de inclusão e receberam uma ou mais doses de terapia IV do estudo foram incluídos na análise primária (intenção de tratamento modificada [ITM]) de resposta no fim da terapia IV do estudo. Uma análise pré-definida para sustentar a ITM – análise dos pacientes avaliáveis – incluiu pacientes que atendiam aos critérios de inclusão e que receberam terapia IV do estudo durante 5 dias ou mais e que tiveram avaliação completa de eficácia no final da terapia IV do estudo. Uma resposta favorável requereu tanto a resolução do sintoma como o desaparecimento da infecção por Candida.
Dos 239 pacientes envolvidos, 224 (109 tratados com Acetato de Caspofungina (substância ativa) e 115 tratados com anfotericina B) atenderam aos critérios de inclusão da análise ITM; destes, 185 (88 tratados com Acetato de Caspofungina (substância ativa) e 97 tratados com anfotericina B) atendiam aos critérios de inclusão na análise de pacientes avaliáveis. Os diagnósticos mais frequentes foram infecções da corrente sanguínea (candidemia) (83%) e peritonite por Candida (10%). A maioria das infecções foi causada por C. albicans (45%) e, secundariamente, por C. parapsilosis (19%), C. tropicalis (16%), C. glabrata (11%) e C. krusei (2%). As taxas de resposta favorável no fim da terapia IV do estudo encontram-se descritas na Tabela 2.
Tabela 2: Taxas de resposta favorável à terapia IV do estudo entre pacientes com candidíase invasiva:
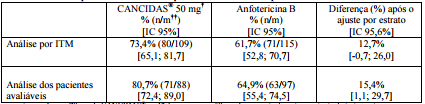 † Os pacientes receberam 70 mg de Acetato de Caspofungina (substância ativa) no 1º dia e, a seguir, 50 mg diariamente durante o restante do tratamento.
† Os pacientes receberam 70 mg de Acetato de Caspofungina (substância ativa) no 1º dia e, a seguir, 50 mg diariamente durante o restante do tratamento.
†† Número de pacientes com resposta favorável no fim da terapia IV do estudo/número de pacientes incluídos na análise.
Em pacientes neutropênicos, as taxas de resposta favorável no final da terapia IV do estudo nos grupos tratados com Acetato de Caspofungina (substância ativa) e anfotericina B foram comparáveis: 50% (7/14) no grupo de Acetato de Caspofungina (substância ativa) e 40% (4/10) no grupo que recebeu anfotericina B. Em pacientes com classificação alta (> 20) na escala APACHE II no início do estudo, as taxas de resposta favorável no grupo de Acetato de Caspofungina (substância ativa) e no grupo tratado com anfotericina B foram semelhantes: 57,1% (12/21) no grupo de Acetato de Caspofungina (substância ativa) e 43,5% (10/23) no grupo tratado com anfotericina B.
As taxas de respostas foram também consistentes entre todas as espécies de Candida. Para todos os outros pontos de tempo (10º dia da terapia IV, fim de todas as terapias antifúngicas, 2ª semana de acompanhamento monitorado pós-terapia e 6ª a 8ª semana de acompanhamento pós-terapia), Acetato de Caspofungina (substância ativa) foi tão eficaz quanto a anfotericina B. Acetato de Caspofungina (substância ativa) foi também comparável à anfotericina B no que se refere à recidiva ou taxa de sobrevivência.
Acetato de Caspofungina (substância ativa) foi comparável à anfotericina B no tratamento de candidíase invasiva no fim da terapia IV do estudo na análise primária de eficácia (ITM). Em uma análise de eficácia pré-definida de pacientes avaliáveis para manter a ITM, Acetato de Caspofungina (substância ativa) foi estatisticamente superior à anfotericina B no fim do estudo da terapia IV.
Candidemia
Dos 224 pacientes do estudo de candidíase invasiva, aqueles que se enquadraram nos critérios de inclusão da análise por ITM – 186 (92 tratados com Acetato de Caspofungina (substância ativa) e 94 tratados com anfotericina B) – apresentaram candidemia. Destes, 150 (71 tratados com Acetato de Caspofungina (substância ativa) e 79 tratados com anfotericina B) atenderam aos critérios de inclusão da análise de pacientes avaliáveis. As taxas de resposta favorável no fim da terapia IV do estudo para pacientes com candidemia são relacionadas na Tabela 3.
Tabela 3: Taxa de resposta favorável à terapia IV do estudo entre pacientes com candidemia:
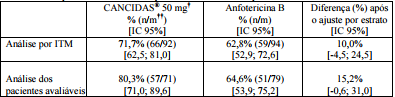 † Os pacientes receberam 70 mg de Acetato de Caspofungina (substância ativa) no 1º dia e, a seguir, 50 mg diariamente (reforço) durante o restante do tratamento. †† Número de pacientes com taxa de resposta favorável no fim da terapia IV do estudo/número de pacientes incluídos na análise.
† Os pacientes receberam 70 mg de Acetato de Caspofungina (substância ativa) no 1º dia e, a seguir, 50 mg diariamente (reforço) durante o restante do tratamento. †† Número de pacientes com taxa de resposta favorável no fim da terapia IV do estudo/número de pacientes incluídos na análise.
Tanto na ITM como na análise de eficácia dos pacientes avaliáveis, Acetato de Caspofungina (substância ativa) foi comparável à anfotericina B no tratamento de candidemia no fim da terapia IV do estudo.
Candidíase esofágica
Foram conduzidos três estudos comparativos para avaliar a eficácia de Acetato de Caspofungina (substância ativa) no tratamento de candidíase esofágica. Um estudo comparou Acetato de Caspofungina (substância ativa) com fluconazol IV, enquanto dois estudos de determinação de dose compararam diferentes doses de Acetato de Caspofungina (substância ativa) com anfotericina B. Nesses três estudos, foi admitido um total de 393 pacientes com candidíase esofágica (Acetato de Caspofungina (substância ativa), n = 222; fluconazol, n = 94; anfotericina B, n = 77). Em todos os três, os pacientes admitidos apresentavam sintomas e documentação microbiológica de candidíase esofágica e muitos deles apresentavam AIDS avançada (contagem de CD4 < 50/mm3). A gravidade da doença foi determinada por esofagoscopia (endoscopia).
Em um estudo randômico e duplo-cego que comparou 50 mg/dia de Acetato de Caspofungina (substância ativa) com 200 mg/dia de fluconazol IV para o tratamento de candidíase esofágica, os pacientes foram tratados durante 7 a 21 dias. Uma resposta global favorável exigiu completa resolução dos sintomas e melhora significativa da endoscopia 5 a 7 dias após a descontinuação do tratamento. A definição da resposta endoscópica foi baseada na gravidade da doença no período basal, a qual foi avaliada utilizando-se uma escala de 4 graus, e exigiu redução de, no mínimo, 2 graus em relação ao escore da endoscopia do período basal ou redução ao grau 0 para pacientes com escore de 2 ou menos no período basal. A proporção de pacientes tratados com Acetato de Caspofungina (substância ativa) e fluconazol que apresentaram resposta global, sintomática e endoscópica favorável foi comparável: 81,5% e 85,1%, respectivamente, para resposta global favorável; 90,1% e 89,4% para resposta sintomática favorável; 85,2% e 86,2% para resposta endoscópica favorável.
Dois estudos duplos-cegos de determinação de dose avaliaram 3 diferentes doses de Acetato de Caspofungina (substância ativa) (35 mg, 50 mg, 70 mg/dia) com anfotericina B (0,5 mg/kg/dia). A proporção de pacientes com resposta global favorável no grupo que recebeu 50 mg/dia de Acetato de Caspofungina (substância ativa) foi de 34/46 (73,9%) no estudo 1 e de 18/20 (90,0%) no estudo 2; a proporção de pacientes com resposta global favorável no grupo que recebeu anfotericina B foi de 34/54 (63,0%) no estudo 1 e de 14/23 (60,9%) no estudo 2. Doses de Acetato de Caspofungina (substância ativa) maiores que 50 mg/dia não proporcionaram benefício adicional no tratamento de candidíase esofágica.
Candidíase orofaríngea
Evidências que embasam a eficácia de Acetato de Caspofungina (substância ativa) para o tratamento de candidíase orofaríngea foram derivadas de dois grupos de pacientes admitidos nos 3 estudos comparativos descritos acima. Os pacientes incluídos no primeiro grupo, provenientes desses estudos comparativos, apresentavam tanto doença orofaríngea como esofágica (n = 173), enquanto aqueles incluídos no segundo grupo apresentavam somente doença orofaríngea (n = 52). Uma resposta favorável foi definida como resolução completa de todos os sintomas da doença orofaríngea e de todas as lesões orofaringeanas visíveis.
Dos 52 pacientes que apresentavam somente doença orofaríngea e foram tratados durante 7 a 10 dias, 14 receberam Acetato de Caspofungina (substância ativa) na dose recomendada de 50 mg/dia. A taxa de resposta favorável foi de 92,9% (13/14) para Acetato de Caspofungina (substância ativa) e de 66,7% (8/12) para a anfotericina B (0,5 mg/kg/dia).
Os resultados dos pacientes tanto com doença orofaríngea como esofágica fornecem evidências adicionais de que Acetato de Caspofungina (substância ativa) (50 mg/dia; n = 67) é eficaz para o tratamento de candidíase orofaríngea, com resultados comparáveis aos obtidos com anfotericina B ou fluconazol. Doses maiores que 50 mg/dia de Acetato de Caspofungina (substância ativa) não proporcionaram benefícios adicionais na candidíase orofaríngea.
Aspergilose invasiva
Sessenta e nove pacientes com 18 a 80 anos de idade com aspergilose invasiva foram admitidos em um estudo não comparativo e aberto para avaliar a segurança, a tolerabilidade e a eficácia de Acetato de Caspofungina (substância ativa); os pacientes admitidos eram refratários ou intolerantes a outro(s) tratamento(s) antifúngico(s).
Foram classificados como refratários os pacientes que apresentaram progressão da doença ou que não apresentaram melhora apesar do tratamento durante 7 dias ou mais com anfotericina B, formulações lipídicas de anfotericina B, itraconazol ou um azol sob pesquisa com atividade relatada contra Aspergillus. A intolerância ao tratamento anterior foi definida como duplicação dos níveis de creatinina (ou creatinina de 2,5 mg/dL ou mais durante o tratamento), outras reações agudas ou toxicidade relacionada à infusão.
Para serem incluídos no estudo, os pacientes com doença pulmonar deveriam ter apresentado aspergilose invasiva classificada como definida (histopatologia ou cultura de tecido positivas obtidas por meio de procedimento invasivo) ou provável (evidência positiva no exame radiológico ou na tomografia computadorizada, confirmada por cultura do lavado broncoalveolar ou do escarro, ensaio imunoabsorvente ligado à enzima de galactomanana e/ou reação em cadeia da polimerase) e os pacientes com doença extrapulmonar deveriam apresentar aspergilose invasiva definida; as definições foram elaboradas de acordo com os Critérios do Grupo de Estudo de Micoses.
Os pacientes receberam uma dose única de ataque de 70 mg de Acetato de Caspofungina (substância ativa) e, subsequentemente, uma dose de 50 mg diariamente. A duração média do tratamento foi de 33,7 dias, com variação de 1 a 162 dias.
Um comitê independente de especialistas avaliou os dados dos pacientes, inclusive o diagnóstico de aspergilose invasiva, a resposta e a tolerabilidade ao tratamento antifúngico anterior, o curso do tratamento com Acetato de Caspofungina (substância ativa) e o resultado clínico.
Uma resposta favorável foi definida como o desaparecimento completo (resposta completa) ou a melhora clinicamente significativa (resposta parcial) de todos os sinais, sintomas e achados radiográficos atribuíveis. Doença estável e não progressiva foi considerada uma resposta desfavorável.
Entre os 69 pacientes admitidos no estudo, 63 atenderam aos critérios diagnósticos de admissão e apresentavam dados de resultados e, destes, 52 receberam tratamento durante mais de 7 dias; 53 (84%) eram refratários e 10 (16%) apresentavam intolerância ao tratamento antifúngico prévio; 45 apresentavam doença pulmonar e 18, doença extrapulmonar. As afecções subjacentes foram neoplasia hematológica (n = 24), transplante alogênico de medula óssea ou transplante de células-tronco (n = 18), transplante de órgãos (n = 8), tumor sólido (n = 3) ou outras afecções (n = 10); todos os pacientes admitidos no estudo receberam tratamento concomitante para as afecções subjacentes. Dezoito pacientes receberam tacrolimo e Acetato de Caspofungina (substância ativa) concomitantemente, dentre os quais 8 receberam também micofenolato mofetil.
No geral, o comitê de especialistas determinou que 41% (26/63) dos pacientes que receberam no mínimo uma dose de Acetato de Caspofungina (substância ativa) apresentaram resposta favorável. Entre os pacientes que receberam Acetato de Caspofungina (substância ativa) por um período superior a 7 dias, 50% (26/52) apresentaram resposta favorável. As taxas de resposta favorável para os pacientes refratários ou intolerantes aos tratamentos prévios foram de 36% (19/53) e de 70% (7/10), respectivamente. As taxas de resposta entre os pacientes com doença pulmonar e doença extrapulmonar foram de 47% (21/45) e de 28% (5/18), respectivamente.
Entre os pacientes com doença extrapulmonar, 2 de 8 pacientes que também tiveram envolvimento de SNC definido, provável ou possível, apresentaram resposta favorável. Também foi feita revisão dos prontuários médicos de 206 pacientes com aspergilose invasiva para avaliar a resposta aos tratamentos convencionais (não os de pesquisa). As características dos pacientes e os fatores de risco importantes nessa revisão foram similares aos dos pacientes admitidos no estudo não comparativo aberto (veja acima) e foram usadas as mesmas definições rigorosas para o diagnóstico e os resultados.
Para inclusão nesse estudo, os pacientes deveriam ter apresentado aspergilose invasiva e recebido no mínimo 7 dias de tratamento antifúngico convencional. A taxa de resposta favorável desse estudo de controle histórico foi de 17% (35/206) para o tratamento convencional em comparação com a taxa de resposta favorável de 41% (26/63) obtida para Acetato de Caspofungina (substância ativa) no estudo não comparativo aberto.
Os resultados de análises multivariadas demonstraram relação de probabilidade de mais de 3 para Acetato de Caspofungina (substância ativa), com um intervalo de confiança de 95% excluindo 1, sugerindo benefício do tratamento com Acetato de Caspofungina (substância ativa).
Pacientes pediátricos
A segurança e a eficácia de Acetato de Caspofungina (substância ativa) foram avaliadas em pacientes pediátricos de 3 meses a 17 anos de idade em dois estudos clínicos multicêntricos prospectivos.
O primeiro estudo, que incluiu 82 pacientes com idade entre 2 e 17 anos, foi randômico, duplo-cego e comparou Acetato de Caspofungina (substância ativa) (50 mg/m2 IV uma vez ao dia após uma dose inicial de 70 mg/m2 no 1º dia [sem exceder 70 mg/dia]) à anfotericina B lipossomal (3 mg/kg/dia IV) em uma proporção de tratamento de 2:1 (56 com caspofungina, 26 com anfotericina B lipossomal) como tratamento empírico em pacientes pediátricos com febre persistente e neutropenia. O desenho do estudo e os critérios para determinação da eficácia foram similares aos do estudo em pacientes adultos.
Os pacientes foram estratificados com base na categoria de risco (pacientes de alto risco foram submetidos a transplante alogênico de células-tronco ou apresentaram recidiva de leucemia aguda). Vinte e sete por cento dos pacientes de ambos os grupos de tratamento eram de alto risco. As taxas de sucesso global nos resultados da análise MITT, ajustadas pelos estratos de alto risco, foram as seguintes: 41,3% (23/56) para Acetato de Caspofungina (substância ativa) e 28,1% (7/25) para anfotericina B lipossomal. Para os pacientes da categoria de alto risco, a taxa de resposta global favorável foi de 60% (9/15) no grupo Acetato de Caspofungina (substância ativa) e 0% (0/7) no grupo que recebeu anfotericina B lipossomal.
O segundo estudo foi prospectivo, aberto, não comparativo, para avaliar a segurança e a eficácia da caspofungina em pacientes pediátricos (3 meses a 17 anos de idade) com candidíase invasiva, candidíase esofágica e aspergilose invasiva (como terapia de resgate).
O estudo empregou critérios diagnósticos baseados nos critérios EORTC/MSG estabelecidos de infecção comprovada ou provável; esses critérios foram similares aos empregados nos estudos em adultos para essas várias indicações. Similarmente, os pontos de tempo de eficácia e os endpoints utilizados nesse estudo foram semelhantes aos empregados nos estudos correspondentes em adultos. Todos os pacientes receberam Acetato de Caspofungina (substância ativa) a 50 mg/m2 IV uma vez ao dia após uma dose de ataque de 70 mg/m2 no 1º dia (sem exceder 70 mg diariamente). Entre os 49 pacientes admitidos que receberam Acetato de Caspofungina (substância ativa), 48 foram incluídos na análise MITT. Desses 48 pacientes, 37 tinham candidíase invasiva, 10 tinham aspergilose invasiva e 1 paciente tinha candidíase esofágica. De acordo com cada indicação, a taxa de resposta favorável ao final do tratamento com caspofungina na análise MITT foi 81% (30/37) em candidíase invasiva, 50% (5/10) em aspergilose invasiva e 100% (1/1) em candidíase esofágica.
Características Farmacológicas
Mecanismo de ação
O acetato de caspofungina, ingrediente ativo de Acetato de Caspofungina (substância ativa), inibe a síntese do ?(1,3)-D-glucana, um componente essencial da parede celular de muitos fungos filamentosos e leveduras que não faz parte das células dos mamíferos.
Farmacocinética
Farmacodinâmica
Cuidados de Armazenamento
Conservar sob refrigeração (entre 2 e 8°C).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido Guarde-o em sua embalagem original.
Após preparo, os frascos reconstituídos podem ser mantidos em temperatura até 25ºC por até 24 horas antes da preparação da solução para infusão.
A solução final para infusão intravenosa deve ser usada em 24 horas se for mantida em temperatura até 25ºC ou em 48 horas se mantida sob refrigeração entre 2°C e 8°C.
Aparência:
Cancidas é um pó de cor branca a esbranquiçada.
Antes de usar, observe o aspecto do medicamento Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Uso restrito a hospitais.
Venda sob prescrição médica.
MS 1.0029.0033
Farm. Resp.:
Fernando C. Lemos – CRF-SP nº 16.243
Registrado e importado por:
Merck Sharp & Dohme Farmacêutica Ltda.
Rua 13 de Maio, 815 – Sousas, Campinas/SP
CNPJ: 45.987.013/0001-34 – Brasil
MSD On Line 0800-0122232
E-mail: [email protected]
www.msdonline.com.br
Fabricado por:
Laboratoires Merck Sharp & Dohme - Chibret
Clermont Ferrand, França
informações complementares
| Fabricante |
| MERCK S/A |
| Princípio ativo |
| Acetato De Caspofungina |
| Categoria do medicamento |
| Medicamentos Especiais |
