- Home
- Medicamentos
- Medicamentos Especiais
- Evotaxel - 6Mg/Ml Solução Inje...
- Bula de Evotaxel - 6Mg/Ml Solução Inje...
para o que é indicado e para que serve?
Paclitaxel é uma substância que possui atividade antitumoral.Continue lendo...
ofertas de Evotaxel - 6Mg/Ml Solução Injetável 100Mg Em 16,7 Ml

ATENÇÃO: O texto abaixo deve ser utilizado apenas como uma referência secundária. É um registro histórico da bula, rótulo ou manual do produto. Este texto não pode substituir a leitura das informações que acompanha o produto, cujo fabricante podem mudar a formulação, recomendação, modo de uso e alertas legais sem que sejamos previamente comunicados. Apenas as informações contidas na própria bula, rótulo ou manual que acompanha o produto é que devem estar atualizadas de acordo com a versão comercializada porém, no caso de qualquer dúvida, consulte o serviço de atendimento ao consumidor do produto ou nossa equipe.
Para que serve
é eficaz na redução da pressão intra-ocular e está indicado para o tratamento da hipertensão ocular e glaucoma crônico de ângulo aberto. Pode ser usado isolado ou em combinação com outras drogas antiglaucomatosas.
Contraindicação
Hipersensibilidade ao componente da fórmula. Bradicardia sinusal, maior do que o bloqueio atrioventricular de primeiro grau, choque cardiogênico ou pacientes com insuficiência cardíaca comprovada.
Como usar
A dose recomendada é uma ou duas gotas no(s) olho(s) afetado(s) duas vezes por dia. Como acontece ao se administrar uma medicação nova, recomenda-se o acompanhamento cuidadoso dos pacientes. Se a pressão intra-ocular do paciente não estiver adequadamente controlada com este tratamento, pode-se instituir terapêutica concomitante com pilocarpina , outros mióticos, epinefrina ou inibidores da anidrase carbônica.
Precauções
O paclitaxel (substância ativa) deve ser administrado sob a supervisão de um médico com experiência na utilização de agentes quimioterápicos.
O paclitaxel (substância ativa) deve ser administrado como infusão após diluição. Os pacientes devem ser tratados com corticosteroides, anti-histamínicos e antagonistas H2 antes da administração de paclitaxel (substância ativa).
O paclitaxel (substância ativa) deverá ser administrado antes do composto de platina quando este for dado em combinação com um composto de platina.
Anafilaxia e Reações Graves de Hipersensibilidade
Anafilaxia e reações graves de hipersensibilidade ocorreram comumente em pacientes recebendo paclitaxel (substância ativa). São Caracterizadas por dispneia requerendo broncodilatadores, hipotensão necessitando de tratamento, angioedema ou urticária generalizada.
Estas reações são provavelmente mediadas por histamina. Raras reações fatais ocorreram em alguns pacientes, apesar do pré-tratamento. Todos os pacientes devem ser pré-tratados com corticosteroides, difenidramina e antagonistas H2. Em caso de reação de hipersensibilidade grave, a infusão de paclitaxel (substância ativa) deve ser descontinuada imediatamente e o paciente não deve ser submetido a novas infusões de paclitaxel (substância ativa).
Toxicidade Hematológica
A depressão da medula óssea (principalmente neutropenia) é dependente da dose e do esquema posológico e é a principal toxicidade dose-limitante dentro de um regime.
A monitorização frequente do hemograma deve ser instituída durante o tratamento com paclitaxel (substância ativa). O paclitaxel (substância ativa) não deve ser administrado a pacientes com contagem basal de neutrófilos < 1.500 células/mm (<1.000 células/mm para pacientes com sarcoma de Kaposi).
Em caso de neutropenia grave (< 500 células/mm) durante um ciclo de tratamento com o medicamento, recomenda-se uma redução de 20% da dose em ciclos subsequentes.
Toxicidade Cardiovascular
Foram observados casos de hipotensão, hipertensão e bradicardia durante a administração de paclitaxel (substância ativa). Os pacientes geralmente permanecem assintomáticos e não requerem tratamento. Em casos graves, pode ser necessária a interrupção ou a descontinuação das infusões de paclitaxel (substância ativa) a critério médico. Recomenda-se a monitorização frequente dos sinais vitais, particularmente durante a primeira hora de infusão de paclitaxel (substância ativa).
A monitorização eletrocardiográfica contínua não é necessária, exceto para os pacientes com distúrbios sérios de condução. Quando paclitaxel (substância ativa) for utilizado em combinação com trastuzumabe ou doxorrubicina para tratamento de câncer de mama metastático, é recomendado monitoramento da função cardíaca.
Sistema Nervoso
A ocorrência de neuropatia periférica é frequente, mas normalmente não é grave. Recomenda-se uma redução da dose de 20% nos ciclos subsequentes de paclitaxel (substância ativa) nos casos de neuropatia grave.
paclitaxel (substância ativa) contém álcool desidratado.
Devem ser considerados os possíveis efeitos do etanol no SNC e seus outros efeitos, em todos os pacientes. Crianças podem ser mais sensíveis aos efeitos do etanol que os adultos.
Reação no local da injeção
Até o momento, se desconhece um tratamento específico para as reações devidas ao extravasamento. Dada a possibilidade de extravasamento, é aconselhável monitorar rigorosamente o local da infusão quanto a uma possível infiltração durante a administração da droga.
Uso pediátrico
A segurança e a eficácia de paclitaxel (substância ativa) em pacientes pediátricos não foram estabelecidas. Relataram-se casos de toxicidade do sistema nervoso central (SNC) (raramente associada à morte) em um estudo clínico em pacientes pediátricos nos quais se administrou paclitaxel (substância ativa) por infusão intravenosa durante 3 horas com doses entre 350 mg/m e 420 mg/m . A toxicidade é provavelmente devida à alta dose de etanol, veículo constituinte do paclitaxel (substância ativa), administrado em um curto período de infusão.
O uso concomitante de anti-histamínicos pode intensificar este efeito.
Embora um efeito direto do paclitaxel (substância ativa) não possa ser descartado, as altas doses utilizadas neste estudo (duas vezes acima da dose recomendada para adultos) devem ser consideradas na avaliação da segurança de paclitaxel (substância ativa) para uso nesta população.
Uso Geriátrico
Dos 2228 pacientes que receberam paclitaxel (substância ativa) em oito estudos clínicos que avaliaram sua segurança e eficácia no tratamento de câncer de ovário avançado, carcinoma de mama ou câncer de não pequenas células do pulmão, e 1570 pacientes que foram randomizados para receber paclitaxel (substância ativa) em um estudo de câncer adjuvante de mama, 649 pacientes (17%) tinham 65 anos ou mais, incluindo 49 pacientes (1%) com 75 anos ou mais.
Na maioria dos estudos, a mielossupressão grave foi mais frequente em pacientes idosos; em alguns estudos, neuropatia grave foi mais comum.
Em dois estudos clínicos em câncer de não-pequenas células de pulmão, os pacientes idosos tratados com paclitaxel (substância ativa) apresentaram uma maior incidência de eventos cardiovasculares. A avaliação de eficácia pareceu similar em pacientes idosos e jovens; entretanto, a eficácia comparativa não pôde ser determinada com confiança devido ao pequeno número de pacientes idosos estudados.
Em um estudo de tratamento de primeira linha de câncer de ovário, pacientes idosos apresentaram menor sobrevida mediana que pacientes jovens, mas nenhum outro parâmetro de eficácia favoreceu o grupo jovem.
Insuficiência Hepática
Pacientes com insuficiência hepática podem apresentar risco de toxicidade aumentado, particularmente mielossupressão graus III-IV. O ajuste de dose é recomendado. Os pacientes devem ser bem monitorados quanto ao desenvolvimento de mielossupressão profunda.
Carcinogênese, Mutagênese, Comprometimento da Fertilidade
O potencial carcinogênico do produto não foi estudado. Demonstrou-se que paclitaxel (substância ativa) é clastogênico in vitro (aberrações cromossômicas em linfócitos humanos) e in vivo (teste de micronúcleo em camundongos). paclitaxel (substância ativa) não foi mutagênico no teste de AMES ou no teste de mutação genética CHO/HGPRT. Ocorreu redução da fertilidade e do número de implantações e fetos vivos em ratos que receberam paclitaxel (substância ativa).
O produto mostrou-se embriotóxico e fetotóxico em coelhos que receberam a droga durante a organogênese.
Gravidez
paclitaxel (substância ativa) poderá causar danos fetais quando administrado a mulheres grávidas. O fármaco mostrou ser embriotóxico e fetotóxico em coelhos, além de diminuir a fertilidade em ratos. Não existem estudos em mulheres grávidas.
Mulheres em idade reprodutiva devem evitar a gravidez durante a terapia com). Se paclitaxel (substância ativa) for utilizado durante a gestação ou se a paciente ficar grávida enquanto em tratamento com a droga, a paciente deverá ser informada sobre os perigos potenciais.
Categoria de risco na gravidez: D.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez.
Lactação
Não se sabe se o paclitaxel (substância ativa) é excretado no leite humano. Recomenda-se descontinuar a amamentação enquanto durar a terapia com paclitaxel (substância ativa).
Fertilidade
Dado o potencial mutagênico de paclitaxel (substância ativa), é necessária uma contracepção efetiva para pacientes do sexo masculino e feminino durante o tratamento e até 6 meses após o fim do tratamento. Como paclitaxel (substância ativa) pode diminuir a fertilidade masculina, a preservação do esperma pode ser considerada com o propósito de fecundidade posterior.
Imunizações
O uso concomitante de paclitaxel (substância ativa) com vacina de vírus vivos pode potencializar a replicação do vírus da vacina e/ou pode aumentar a reação adversa do vírus da vacina porque os mecanismos de defesa natural podem ser suprimidos pelo paclitaxel (substância ativa). A vacinação com vacinas de vírus vivos em pacientes recebendo paclitaxel (substância ativa) pode resultar em infecção grave. A resposta dos anticorpos destes pacientes a vacinas pode estar diminuída. O uso de vacinas vivas deve ser evitado e o conselho de um especialista deve ser considerado.
Reações Adversas
A frequência e a gravidade dos eventos adversos são geralmente similares entre os pacientes que receberam paclitaxel para o tratamento de câncer de ovário, mama, não-pequenas células de pulmão ou sarcoma de Kaposi. Entretanto, pacientes com sarcoma de Kaposi relacionado à AIDS podem sofrer com maior frequência e gravidade toxicidade hematológica, infecções e neutropenia febril. Estes pacientes necessitam de uma redução na intensidade da dose e de cuidados de suporte.
Análise Agrupada dos Eventos Adversos Ocorridos em Estudos com o Agente Único
Outros Eventos Clínicos
A alopecia foi observada em quase todos os pacientes (87%).
Foram observadas alterações transitórias na pele resultante da reação de hipersensibilidade relacionadas ao paclitaxel, porém nenhuma outra toxicidade cutânea foi significativamente associada à administração de paclitaxel. Alterações nas unhas (mudanças de pigmentação ou descoloração do leito ungueal) foram incomuns (2%).
Edema foi relatado em 21% dos pacientes (17% deles sem edema basal); somente 1% apresentou edema grave e nenhum paciente necessitou de descontinuação do tratamento. O edema era usualmente focal e relacionado à doença. Observou-se edema em 5% dos ciclos nos pacientes normais e não se registrou aumento com o tempo no estudo.
Anormalidades cutâneas relacionados à radiação assim como relatos de erupção maculopapulosa, prurido, síndrome de Stevens- Johnson, e necrose epidérmica tóxica foram reportados.
Relatos de astenia e mal-estar também foram recebidos como parte da contínua análise de segurança de paclitaxel.
Terapia combinada
Eventos adversos por frequência
A frequência dos eventos adversos listada abaixo é definida usando o seguinte:
- Muito comum (?10%);
- Comum (? 1%, < 10%);
- Incomum (? 0,1%, < 1%);
- Raro (? 0,01%, < 0,1%);
- Muito raro (< 0,01%);
- Não conhecido (não pode ser estimado com base nos dados disponíveis).
Infecções e infestações
Desordens do sangue e do sistema linfático
Desordens do sistema imunológico
Desordens no metabolismo e nutrição
Desordens psiquiátricas
Desordens do sistema nervoso
Desordens nos olhos
Desordens no ouvido e labirinto
Desordens cardíacas
Desordens vasculares
Desordens respiratórias, torácicas e do mediastino
Desordens gastrointestinais
Desordens hepato-biliares:
Desordens do tecido subcutâneo e da pele
Desordens musculo-esqueléticas, nos ossos e tecidos de conexão
Desordens gerais e condições do local da administração
Investigações
Interação Medicamentosa
Cisplatina
Em estudos clínicos combinados, a mielossupressão foi mais acentuada e o clearance do paclitaxel (substância ativa) foi reduzido em cerca de 20% quando se administrou paclitaxel (substância ativa) após a cisplatina, comparativamente a paclitaxel (substância ativa) administrado antes da cisplatina.
Substratos, Indutores, Inibidores do Citocromo P450 2C8 e 3A4
O metabolismo de paclitaxel (substância ativa) é catalisado pelo citocromo P450, isoenzimas CYP2C8 e CYP3A4. Deve-se ter cuidado quando da administração de paclitaxel (substância ativa) concomitantemente com conhecidos substratos, indutores (ex. rifampicina, carbamazepina, fenitoína, enfavirenz, nevirapina) ou inibidores (ex. eritromicina, fluxetina, genfibrozil) do citocromo P450, isoenzimas CYP2C8 e CYP3A4.
Doxorrubicina
Efeitos relacionados a administração sequencial, caracterizados por episódios mais acentuados de neutropenia e estomatite foram observados com o uso combinado de paclitaxel (substância ativa) e doxorrubicina quando se administrou paclitaxel (substância ativa) antes da doxorrubicina e por períodos de infusão mais longos do que os recomendados. Os níveis plasmáticos de doxorrubicina (e de seu metabólito ativo doxorrubicinol) podem aumentar quando paclitaxel (substância ativa) e doxorrubicina são utilizados em combinação. Entretanto, dados de um estudo utilizando doxorrubicina in bolus e infusão de paclitaxel (substância ativa) por 3 horas não mostraram efeitos sequenciais nos padrões de toxicidade.
Outras interações
Há um risco aumentado de doença sistêmica fatal por vacina com o uso concomitante com vacinas vivas. Vacinas vivas não são recomendadas em pacientes imunodeprimidos.
Ação da Substância
Resultados da eficácia
Carcinoma de ovário
Câncer de mama
Câncer de Não-pequenas Células do Pulmão (CNPCP)
Em estudo Fase III, aberto, randomizado e conduzido pelo ECOG, 599 pacientes foram randomizados com paclitaxel (T) na dosagem de 135 mg/m2 com infusão de 24 horas em combinação com cisplatina (c) 75 mg/m2, com paclitaxel (T) na dosagem de 250 mg/m2 com infusão de 24 horas em combinação com cisplatina (c) 75 mg/m2 com suporte G-CSF, ou cisplatina (c) 75 mg/m2 no dia 1, seguido por etoposídeo (VP) 100 mg/m2 nos dias 1, 2, e 3 (controle).
As taxas de resposta, o tempo mediano para progressão, a sobrevida mediana e as taxas de 1 ano de sobrevida estão descritos na tabela a seguir. Os valores de p fornecidos não foram ajustados para múltiplas comparações. Houve diferenças estatisticamente significativas a favor de cada um dos braços de paclitaxel + cisplatina, para a taxa de resposta e tempo de progressão da doença.
Não houve diferenças estatisticamente significativas na sobrevida entre o braço paclitaxel + cisplatina e o braço cisplatina + etoposídeo.
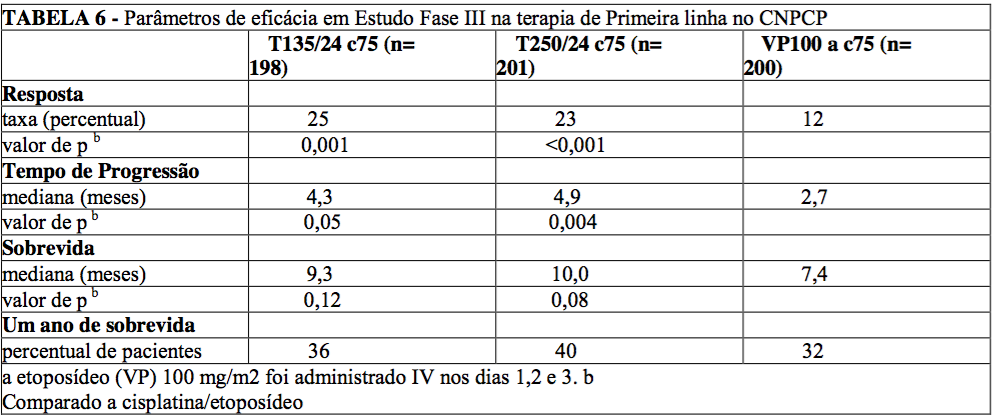
No estudo ECOG, o questionário da Avaliação Funcional da Terapia de Câncer do Pulmão (FACT-L) teve sete sub- escalas que mediram a avaliação subjetiva do tratamento. Das sete, a sub-escala dos sintomas específicos do câncer de pulmão favoreceu o braço paclitaxel 135 mg/m2 (24 horas) + cisplatina, comparado ao braço cisplatina + etoposídeo. Para todos os outros fatores, não houve diferença entre os grupos de tratamento.
O perfil dos eventos adversos dos pacientes que receberam paclitaxel em combinação com cisplatina no estudo em geral foi consistente com o perfil observado na análise de dados dos 812 pacientes tratados apenas com paclitaxel, em 10 estudos clínicos realizados.
Sarcoma de Kaposi Relacionado à AIDS
Dados de dois estudos abertos FASE II suportam o uso de paclitaxel como segunda linha de tratamento em pacientes com sarcoma de Kaposi Relacionado à AIDS. Cinquenta e nove dos 85 pacientes envolvidos nestes estudos receberam previamente terapia sistêmica, incluindo Interferon Alfa (32%), DaunoXome (31%), DOXIL(2%) e quimioterapia com doxorrubicina ( 42%), sendo que 64 % haviam recebido medicamentos da classe das antraciclinas. Oitenta e cinco por cento dos pacientes pré-tratados progrediram ou não toleraram a terapia sistêmica prévia.
No estudo CA 139-174, os pacientes receberam paclitaxel 135 mg/m2 com infusão de 3 horas a cada 3 semanas (intensidade da dose pretendida 45 mg/m /semana). Os pacientes receberam 155 mg/m2 e 175 mg/m2 em ciclos subsequentes, caso nenhuma toxicidade dose limitante fosse observada.
Fatores de crescimento hematopoiético não foram utilizados inicialmente. No estudo CA 139-281 os pacientes receberam paclitaxel 100 mg/m2 com infusão de 3 horas a cada 2 semanas (intensidade da dose pretendida 50 mg/m /semana). Neste estudo os pacientes poderiam receber suporte hematopoiético antes de iniciar a terapia com paclitaxel, ou este suporte poderia ser iniciado como indicado; a dose de paclitaxel não foi aumentada. A intensidade da dose de paclitaxel utilizado nesta população foi menor do que a intensidade da dose recomendada para outros tumores sólidos.
Todos os pacientes apresentavam doenças disseminadas e de baixo risco. Aplicando os critérios da escala (ACTG) para os pacientes submetidos à terapia sistêmica prévia, 93 % eram de baixo risco em relação à extensão da doença (T1), 88 % com a contagem de CD4 <200 células/mm3 (I1) e considerando respectivas doenças sistêmicas 97 % apresentavam baixo risco (S1).
Todos os pacientes no estudo CA 139-174 apresentavam um status do desempenho Karnofsky de 80 ou 90 no valor basal; no estudo CA 139-281, havia 26 (46%) pacientes com um status do desempenho Karnofsky de 70 ou pior no valor basal.
| TABELA 7 - Extensão da Doença no Início do Estudo -Percentual de Pacientes | |
| Visceral ±edema ± oral ± cutâneo | Terapia Sistêmica Prévia (n= 59) 42 |
| Edema ou linfonodo ± oral ± cutâneo | 41 |
| Oral ± cutâneo | 10 |
| Somente Cutâneo | 7 |
Embora a intensidade da dose planejada em dois estudos tenha sido ligeiramente diferente (45 mg/m2/semana no estudo CA 139-174 e 50 mg/m2/semana no estudo CA 139-281), a intensidade da dose administrada foi de 38-39 mg/m2/ semana em ambos estudos, com uma variação similar (20-24 a 51-61).
Benefícios Clínicos Adicionais
A maioria dos dados dos pacientes beneficiados foi avaliada retrospectivamente (planos para esta análise não foram incluídos nos protocolos dos estudos). No entanto, as descrições clínicas e fotográficas indicaram benefícios claros em alguns pacientes, incluindo melhora da função pulmonar em pacientes com comprometimento pulmonar, melhora na deambulação, resolução de úlceras e diminuição de necessidade de analgésicos em pacientes com Sarcoma de Kaposi nos pés e melhora de lesões faciais e edema em pacientes com SK na face, extremidades e genitália.
Segurança
O perfil dos eventos adversos apresentados pelos pacientes com AIDS avançada ou de baixo risco de Sarcoma de Kaposi relacionado à AIDS que receberam paclitaxel foi, em geral, semelhante ao observado na análise de dados dos 812 pacientes com tumores sólidos.
Nos pacientes imunossuprimidos, entretanto, é recomendada uma menor intensidade de dose de paclitaxel e terapia de apoio, incluindo fatores de crescimento hematopoiético em pacientes com neutropenia grave. Pacientes com Sarcoma de Kaposi relacionado à AIDS podem apresentar toxicidade hematológica mais severa do que em pacientes com tumores sólidos.
Características Farmacológicas
O paclitaxel possui atividade antitumoral.
Mecanismo de ação
O paclitaxel é um novo agente antimicrotúbulo que promove a agregação dos microtúbulos a partir dos dímeros de tubulina. Ele estabiliza os microtúbulos prevenindo a despolimerização, resultando na inibição da dinâmica normal de reorganização da rede de microtúbulos essencial para as funções celulares. O paclitaxel também induz a formação anormal ou feixe de microtúbulos durante o ciclo celular e múltiplos ásteres de microtúbulos durante a mitose.
Farmacocinética
A farmacocinética do paclitaxel foi avaliada em uma série de doses, até 300 mg/m2, e esquemas de infusão, variando de 3 a 24 horas e demonstrou ser não-linear e saturável com um aumento desproporcionalmente grande dos valores de concentração máxima (Cmáx) e área sob a curva (AUC) com o aumento da dose, acompanhado por uma diminuição aparente, relacionada à dose, do clearance corpóreo total.
Após a administração intravenosa, o paclitaxel mostra um declínio bifásico das concentrações plasmáticas. O declínio rápido inicial representa a distribuição para os compartimentos periféricos e a eliminação da droga. A última fase deve-se, em parte, a um efluxo relativamente lento do paclitaxel do compartimento periférico. Em pacientes tratados com doses de 135 e 175 mg/m2 administrados por infusões de 3 e 24 horas, a meia-vida final média variou de 13,1 a 52,7 horas e o clearance corpóreo total variou de 12,2 a 23,8 L/h/m . O volume médio de distribuição no estado de equilíbrio variou de 198 a 688 L/m , indicando uma distribuição extravascular extensa e/ou ligação do paclitaxel aos tecidos.
A variabilidade na exposição sistêmica do paclitaxel, avaliada pela AUC(o-oo) para ciclos de tratamento sucessivos é mínima; não há evidências de acúmulo do paclitaxel quando administrado em múltiplos ciclos de tratamento.
Distribuição
Em média, 89% da droga encontra-se ligada às proteínas séricas; a presença de cimetidina, ranitidina, dexametasona ou difenidramina não altera a taxa de ligação protéica do paclitaxel.
Metabolismo
Estudos in vitro com microssomos hepáticos humanos e pedaços de tecidos demonstraram que o paclitaxel é metabolizado fundamentalmente ao 6?-hidroxipaclitaxel pelo citocromo P450 isoenzima CYP2C8; e a dois metabólitos menores, o 3-p-hidroxipaclitaxel e o 6?,3'-p-diidroxipaclitaxel pelo CYP3A4. In vitro, o metabolismo do paclitaxel a 6?-hidroxipaclitaxel foi inibido por vários agentes. O efeito da disfunção renal sobre a disposição do paclitaxel não foi estudado.
Excreção
Após administração intravenosa de doses de 15 a 275 mg/m2 de paclitaxel por 1, 6 ou 24 horas de infusão, os valores médios de recuperação urinária cumulativa da droga inalterada variaram de 1,3% a 12,6% da dose. Isto indica um clearance não-renal extenso de paclitaxel. Em 5 pacientes que receberam doses radio marcadas de 225 ou 250 mg/m2 de paclitaxel por infusão de 3 horas, 14% da radioatividade foi recuperada na urina e 71% foi excretada nas fezes em 120 horas. A recuperação total da radioatividade variou de 56% a 101% da dose. O paclitaxel representou uma média de 5% da radioatividade recuperada nas fezes, enquanto que os metabólitos, principalmente o 6?-hidroxipaclitaxel, responderam pelo restante.
Insuficiência Hepática
A disposição e toxicidade da infusão de 3 horas de paclitaxel foi avaliada em 35 pacientes com variados graus de função hepática. Em comparação com os pacientes com bilirrubina normal, a exposição plasmática ao paclitaxel em pacientes com nível de bilirrubina sérica anormal menor ou igual a 2 vezes o limite superior da normalidade (LSN), que receberam 175 mg/m2, foi aumentada, mas não com aumento aparente na frequência ou severidade da toxicidade.
Em cinco pacientes com nível de bilirrubina sérica total maior que 2 vezes LSN, houve uma incidência maior estatisticamente não significativa de mielossupressão grave, mesmo com dose reduzida (110 mg/m2), mas não foi observado aumento na exposição plasmática.
informações complementares
| Fabricante |
| FARMARIN |
| Princípio ativo |
| Paclitaxel |
| Categoria do medicamento |
| Medicamentos Especiais |
EVOTAXEL - 6MG/ML SOLUÇÃO INJETÁVEL 100MG EM 16,7 ML É UM MEDICAMENTO, NÃO USE SEM PRESCRIÇÃO MÉDICA E ORIENTAÇÃO DO FARMACÊUTICO. AO PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
