Comparamos o preço de Angeliq - C 28 Comprimidos, veja o menor preço

R$ 102,29
RReferência
1
ofertasMelhores preços a partir de R$ 102,29 até R$ 102,29
Menor preço
vendido por Drogaria Nova Esperança
R$ 102,29
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
Para que serve
Angeliq é indicado na terapia de reposição hormonal para o tratamento de sintomas do climatério em mulheres na pós-menopausa há mais de um ano, tais como ondas de calor e suor excessivo, distúrbios do sono, comportamento depressivo, nervosismo e sinais de involução da bexiga e dos órgãos genitais.
Angeliq é adequado para mulheres que ainda possuem útero (útero intacto).
Algumas mulheres são mais predispostas do que outras ao desenvolvimento de osteoporose quando atingem idade mais avançada, dependendo de seu histórico clínico e estilo de vida. Se for adequado, você pode ter a prescrição de Angeliq para prevenção de osteoporose.
Informações à paciente:
Antes de iniciar o uso de um medicamento, é importante ler as informações contidas na bula, verificar o prazo de validade, o conteúdo e a integridade da embalagem.
Mantenha a bula do medicamento sempre em mãos para qualquer consulta que se faça necessária. Leia com atenção as informações presentes na bula antes de usar o medicamento, pois ela contém informações sobre os benefícios e os riscos associados ao uso de terapia de reposição hormonal.
Você também encontrará informações sobre o uso adequado do medicamento e sobre a necessidade de consultar o seu médico regularmente.
Converse com o seu médico para obter mais esclarecimentos sobre a ação do medicamento e sua utilização.
Como Angeliq funciona?
Angeliq é apresentado na forma de um comprimido revestido para terapia de reposição hormonal (TRH).
Cada comprimido revestido contém estradiol e um progestógeno (drospirenona), hormônios que deixam de ser produzidos durante o climatério (fase da vida da mulher após a menopausa).
Desta forma, este medicamento repõe os hormônios que o organismo não produz mais. Embora o climatério seja natural, frequentemente causa sintomas relacionados à perda gradual dos hormônios produzidos pelos ovários.
Adicionalmente, essa perda deixa os ossos mais fracos. Em algumas mulheres, este efeito pode ser acentuado e dar origem à osteoporose que, posteriormente pode resultar em fraturas.
Estudos clínicos realizados com medicamentos que promovem reposição hormonal indicam que o tratamento a longo prazo reduz o risco de fraturas ósseas. De acordo com “Women’s Health Questionnaire”, Angeliq promove efeito positivo no bem-estar e na qualidade de vida. As principais melhorias podem ser observadas nos sintomas somáticos, ansiedade e dificuldades cognitivas.
Além disso, estudos clínicos sugerem que, em mulheres após a menopausa (após o último episódio de sangramento), o risco de se ter câncer no intestino grosso (cólon) pode ser reduzido.
O estrogênio (por exemplo, a substância ativa estradiol) evita ou alivia os sintomas desagradáveis do climatério. A adição contínua do progestógeno (por exemplo, a substância ativa drospirenona) evita o espessamento do revestimento do útero (endométrio) e leva à redução (e à subsequente eliminação na maioria das mulheres) de sangramento do tipo menstrual.
Contraindicação
Você não deve tomar Angeliq nas situações descritas a seguir.
Caso apresente qualquer uma destas condições, informe ao seu médico:
- Presença de sangramento vaginal sem explicação;
- Ocorrência ou suspeita de câncer de mama;
- Ocorrência ou suspeita de outras doenças malignas influenciáveis por hormônios sexuais;
- Presença ou antecedente de tumor no fígado (benigno ou maligno);
- Presença de doença grave no fígado;
- Presença ou antecedente de doença renal grave , enquanto os valores laboratoriais para função renal estiverem fora do intervalo considerado normal;
- Histórico de ataque cardíaco (infarto) e/ou derrame recentes;
- Histórico atual ou anterior de trombose (formação de coágulo de sangue) nos vasos sanguíneos das pernas (trombose venosa profunda) ou dos pulmões (embolia pulmonar);
- Alto risco de trombose em veias ou artérias;
- Presença de níveis muito elevados de triglicérides (um tipo especial de gordura no sangue);
- Gravidez ou lactação;
- Hipersensibilidade a qualquer um dos componentes de Angeliq.
Se qualquer uma destas situações ocorrer pela primeira vez enquanto você estiver tomando Angeliq, descontinue o uso do medicamento imediatamente e consulte seu médico.
O medicamento não deve ser utilizado durante a gravidez e a amamentação. Informe ao seu médico se ficar grávida ou começar a amamentar durante o uso deste medicamento.
Angeliq é indicado para mulheres na pós-menopausa há mais de um ano.
Como usar
A cartela de Angeliq contém 28 comprimidos revestidos. Tome um comprimido por dia.
Não importa em que período do dia você toma o comprimido, mas, uma vez escolhido um determinado horário, você deve mantê-lo aproximadamente constante.
Tome o comprimido com líquido, se necessário. A ingestão junto com alimentos não interfere com a ação de Angeliq.
Inicie uma nova cartela no dia seguinte à tomada do último comprimido da cartela anterior. Nunca deixe intervalo entre as cartelas.
A tomada de comprimidos é contínua. Seu médico irá lhe informar sobre a duração do tratamento.
Se você estiver usando TRH pela primeira vez ou se estiver mudando de um medicamento para TRH combinada contínua (onde todos os comprimidos contêm a mesma composição), a tomada de Angeliq pode ser iniciada a qualquer momento.
Se você estiver mudando de uma TRH combinada sequencial (na qual os comprimidos têm composição diferente e geralmente apresentam cores diferenciadas), complete o ciclo atual da terapia antes de iniciar o uso de Angeliq.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Este medicamento não deve ser partido, aberto ou mastigado.?
Posologia para populações especiais
Crianças e adolescentes
Angeliq não é indicado para o uso em crianças e adolescentes.
Pacientes idosas
Não existem dados que sugiram a necessidade de ajuste de dose em pacientes idosas. Informe seu médico se você tem 65 anos ou mais.
Pacientes com insuficiência hepática (mau funcionamento do fígado)
Em mulheres com insuficiência hepática leve ou moderada, a drospirenona é bem tolerada. Angeliq é contraindicado em mulheres com doença grave do fígado.
Pacientes com insuficiência renal (mau funcionamento dos rins)
Em mulheres com insuficiência renal leve ou moderada, foi observado um pequeno aumento na exposição da drospirenona, no entanto não é esperado ser de relevância clínica. Angeliq é contraindicado em mulheres com doença grave dos rins.
O que devo fazer se apresentar sangramento diferente?
Angeliq foi planejado para terapia de reposição hormonal sem ocorrência de sangramento no ciclo.
Entretanto, durante os primeiros meses de tratamento, pode ocorrer sangramento a qualquer momento, mas é improvável que seja abundante.
Os sangramentos devem diminuir e finalmente parar. Se continuar a ocorrer sangramento importante ou se o sangramento ou gotejamento tornarem-se incômodos para você, consulte seu médico sobre a descontinuação do tratamento ou mudança para uma terapia sequencial.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
O que devo fazer quando eu me esquecer de usar Angeliq?
Se houver um atraso de menos de 24 horas, tome o comprimido esquecido assim que lembrar e tome o próximo comprimido no horário habitual.
Se houver um esquecimento com atraso de mais de 24 horas do horário habitual, deixe o comprimido esquecido na cartela e continue tomando os comprimidos restantes no horário habitual nos dias seguintes.
Se houver interrupção da tomada dos comprimidos por vários dias, pode ocorrer sangramento irregular.
Precauções
Seu médico poderá solicitar exame ginecológico, exame das mamas, avaliação da pressão arterial e outros exames que forem julgados adequados.
Se você apresenta história de qualquer doença no fígado, seu médico irá monitorar sua função hepática periodicamente. Em caso de presença de tumor benigno (adenoma) do lobo anterior da hipófise (uma pequena glândula na base do cérebro), é necessário acompanhamento médico rigoroso, incluindo exames de sangue para avaliar os níveis de um hormônio denominado prolactina.
Angeliq não é um contraceptivo oral. Se você ainda tem a possibilidade de engravidar, é improvável que Angeliq altere esta possibilidade.
Que precauções devem ser adotadas?
Antes do início do tratamento converse com seu médico sobre os riscos e os benefícios de Angeliq. Seu médico irá discutir com você os benefícios e os riscos do uso de Angeliq.
Ele irá verificar, por exemplo, se você tem risco mais elevado de trombose devido a uma combinação de fatores. Neste caso, o risco pode ser ainda maior.
Dois grandes estudos clínicos realizados com estrogênios equinos conjugados (EEC) combinados com acetato de medroxiprogesterona (AMP), hormônios utilizados na terapia de reposição hormonal (TRH), sugerem que o risco de ocorrência de ataque cardíaco (infarto do miocárdio) pode aumentar discretamente no primeiro ano de uso destas substâncias.
Este risco não foi observado em um grande estudo clínico realizado somente com estrogênios equinos conjugados (EEC). Em dois outros grandes estudos clínicos realizados com estes hormônios, o risco de ocorrer derrame aumentou em 30 a 40%.
Embora estes estudos não tenham sido feitos com Angeliq, não se deve usar este medicamento para prevenir doença cardíaca e/ou derrame.
O uso de terapia de reposição hormonal requer cuidadosa supervisão médica na presença de qualquer uma das situações descritas a seguir, as quais devem ser comunicadas ao médico antes do início da TRH com Angeliq:
- Risco aumentado de trombose (formação de coágulo sanguíneo) (o risco aumenta com a idade, podendo ser maior no caso de você ou algum familiar direto tiverem histórico de trombose nos vasos sanguíneos das pernas ou dos pulmões, se você estiver acima do peso ou possuir varizes);
- Se você já toma Angeliq, informe seu médico, com antecedência, sobre qualquer previsão de hospitalização ou cirurgia. O risco de trombose venosa profunda pode aumentar temporariamente com cirurgias de grande porte, traumatismos graves ou imobilização prolongada;
- Se você sofre de doença dos rins leve a moderada e está sob terapia (medicamentos poupadores de potássio). Neste caso, informe ao seu médico que tipo de medicamento você está utilizando, ele poderá lhe orientar;
- Se você tem leiomioma (tumor benigno do útero);
- Se você tem ou já teve endometriose (presença de tecido de revestimento do útero – endométrio - em locais no organismo onde normalmente esse tecido não seria encontrado);
- Doença do fígado ou da vesícula biliar;
- Histórico de icterícia (pele amarelada) durante gestação ou uso prévio de hormônios sexuais;
- Diabetes;
- Presença de níveis elevados de triglicérides (um tipo de gordura no sangue);
- Pressão alta;
- Presença ou antecedentes de cloasma (pigmentação marrom-amarelada na pele). Neste caso, evite exposição excessiva ao sol ou à radiação ultravioleta durante a terapia de reposição hormonal;
- Epilepsia;
- Mamas com nódulo ou doloridas (doença benigna de mama);
- Asma;
- Enxaqueca;
- Doenças hereditárias, tais como porfiria (distúrbio metabólico) ou otosclerose (surdez);
- Lúpus eritematoso sistêmico (LES, doença imunológica crônica);
- Presença ou antecedente de coreia menor (doença que provoca movimentos involuntários e anormais do corpo);
- Episódios de inchaço em partes do corpo, tais como mãos, pés, face, vias aéreas, causados por angioedema hereditário. O hormônio estradiol contido em Angeliq pode desencadear ou intensificar estes sinais e sintomas do angioedema hereditário;
- 65 anos ou mais ao iniciar a TRH, pois há evidências limitadas de estudos clínicos que mostram que o tratamento hormonal pode aumentar o risco de perda significativa de habilidades intelectuais como memória (demência).
TRH e o câncer
Câncer do endométrio
O risco de câncer do endométrio (câncer do revestimento do útero) aumenta quando estrogênios são usados isoladamente por períodos prolongados. O progestógeno presente em Angeliq diminui este risco.
Câncer de mama
Em alguns estudos, observou-se que o câncer de mama é diagnosticado com frequência um pouco maior entre mulheres que utilizaram terapia de reposição hormonal (TRH) durante vários anos. O risco aumenta com a duração do tratamento e pode ser mais baixo ou possivelmente neutro com medicamentos que contém somente estrogênios.
Quando se interrompe a TRH, este risco aumentado desaparece em poucos anos. São observados aumentos semelhantes dos diagnósticos de câncer de mama, por exemplo, nos casos de atraso da menopausa natural, consumo excessivo de bebidas alcoólicas ou obesidade.
A TRH pode alterar a mamografia (aumenta a densidade das imagens mamográficas) e dificultar a detecção de câncer de mama em alguns casos. Desta forma, seu médico pode optar pelo uso de outras técnicas para detecção de câncer de mama.
Câncer de ovário
O câncer de ovário é menos comum do que o câncer de mama. Alguns estudos mostram um ligeiro aumento do risco global de desenvolver câncer de ovário em mulheres que usaram TRH quando comparado com as que nunca usaram TRH.
Em mulheres que atualmente usam TRH, esse risco foi mais aumentado. Estas associações não foram mostradas em todos os estudos.
Não há evidência consistente de que o risco de desenvolver câncer de ovário esteja relacionado com a duração da TRH. No entanto, o risco pode ser mais relevante com o uso prolongado (durante vários anos).
Câncer de fígado
Durante ou após o uso de hormônios sexuais tais como os contidos em Angeliq, foram observados raros casos de tumores hepáticos benignos e, ainda mais raramente de tumores hepáticos malignos que, em casos isolados, ocasionaram hemorragias intra-abdominais com risco para a vida da paciente.
Embora tais eventos sejam extremamente improváveis, informe seu médico se você apresentar quaisquer distúrbios abdominais incomuns que não desapareçam em curto espaço de tempo.
Descontinue o uso de Angeliq e procure o médico imediatamente se apresentar:
- Ocorrência, pela primeira vez, de enxaqueca (tipicamente representada por dor de cabeça latejante e náuseas e precedida por distúrbios visuais);
- Agravamento de enxaqueca preexistente ou dor de cabeça com intensidade ou frequência incomuns;
- Distúrbios repentinos de visão ou audição;
- Veias inflamadas (flebite).
Descontinue imediatamente a terapia com Angeliq e procure seu médico se você apresentar:
- Falta de ar;
- Tosse com sangue;
- Dores incomuns ou inchaço nas pernas ou braços;
- Dificuldade respiratória repentina;
- Desmaio.
Podem ser sinais indicativos de formação de coágulo (trombose).
Angeliq também deve ser interrompido imediatamente se você ficar grávida ou apresentar icterícia (pele e mucosas amareladas).
Procure seu médico se ocorrer sangramento após um período prolongado de ausência de menstruação (amenorreia).
Consumo de álcool
O consumo excessivo de bebida alcoólica durante o uso de TRH exerce influência sobre o tratamento. Seu médico poderá orientá-la a respeito.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Como todos os medicamentos, Angeliq pode ocasionar reações adversas.
Resumo do perfil de segurança:
As reações adversas graves que estão associadas à utilização da terapia de reposição hormonal e sintomas relacionados estão descritas no item “Precauções”. Leia essas informações com cuidado e, se necessário, consulte seu médico.
As reações adversas mais frequentemente relatadas com o uso de Angeliq são:
- Dor nas mamas;
- Sangramento vaginal (sangramento do trato genital feminino);
- Dores abdominais e gastrintestinais.
Durante os primeiros meses de tratamento, pode ocorrer sangramento vaginal em episódios inesperados (sangramento e gotejamento). Estes geralmente são temporários e normalmente desaparecem com a continuação do tratamento.
Se isto não ocorrer, consulte seu médico.
As reações adversas graves incluem coágulos nas artérias e veias (trombose) e câncer de mama.
As reações adversas descritas a seguir são baseadas nos relatórios dos estudos clínicos.
As reações adversas estão representadas em ordem decrescente de gravidade, separadas por grupo de frequência.
Reações adversas muito comuns (mais de 10 pessoas a cada 100 podem apresentar estas reações):
- Dor nas mamas***;
- Sangramento vaginal (sangramento do trato genital feminino).
Reações adversas comuns (entre 1 e 10 pessoas a cada 100 podem apresentar estas reações):
- Labilidade emocional;
- Enxaqueca;
- Dores abdominais e gastrintestinais;
- Pólipo no colo do útero.
Reações adversas incomuns (entre 1 e 10 pessoas a cada 1 000 podem apresentar estas reações):
- Formação de coágulos arteriais e venosos (trombose)*;
- Câncer de mama**.
*A evidência relacionada ao grau de parentesco e a frequência estimada foram derivadas dos estudos epidemiológicos com Angeliq (EURAS HRT).
“Eventos tromboembólicos arteriais e venosos” envolvem as seguintes entidades médicas:
- Oclusão venosa profunda periférica;
- Trombose e embolia/oclusão vascular pulmonar;
- Trombose, embolia e infarto/infarto do miocárdio/infarto cerebral e derrame não caracterizado como hemorrágico.
**A evidência relacionada ao grau de parentesco foi derivada dos dados da experiência pós-comercialização, e a frequência estimada foi derivada de estudos clínicos com Angeliq.
***Incluindo desconforto nas mamas.
Para informações adicionais sobre eventos tromboembólicos arteriais e venosos, câncer de mama e enxaqueca vide item “Contraindicações”.
Descrição das reações adversas reportadas:
As reações adversas com frequência muito baixa ou aparecimento tardio dos sintomas que estão relacionadas ao grupo de medicamentos combinados de uso contínuo para terapia de reposição hormonal estão listadas a seguir.
Tumores:
- Tumor de fígado (benigno e maligno);
- Condições malignas e pré-malignas influenciadas por esteroides sexuais (se uma determinada condição é conhecida, constitui-se uma contraindicação para o uso de Angeliq).
Em alguns estudos, a ocorrência de câncer de ovário foi observada com frequência ligeiramente maior em usuárias de TRH (TRH com apenas estrogênio ou combinado de estrogênio-progestógeno). O risco pode ser mais relevante com o uso prolongado (durante vários anos).
Outras condições:
- Doença da vesícula biliar (sabe-se que os estrogênios aumentam a formação de cálculos da vesícula biliar);
- Demência (existe evidência limitada, observada em estudos clínicos com produtos contendo estrogênios equinos conjugados (EEC), de que a terapia hormonal pode aumentar o risco de provável demência se iniciada em mulheres com idade igual ou superior a 65 anos. O risco pode diminuir se o tratamento for iniciado próximo da menopausa, como observado em outros estudos. Não se sabe se estes dados também se estendem a outros medicamentos para TRH);
- Câncer do endométrio (estudos sugerem que a adição apropriada de progestógeno na terapia elimina o aumento no risco resultante da terapia utilizando apenas estrogênios);
- Pressão alta (Angeliq apresenta potencial para diminuir a pressão arterial em mulheres com pressão arterial elevada);
- Distúrbios da função hepática;
- Níveis elevados de triglicérides (risco aumentado de pancreatite em usuárias de TRH);
- Alterações na tolerância à glicose e resistência periférica à insulina;
- Aumento do tamanho de miomas uterinos;
- Reativação de endometriose;
- Adenoma (tumor geralmente benigno) de hipófise (prolactinoma) (risco de agravamento de hiperprolactinemia ou indução de crescimento de tumor);
- Cloasma (manchas castanho amarelada na pele);
- Icterícia e/ou prurido (coceira intensa) relacionado à colestase (supressão do fluxo da bile);
- Em mulheres com angioedema hereditário, o uso de estrogênios exógenos pode induzir ou intensificar os sintomas de angioedema (episódios de inchaço em partes do corpo, tais como mãos, pés, face, vias aéreas);
- Hipersensibilidade (incluindo erupção cutânea e urticária).
- Ocorrência ou agravamento de doenças para as quais a associação com TRH não é conclusiva: epilepsia, doença benigna das mamas, asma, porfiria, lúpus eritematoso sistêmico, otosclerose, coreia menor;
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também a empresa através do seu serviço de atendimento.
População Especial
Gravidez e lactação
Angeliq não deve ser utilizado por mulheres durante a gravidez ou lactação. Entretanto, estudos têm demonstrado que hormônios esteroides (tais como, as substâncias ativas contidas em Angeliq) não parecem aumentar o risco de malformações congênitas em crianças nascidas de mulheres que tenham utilizado tais hormônios antes da gestação ou que utilizaram inadvertidamente no início da gestação.
A TRH não deve ser utilizada durante a amamentação, pois pequenas quantidades de hormônios sexuais podem ser excretadas no leite materno.
Efeitos sobre a capacidade de dirigir veículos e operar máquinas
Não há conhecimento de efeitos ou restrições sobre o uso de Angeliq quanto à capacidade de dirigir e operar máquinas.
Composição
Cada comprimido revestido de Angeliq contém:
1mg de estradiol (correspondente a 1,033mg de estradiol hemi-hidratado) e 2mg de drospirenona.
Excipientes: lactose monoidratada, amido, povidona, estearato de magnésio, hipromelose, macrogol, talco, dióxido de titânio, pigmento de óxido de ferro vermelho.
Superdosagem
Não há relatos de efeitos adversos relacionados à superdose.
A superdose pode causar náuseas, vômitos e sangramento irregular.
Não é necessário tratamento específico, mas caso você não tenha certeza, consulte o seu médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Nota: As informações de medicamentos usados concomitantemente devem ser consultadas para que sejam identificadas potenciais interações.
Efeitos de outros medicamentos sobre Estradiol Hemi-Hidratado + Drospirenona (substância ativa)
Podem ocorrer interações com medicamentos que induzem as enzimas microssomais as quais podem resultar em aumento da depuração de hormônios sexuais e que podem levar a alterações no perfil do sangramento uterino e/ou redução do efeito terapêutico.
A indução enzimática já pode ser observada após alguns dias de tratamento, e atinge graus máximos geralmente em poucas semanas. A indução enzimática pode ser mantida por cerca de 4 semanas, após a descontinuação da medicação.Substâncias que aumentam a depuração doshormônios sexuais (diminuição da eficácia por indução enzimática), por exemplo: fenitoína, barbitúricos, primidona, carbamazepina, rifampicina, e possivelmente também oxcarbazepina, topiramato, felbamato, griseofulvina e produtos que contenham erva-de-São-João.
Substâncias com efeitos variáveis na depuração de hormônios sexuais. Quando coadministrados com hormônios sexuais, muitos inibidores de protease e inibidores não-nucleosídicos da transcriptase reversa do HIV/HCV podem aumentar ou reduzir a concentração plasmática do estrogênio ou do progestógeno ou de ambos. Estas alterações podem ser clinicamente relevantes em alguns casos.
Substâncias que diminuem a depuração de hormônios sexuais (inibidores enzimáticos) Inibidores fortes e moderados do CYP3A4, tais como antifúngicos azólicos (por exemplo, fluconazol, itraconazol, cetoconazol, voriconazol,), macrolídeos (por exemplo, claritromicina, eritromicina), verapamil, diltiazem podem aumentar as concentrações plasmáticas do progestógeno ou do estrogênio ou de ambos. Em um estudo de dose múltipla com uma associação de drospirenona (3 mg/dia) / estradiol (1,5 mg/dia), a coadministração do cetoconazol, forte inibidor do CYP3A4, por 10 dias aumentou a ASC (0-24 h) da drospirenona em 2,30 vezes (IC 90%: 2,08; 2,54). Nenhuma alteração foi observada para estradiol, embora o ASC (0-24 h) da estrona, seu metabólito menos potente, tenha aumentado 1,39 vezes (IC 90%: 1,27; 1,52).
Efeitos de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) sobre outros medicamentos
In vitro, a drospirenona é capaz de inibir fraca a moderadamente as enzimas do citocromo P450 CYP1A1, CYP2C9, CYP2C19 e CYP3A4. Com base em estudos de interação in vivo, em voluntárias utilizando omeprazol, sinvastatina, ou midazolam como substratos marcadores, que é improvável a interação clinicamente relevante da drospirenona na dose de 3 mg com o metabolismo de outros fármacos mediado pelo citocromo P450.
Interação farmacodinâmica com anti-hipertensivos e antiinflamatórios não esteroidais (AINEs)
Mulheres hipertensas que fazem uso de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) e medicação anti-hipertensiva, como por exemplo, inibidores da ECA, antagonistas dos receptores de angiotensina II e hidroclorotiazida, podem apresentar diminuição adicional na pressão arterial.
É improvável o aumento no potássio sérico com o uso conjunto de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) e antiinflamatórios não-esteroidais ou medicamentos anti-hipertensivos. O uso concomitante desses três tipos de medicação pode causar um pequeno aumento no potássio sérico, mais pronunciado em mulheres diabéticas.
Exames laboratoriais
O uso de esteroides sexuais pode influenciar os resultados de certos exames laboratoriais, incluindo parâmetros bioquímicos das funções hepática, tiroidiana, adrenal e renal; níveis plasmáticos de proteínas (transportadoras), por exemplo, globulina de ligação aos hormônios sexuais, frações lipídicas/lipoproteicas; e parâmetros da coagulação e fibrinólise. As alterações geralmente permanecem dentro do intervalo laboratorial considerado normal. A tolerância à glicose não foi afetada pelo uso de Estradiol Hemi-Hidratado + Drospirenona (substância ativa).
Interação Alimentícia
Substâncias que diminuem a depuração de hormônios sexuais (inibidores enzimáticos)
Suco de toranja (grapefruit) pode aumentar as concentrações plasmáticas do progestógeno ou do estrogênio ou de ambos.
Interação com bebidas alcoólicas
A ingestão aguda de bebidas alcoólicas durante a TRH pode ocasionar elevação nos níveis de estradiol circulante.
Ação da Substância
Resultados de eficácia
Três estudos (96082, 97182 e 96097) mostraram superioridade de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) em comparação ao placebo na diminuição da frequência e da intensidade dos sintomas climatéricos. O estudo fase II/III 96082 mostrou que placebo reduziu as ondas de calor em 45% e Estradiol Hemi-Hidratado + Drospirenona (substância ativa) reduziu em 90%. O estudo 97182 mostrou que Estradiol Hemi-Hidratado + Drospirenona (substância ativa) diminuiu a prevalência de ondas de calor, de 70% na linha basal para menos de 30% na 4ª semana e para menos de 10% na 12ª semana, mantendo a prevalência em cerca de 5% ao fim de dois anos de tratamento.
Em um estudo clínico com 1.142 pacientes foi observada atrofia/inativação do endométrio em 72% a 77% das mulheres após 12 meses de tratamento com Estradiol Hemi-Hidratado + Drospirenona (substância ativa). Estradiol Hemi-Hidratado + Drospirenona (substância ativa) opõe-se efetivamente ao desenvolvimento de hiperplasia endometrial induzida por estrógeno. Em um subgrupo deste estudo foi demonstrado perfil lipídico com diminuição de todas as frações do colesterol.
Caraterísticas Farmacológicas
Farmacodinâmica
Estradiol Hemi-Hidratado + Drospirenona (substância ativa) contém 17-beta-estradiol, que é química e biologicamente idêntico ao estrogênio (E2) humano endógeno (natural), e o progestógeno sintético drospirenona (DRSP). O 17-beta-estradiol propicia reposição hormonal durante e após o climatério.
A adição de drospirenona (DRSP) auxilia na promoção do controle de sangramento e contrapõe-se ao desenvolvimento de hiperplasia endometrial causada por estrogênios.
Efeitos do estradiol
A perda da função ovariana, acompanhada por depleção da produção de estrogênio e progesterona, leva à síndrome menopausal caracterizada por sintomas vasomotores e orgânicos. A terapia de reposição hormonal (TRH) é indicada para eliminar estes sintomas. De todos os estrogênios fisiológicos, o E2 é o mais potente e com maior afinidade pelo receptor de estrogênio. Órgãos-alvo do estrogênio incluem, particularmente, útero, hipotálamo, hipófise, vagina, mamas e ossos (osteoclastos).
Outros efeitos dos estrogênios incluem redução das concentrações de insulina e glicose sanguíneas, efeitos vasoativos locais mediados por receptores e efeitos independentes do receptor sobre o músculo liso vascular. Receptores de estrogênio foram sido identificados no coração e nas artérias coronarianas.
A administração oral de estrogênios naturais é vantajosa em certos casos de hipercolesterolemia, com a finalidade de maximizar os efeitos benéficos do metabolismo hepático sobre os lípides. Após um ano de tratamento com Estradiol Hemi-Hidratado + Drospirenona (substância ativa), as alterações médias nos níveis de HDLcolesterol foram pequenas, com leve aumento de 1,1% para a associação com 1 mg de DRSP e leve diminuição de -1,6% e -3,4% para a associação com 2 mg e 3 mg de DRSP, respectivamente.
Os níveis séricos de LDL-colesterol diminuíram em média -11% (1 mg DRSP), -14% (2 mg DRSP) e -13% (3 mg DRSP) quando comparados a diminuição de 9% após um ano de tratamento com 1 mg de E2 isoladamente. A associação com DRSP parece atenuar o aumento nos níveis de triglicérides promovido pelo tratamento com 1 mg de E2 isoladamente. Após 1 ano de tratamento com 1 mg de E2, os níveis de triglicérides das pacientes estavam, na média, aproximadamente 18% acima dos valores basais, quando comparados aos aumentos médios de 9% (1 mg de DRSP), 5% (2 mg DRSP) e 4% para as associações de 1 mg de E2 com DRSP.
O tratamento com Estradiol Hemi-Hidratado + Drospirenona (substância ativa) por 2 anos promoveu aumento médio na densidade mineral óssea de aproximadamente 3 a 5%, enquanto que após a administração de placebo observou-se diminuição média de aproximadamente 0,5%. Tanto nas pacientes osteopênicas quanto nas não-osteopênicas verificou-se uma diferença estatisticamente significativa na densidade mineral do osso ilíaco entre o tratamento com a substância ativa e o tratamento com o placebo. Também foi observado aumento na densidade mineral óssea da coluna lombar e no corpo todo nos grupos que receberam substância ativa.
Em mulheres que não apresentam osteoporose na pós-menopausa, o uso de TRH por períodos prolongados tem demonstrado diminuir o risco de ocorrência de fraturas periféricas. A TRH também exerce efeito positivo sobre o colágeno e a espessura da pele e pode retardar o processo de enrugamento da pele. Monoterapia com estrogênio exerce efeito estimulante dose-dependente sobre a mitose e a proliferação do endométrio, aumentando, assim, a frequência de hiperplasia endometrial e, consequentemente, o risco de carcinoma endometrial. Com a finalidade de evitar hiperplasia endometrial, é necessária a associação com um progestógeno.
Efeitos da drospirenona
A drospirenona exerce efeitos farmacodinâmicos muito semelhantes ao da progesterona natural.
Atividade progestogênica
A drospirenona é um progestógeno potente com efeito inibidor central sobre o eixo hipotálamo-hipófise-gônadas. Em mulheres férteis, a DRSP exerce efeito contraceptivo; a ovulação é inibida quando a DRSP é administrada isoladamente. A dose mínima de DRSP para inibição da ovulação é de 2 mg/dia. A transformação completa de um endométrio estimulado por estrogênio ocorre após uma dose de 4 ou 6 mg/dia por 10 dias (= 40 a 60 mg por ciclo). Estradiol Hemi-Hidratado + Drospirenona (substância ativa) é uma terapia de reposição hormonal combinada contínua administrada com a intenção de evitar o sangramento regular por privação associado à TRH cíclica ou sequencial.
Durante os primeiros meses de tratamento, sangramento e gotejamento são bastante comuns, mas diminuem com a continuação da terapia. Com Estradiol Hemi-Hidratado + Drospirenona (substância ativa) (2 mg de DRSP), a taxa de amenorreia aumenta rapidamente para 81%, 86% e 91% nos ciclos 6, 12 e 24, respectivamente. A drospirenona contida em Estradiol Hemi-Hidratado + Drospirenona (substância ativa) contrapõe-se efetivamente ao desenvolvimento de hiperplasia endometrial induzida por estrogênio. Após 12 meses de tratamento com Estradiol Hemi-Hidratado + Drospirenona (substância ativa) (doses de 0,5, 1, 2 ou 3 mg de DRSP) foi observado endométrio atrófico / inativo em 71 – 77% das mulheres.
Atividade antimineralocorticoide
A drospirenona tem propriedades antagonistas competitivas à aldosterona. Efeitos hipotensores são mais pronunciados com altas doses de DRSP em mulheres hipertensas. Pacientes hipertensas que receberam Estradiol Hemi-Hidratado + Drospirenona (substância ativa) por 8 semanas demonstraram redução significativa nos valores de pressão sistólica/diastólica (medição não-ambulatorial versus valor basal -12/-9 mmHg, versus placebo -3/-4 mmHg; 24h de monitorização ambulatorial da pressão arterial (MAPA) versus valor basal -5/-3 mmHg, versus placebo 3/-2 mmHg). Os efeitos são aparentes dentro de 2 semanas com efeitos máximos observados dentro de 6 semanas a partir do início da terapia.
Tabela: Alteração média ajustada da pressão arterial sistólica/diastólica com relação aos valores basais, em mmHg:
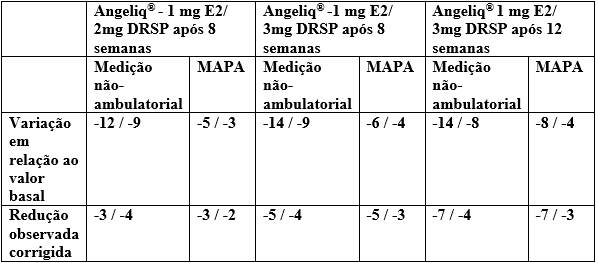
 MAPA = Monitorização Ambulatorial de Pressão Arterial de 24h.
MAPA = Monitorização Ambulatorial de Pressão Arterial de 24h.
Mulheres normotensas não apresentaram alterações relevantes na pressão arterial. Em estudos clínicos com Estradiol Hemi-Hidratado + Drospirenona (substância ativa), o peso corporal médio permaneceu inalterado (1 mg de DRSP) ou diminuiu durante o período de tratamento de 12 meses em 1,1 a 1,2 kg (3 ou 2 mg de DRSP diariamente). Comparativamente, foi observado aumento de 0,5 kg em pacientes que receberam E2 isoladamente.
Mulheres que receberam DRSP em associação com estradiol durante estudo clínico relataram menos edema periférico do que as que receberam E2 isolado. Em mulheres com angina pectoris, a administração de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) (2mg de drospirenona) durante 6 semanas, melhorou a adaptação ao estresse do fluxo coronário de reserva (alteração relativa de + 14% vs. -15% no grupo placebo).
Atividade anti-androgênica
Assim como a progesterona natural, a DRSP apresenta propriedades anti-androgênicas.
Efeitos sobre o metabolismo de carboidratos
A drospirenona não apresenta atividade glicocorticoide ou antiglicocorticoide e nenhum efeito sobre a tolerância à glicose e resistência à insulina. A tolerância à glicose não é modificada pelo uso de Estradiol Hemi-Hidratado + Drospirenona (substância ativa).
Outras propriedades
Estradiol Hemi-Hidratado + Drospirenona (substância ativa) exerce efeito positivo sobre o bem-estar e a qualidade de vida. Os efeitos benéficos avaliados pelo “Women's Health Questionnaire" foram significativamente superiores ao tratamento com E2 isoladamente (escore total). Este aumento foi devido, principalmente, à melhora em sintomas somáticos, ansiedade/medos e dificuldades cognitivas. Estudos observacionais e o estudo do “Women’s Health Initiative” (WHI) com estrogênios equinos conjugados (EEC) associados ao acetato de medroxiprogesterona (AMP) sugerem redução na morbidade do câncer de cólon em mulheres na pósmenopausa que utilizam TRH. No estudo WHI com monoterapia de EEC não foi observada redução no risco. Não se sabe se estes achados também se estendem a outros medicamentos para TRH.
Farmacocinética
Drospirenona
Absorção
A DRSP é rápida e quase que totalmente absorvida quando administrada por via oral. As concentrações séricas máximas da drospirenona, conforme indicadas na tabela a seguir, são alcançadas em cerca de 1 hora após a ingestão de dose única ou múltipla de Estradiol Hemi-Hidratado + Drospirenona (substância ativa). A farmacocinética da DRSP é proporcional à dose dentro do intervalo de dose de 0,25 a 4 mg. A biodisponibilidade está compreendida entre 76 e 85%. A ingestão de alimentos não exerce qualquer influência sobre a biodisponibilidade da DRSP quando comparado à ingestão da drospirenona em jejum.
Parâmetro farmacocinético
Estradiol Hemi-Hidratado + Drospirenona (substância ativa) 1 mg E2 / 2 mg DRSP* Cmáx, dose única [ng/ml] 21,9 Cmáx, estado de equilíbrio [ng/ml] 35,9 ASC (0 – 24 h), dose única [ng/ml] 161 ASC (0 – 24 h), estado de equilíbrio [ng/ml] 408 * dados para Estradiol Hemi-Hidratado + Drospirenona (substância ativa) foram calculados por interpolação entre as doses investigadas de 1 mg de DRSP + 1 mg de E2 e 4 mg de DRSP + 1 mg de E2. Cmáx: concentração máxima.
Distribuição
Após administração oral, os níveis séricos da DRSP diminuem em duas fases, com meia-vida terminal média de cerca de 35 a 39 horas. A drospirenona liga-se à albumina sérica, mas não à globulina de ligação aos hormônios sexuais (SHBG) ou à globulina de ligação aos corticoides (CBG). Somente 3 a 5% das concentrações séricas totais do fármaco estão presentes na forma de esteroides livres. A média do volume aparente de distribuição da DRSP é de 3,7 a 4,2 l/kg.
Metabolismo
A drospirenona é amplamente metabolizada após administração oral. Os principais metabólitos no plasma são: a forma ácida da DRSP, formada pela abertura do anel de lactona e o 4,5-diidro-drospirenona-3-sulfato, ambos formados sem o envolvimento do sistema P450. Verifica-se, a partir de dados de estudo in vitro, que a drospirenona é metabolizada em pequena proporção pelo citocromo P450 3A4.
Eliminação
A depuração total da DRSP do soro é de 1,2 a 1,5 ml/min/kg. A drospirenona é eliminada na forma inalterada apenas em quantidades mínimas. Seus metabólitos são excretados nas fezes e urina a uma razão de excreção de aproximadamente 1,2 a 1,4. A meia-vida de excreção dos metabólitos na urina e nas fezes é de cerca de 40 horas.
Condições no estado de equilíbrio
Após administração repetida diária de Estradiol Hemi-Hidratado + Drospirenona (substância ativa), a concentração sérica máxima da DRSP no estado de equilíbrio é alcançada conforme indicado na tabela anterior. As condições no estado de equilíbrio são alcançadas após cerca de 10 dias de tratamento diário com Estradiol Hemi-Hidratado + Drospirenona (substância ativa). Os níveis séricos de DRSP acumulam-se por um fator de cerca de 2 a 3 como consequência da proporção entre a meia-vida terminal e o intervalo de administração do medicamento.
Estradiol
Absorção
O E2 é rápida e completamente absorvido quando administrado por via oral. Durante a absorção e a primeira passagem pelo fígado, o E2 sofre extensa metabolização reduzindo, desta forma, a biodisponibilidade absoluta após administração oral a cerca de 5% da dose. Concentrações máximas de cerca de 16 ou 22 pg/ml foram geralmente obtidas em 2 a 8 horas após administração oral única de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) contendo 0,5 ou 1 mg de E2, respectivamente. A ingestão de alimentos não exerce qualquer influência sobre a biodisponibilidade do E2 quando comparado à ingestão do fármaco em jejum.
Distribuição
Após administração oral de Estradiol Hemi-Hidratado + Drospirenona (substância ativa), em intervalos de 24 horas, observou-se apenas alteração gradual dos níveis séricos de E2. Devido ao grande número de sulfatos e glicuronídios de estrogênio em circulação e também à recirculação êntero-hepática, a meia-vida terminal do E2 representa um parâmetro composto que é dependente de todos estes processos e encontra-se no intervalo de cerca de 13 a 20 horas, após administração oral. O estradiol liga-se de forma inespecífica à albumina sérica e de forma específica à SHBG. Apenas cerca de 1 a 2% do E2 circulante está presente na forma de esteroide livre, 40 a 45% estão ligados à SHBG.
O E2 administrado por via oral induz a formação de SHBG que influencia a distribuição com referência às proteínas séricas, promovendo aumento da fração ligada à SHBG e diminuição da fração ligada à albumina e da fração não-ligada, indicando não-linearidade da farmacocinética do E2 após a ingestão de Estradiol Hemi-Hidratado + Drospirenona (substância ativa). O volume aparente de distribuição de E2 após administração de dose única por via intravenosa é de cerca de 1 l/kg.
Metabolismo
O estradiol é rapidamente metabolizado e além de estrona e sulfato de estrona, um grande número de outros metabólitos e conjugados são formados. Estrona e estriol são conhecidos como metabólitos farmacologicamente ativos do E2; apenas a estrona ocorre em concentrações relevantes no plasma. A estrona alcança níveis séricos aproximadamente 6 vezes mais elevados do que os do E2. Os níveis séricos dos conjugados de estrona são aproximadamente 26 vezes mais altos do que as concentrações correspondentes de estrona livre.
Eliminação
Observa-se que a depuração metabólica é de cerca de 30 ml/min/kg. Os metabólitos do E2 são excretado na urina e na bile, com meia-vida de aproximadamente 1 dia.
Condições no estado de equilíbrio
Após administração oral diária de Estradiol Hemi-Hidratado + Drospirenona (substância ativa), as concentrações de E2 atingem o estado de equilíbrio após cerca de 5 dias. Os níveis de E2 sérico acumulam-se em aproximadamente 2 vezes. Com um intervalo de dose de 24 horas, os níveis séricos médios no estado de equilíbrio do E2 variam dentro do intervalo de 12 a 29 ou 20 a 43 pg/ml após administração de Estradiol Hemi-Hidratado + Drospirenona (substância ativa) contendo 0,5 ou 1 mg de E2, respectivamente.
Populações especiais
Insuficiência hepática
A farmacocinética de uma dose oral única de 3 mg de DRSP associada a 1 mg de E2 foi avaliada em 10 pacientes com insuficiência hepática moderada (Child Pugh B) e 10 voluntárias saudáveis comparáveis em termos de idade, peso e histórico de tabagismo.
Os perfis concentração de DRSP sérica média versus tempo foram comparáveis em ambos os grupos de mulheres durante as fases de absorção/distribuição com valores de Cmáx e tmáx similares, sugerindo que a taxa de absorção não foi afetada pela insuficiência hepática. A meia-vida terminal média foi prolongada em torno de 1,8 vezes e a exposição sistêmica aumentou cerca de 2 vezes, correspondendo a uma diminuição de aproximadamente 50% na depuração oral aparente (CL/f) em voluntárias com insuficiência hepática moderada quando comparadas àquelas com função hepática normal.
O declínio observado na depuração da DRSP em voluntárias com insuficiência hepática moderada comparado ao de voluntárias com função hepática normal não apresentou qualquer diferença aparente em relação às concentrações séricas de potássio entre os dois grupos de voluntárias. Mesmo na presença de diabetes e tratamento concomitante com espironolactona (dois fatores que podem predispor a paciente à hipercalemia), não foi observado aumento nas concentrações séricas de potássio acima do limite superior do intervalo de normalidade. Portanto, pode-se concluir que a DRSP é bem tolerada em pacientes com insuficiência hepática leve ou moderada (Child Pugh B).
Insuficiência renal
O efeito da insuficiência renal sobre a farmacocinética da DRSP (3 mg diariamente por 14 dias) foi investigado em mulheres com função renal normal e com insuficiência renal leve e moderada. No estado de equilíbrio do tratamento com DRSP, os níveis séricos de DRSP no grupo com insuficiência renal leve (depuração de creatinina de 50 a 80 ml/min) foram comparáveis aos do grupo com função renal normal (depuração de creatinina maior do que 80 ml/min).
Os níveis séricos de DRSP foram em média 37% mais elevados no grupo com insuficiência renal moderada (depuração de creatinina de 30 a 50 ml/min) quando comparados com o grupo que apresenta função renal normal. A análise de regressão linear da área sob a curva (AUC) dos valores de DRSP (0 a 24 h) em relação à depuração de creatinina revelou aumento de 3,5%, com uma redução da depuração de creatinina de 10 ml/min. Não se espera que este leve aumento tenha relevância clínica.
Grupos Étnicos
O impacto de fatores étnicos sobre a farmacocinética da DRSP (1 – 6 mg) e etinilestradiol (0,02mg) foi estudado após administração oral de doses única e repetida diariamente em mulheres sadias, jovens, caucasianas e japonesas. Os resultados mostraram que as diferenças étnicas entre as mulheres caucasianas e japonesas não tiveram influência clinicamente relevante sobre a farmacocinética da DRSP e etinilestradiol.
Dados de segurança pré-clínicos
Os dados pré-clínicos baseados em estudos convencionais de toxicidade de dose repetida, genotoxicidade, potencial carcinogênico e toxicidade para reprodução não indicaram riscos relevantes para seres humanos. No entanto, deve-se considerar que esteroides sexuais podem promover o crescimento de certos tecidos e tumores dependentes de hormônios.
Cuidados de Armazenamento
Angeliq deve ser conservado em temperatura ambiente (entre 15oC e 30oC). Proteger da umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características do medicamento:
Angeliq apresenta-se na forma de comprimidos revestidos de cor vermelho rosado sem odor ou gosto característico.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Venda sob prescrição médica.
MS - 1.7056.0039
Farm. Resp.:
Dra. Dirce Eiko Mimura CRF-SP nº 16532.
Fabricado por:
Bayer Weimar GmbH und Co. KG Weimar - Alemanha.
Embalado por:
Schering do Brasil, Química e Farmacêutica Ltda.
São Paulo - SP.
Importado por:
Bayer S.A.
Rua Domingos Jorge, 1.100 – Socorro 04779-900 – São Paulo - SP
C.N.P.J. n.º 18.459.628/0001-15
Indústria Brasileira.