Comparamos o preço de Apidra - 100Ui Injetável Solostar 3Ml, veja o menor preço

R$ 38,50
BBiológicos
13
ofertasMelhores preços a partir de R$ 38,50 até R$ 48,59
Menor preço
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Entregas para todo o Brasil. Clique e confira!
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
Enviamos para todo o Brasil. Clique e confira!
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Pagamento em até 6X sem juros. Frete Grátis! Regras no Site.
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Preço Válido para compra em Boleto
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Para que serve
Apidra é destinada ao tratamento do diabetes mellitus que requer tratamento com insulina.
Como Apidra SoloStar funciona?
Apidra Solostar é um antidiabético que contém insulina glulisina, uma insulina humana análoga, produzida a partir da tecnologia de DNA recombinante. A atividade principal das insulinas é a regulação do metabolismo da glicose.
Tempo médio de início de ação:
Após a administração subcutânea, o efeito de Apidra SoloStar apresenta início de ação mais rápido e duração mais curta do que a insulina humana regular.
Contraindicação
Apidra SoloStar não deve ser utilizada em pacientes com alergia à insulina glulisina ou a qualquer um dos componentes da fórmula.
Como usar
Apidra SoloStar deve ser administrada por via subcutânea por injeção (em até 15 minutos antes ou imediatamente após uma refeição).
A injeção subcutânea deve ser administrada na parede abdominal, na coxa ou no músculo deltoide. Como ocorre com todas as insulinas, os locais de injeção dentro de uma determinada área (abdome, coxa ou deltoide) devem ser alternados de uma administração para a outra.
Como ocorre com todas as insulinas, a taxa de absorção e, consequentemente, o início e a duração da ação podem ser alterados pelo local da administração, exercícios e outras variáveis.
Preparo e Manipulação
Antes do primeiro uso, Apidra SoloStar deve ser mantida em temperatura ambiente por 1 a 2 horas.
Apidra SoloStar não permite que o seu conteúdo seja misturado a nenhuma outra insulina.
Apidra SoloStar só deve ser utilizada se a solução estiver límpida, incolor, sem nenhuma partícula sólida visível e se tiver consistência aquosa.
As canetas vazias nunca devem ser reutilizadas, devendo ser adequadamente descartadas.
Populações especiais
Caso você apresente insuficiência do fígado ou dos rins, as exigências de insulina podem ser menores.
Como utilizar a caneta
Verifique sempre o manual para utilização de Apidra SoloStar e siga estritamente suas recomendações. Se você tiver dúvidas relacionadas à caneta e sua utilização, entre em contato com o Serviço de Atendimento ao Consumidor da Sanofi-Aventis.
Não há estudos dos efeitos de Apidra SoloStar administrada por vias não recomendadas. Portanto, por segurança e para garantir a eficácia deste medicamento, a administração deve ser somente por via subcutânea, conforme prescrição médica.
Posologia
Apidra SoloStar deve ser administrada por via subcutânea.
Apidra SoloStar é uma insulina humana recombinante análoga que demonstrou ter a mesma potência da insulina humana. Uma unidade internacional de Apidra SoloStar tem o mesmo efeito redutor da glicose no sangue de uma unidade internacional de insulina humana regular. Após a administração subcutânea, seu início de ação é mais rápido e sua duração de ação mais curta.
A dose de Apidra SoloStar deve ser individualizada e determinada com base nas orientações médicas de acordo com as suas necessidades.
Apidra SoloStar deve normalmente ser usada em esquemas que incluem uma insulina de ação mais prolongada ou uma insulina basal análoga.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
Instruções para uso da caneta SoloStar
SoloStar é uma caneta preenchida para aplicação de insulina. Seu médico decidiu que SoloStar é apropriada para você, com base na sua capacidade de manuseá-la. Converse com ele sobre a técnica de injeção apropriada antes de usar SoloStar.
Leia cuidadosamente estas Instruções antes de utilizar SoloStar. Se não sentir-se capaz de utilizar a caneta SoloStar ou seguir todas as instruções de forma adequada sozinho, você deve utilizar SoloStar somente com a ajuda de uma pessoa que possa seguir completamente as instruções. Segure a caneta de acordo com as figuras deste manual. Para garantir que você está lendo corretamente a dose, segure a caneta horizontalmente, com a agulha virada para a esquerda e o seletor de dosagem para a direita, conforme figura ao lado.
Cada SoloStar contém um total de 300 unidades de insulina. Você pode ajustar dosagens de 1 a 80 unidades de 1 em 1 unidade. Cada caneta contém múltiplas doses.
Guarde este folheto para consulta futura.
Se você tiver dúvidas quanto ao uso da caneta SoloStar ou sobre diabetes, consulte seu médico ou ligue para o Serviço de Atendimento ao Consumidor da sanofi-aventis.
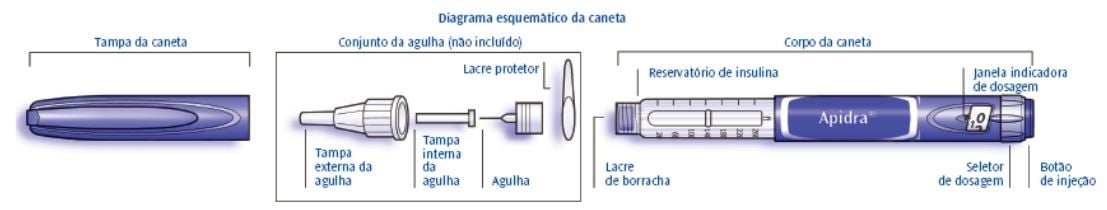
Informações importantes para o uso de SoloStar:
- Sempre afixe uma agulha nova antes de cada uso. Somente utilize agulhas que sejam compatíveis para o uso com SoloStar.
- Não selecione uma dose e/ou pressione o botão de injeção sem que a agulha esteja afixada.
- Sempre faça o teste de segurança antes de cada injeção.
- Esta caneta é apenas para seu uso. Não a compartilhe com mais ninguém.
- Caso o produto seja aplicado por outra pessoa que não você, devem ser tomados cuidados especiais para evitar acidentes com a agulha e a transmissão de doenças infecciosas.
- Nunca use SoloStar se a mesma estiver danificada ou se você não tiver certeza de que ela esteja funcionando adequadamente.
- Tenha sempre uma SoloStar de reserva para o caso da sua se perder ou se danificar.
1ª Etapa: Verificação da insulina
- Verifique o rótulo da caneta SoloStar para certificar-se de que você está com a insulina correta. Apidra SoloStar é azul e tem um botão de aplicação azul escuro com um anel no topo.
- Remova a tampa da caneta.
- Verifique a aparência de sua insulina. Apidra SoloStar é uma insulina límpida, incolor, sem partículas sólidas visíveis e com consistência aquosa. Não use a SoloStar se a insulina estiver turva, com cor ou com partículas.
2ª Etapa: Afixando a agulha
Use sempre uma agulha estéril nova para cada aplicação. Isso ajuda a prevenir contaminação e possíveis entupimentos da agulha.
As agulhas mostradas nas figuras são ilustrativas.
Limpe o lacre de borracha com álcool.
- Retire o lacre protetor da agulha nova.
- Alinhe a agulha com a caneta ainda com sua tampa protetora e mantenha-a em linha reta até que se consiga fixá-la (rosqueie ou empurre dependendo do tipo de agulha).
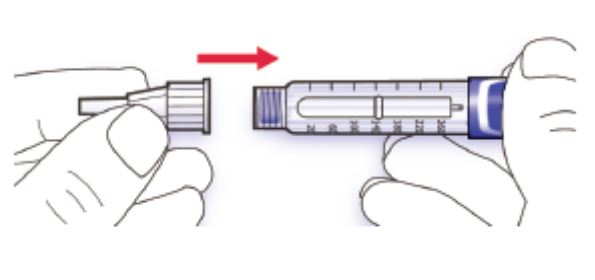
- Se a agulha não for mantida reta enquanto você a fixa, ela pode danificar o lacre de borracha e provocar vazamento ou quebrar a agulha.
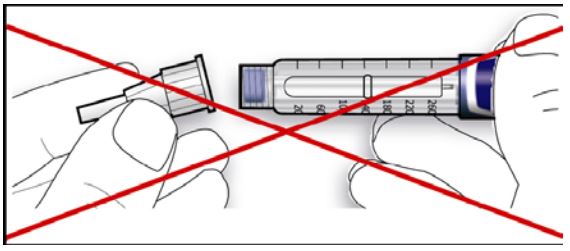
3ª Etapa: Teste de segurança
Sempre faça o teste de segurança antes de cada injeção. Isto assegura que você obtenha uma dose precisa, pois garante que a caneta e a agulha estão funcionando adequadamente e remove bolhas de ar.
- Selecione a dose de 2 unidades girando o seletor de dosagem.
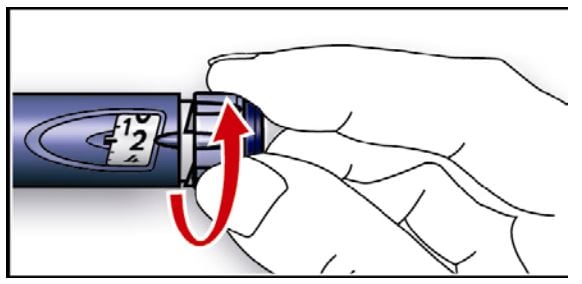
- Retire a tampa externa da agulha e guarde-a para remover a agulha usada após a aplicação. Retire a tampa interna da agulha e descarte-a.
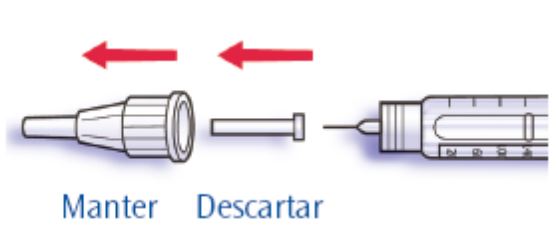
- Segure a caneta com a agulha apontando para cima.
- Bata levemente no reservatório de insulina, assim qualquer bolha subirá até a agulha.
- Pressione o botão da injeção todo para dentro. Verifique se a insulina sai da ponta da agulha.
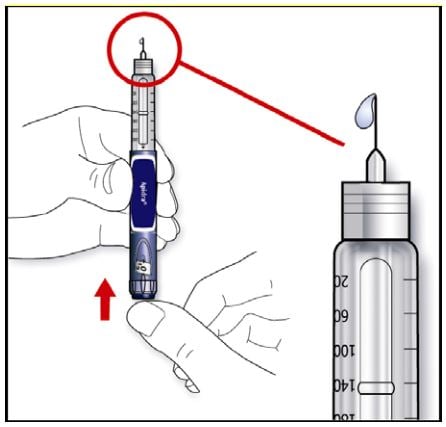
Pode ser necessário fazer o teste de segurança diversas vezes antes da insulina começar a aparecer.
Se a insulina não aparecer, verifique se há bolhas de ar e repita o teste de segurança mais 2 vezes para removê-las.
Se ainda assim a insulina não aparecer, pode ser que a agulha esteja entupida. Substitua a agulha e tente novamente.
Se após a troca da agulha ainda não começar a aparecer insulina, pode ser que a caneta SoloStar esteja danificada. Não utilize mais esta SoloStar.
4ª Etapa: Seleção da dose
Você pode selecionar as dosagens de 1 em 1 unidade, sendo o mínimo 1 unidade e o máximo 80 unidades. Se você precisar de uma dosagem superior a 80, será necessário aplicar duas ou mais injeções.
- Verifique que a janela indicadora de dosagem mostra “0” após o teste de segurança.
- Selecione a sua dosagem (no exemplo a seguir, a dosagem selecionada foi 30 unidades). Se você ajustar uma dose maior que a necessária, você pode retornar à dosagem correta movimentando o seletor de dosagem.
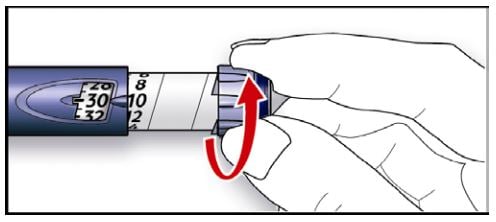
Não empurre o botão enquanto o gira, pois a insulina pode ser expelida.
Não gire o botão seletor da dosagem além do número de unidades à esquerda na caneta. Não force o botão seletor para girá-lo. Neste caso, você pode injetar o que resta na caneta e completar sua dosagem com uma nova SoloStar ou usar uma nova SoloStar para sua dosagem total.
5ª Etapa: Injetando a dose
- Use o método de aplicação conforme a orientação de seu médico
- Introduza a agulha na pele.
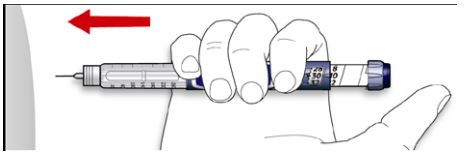
- Injete a dose pressionando o botão de injeção até o final. O número na janela indicadora de dosagem retornará a “0” assim que a injeção for finalizada.
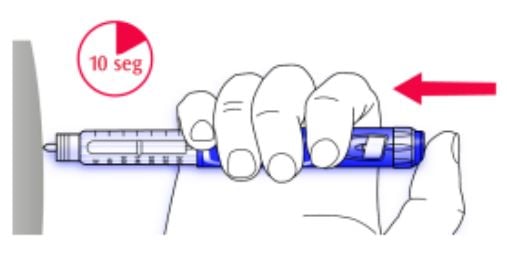
- Mantenha o botão de injeção pressionado até o final. Lentamente conte até 10 antes de retirar a agulha da pele. Isto garantirá que toda a dosagem seja liberada.
O êmbolo da caneta se moverá a cada aplicação. O êmbolo chegará ao final do carpule quando todas as 300 unidades de insulina forem utilizadas.
6ª Etapa: Remoção e descarte da agulha
Sempre remova a agulha após cada aplicação e guarde a SoloStar sem nenhuma agulha afixada. Isto ajuda a prevenir contaminação e/ou infecção e entrada de ar no reservatório da insulina e vazamento de insulina, o que pode provocar imprecisão da dosagem.
- Recoloque a tampa externa na agulha e use-a para desrosquear a agulha da caneta. Para reduzir o risco de se machucar acidentalmente com a agulha, nunca recoloque a tampa interna da agulha.
Se a aplicação for feita por outra pessoa, ou se você for aplicar em outra pessoa, deve-se ter cuidado especial ao remover e descartar a agulha. Siga as medidas de segurança recomendadas para remoção e descarte das agulhas (em caso de dúvida, consulte o seu médico) a fim de reduzir o risco de se machucar acidentalmente e de transmissão de doenças infecciosas.
- Descarte a agulha de forma segura, conforme orientado por seu médico.
- Sempre coloque a tampa de volta na caneta e então guarde-a até a próxima aplicação.
Instruções para Conservação
Verifique a bula da insulina para informações sobre os cuidados de conservação da SoloStar.
Se a sua SoloStar estiver sob refrigeração, retire-a da refrigeração de 1 a 2 horas antes da injeção para que ela atinja a temperatura ambiente. A injeção de insulina fria é mais dolorosa.
Mantenha sua SoloStar fora do alcance das crianças.
Conservar em local frio (temperatura entre 2° e 8°C) até o primeiro uso. Não congelar. Evitar contato direto do produto com o compartimento do congelador ou pacotes congelados.
Após a retirada da SoloStar do ambiente frio para uso ou para reserva, você poderá utilizá-la por 28 dias. Durante esse período, a caneta pode ser armazenada seguramente à temperatura ambiente (temperatura até 25°C) e não deve ser armazenada em geladeira. Não utilize a caneta após esse período.
Não utilize SoloStar após a data de vencimento gravada no rótulo da caneta ou no cartucho.
Proteja SoloStar da luz e do calor.
Descarte sua SoloStar como orientado pelas autoridades sanitárias em local apropriado.
Manutenção
Proteja sua caneta do pó e sujeira.
Você pode limpar a parte externa da sua SoloStar esfregando-a com um pano úmido.
Não molhe, lave ou lubrifique a caneta, pois pode danificá-la.
Sua caneta SoloStar foi desenvolvida para funcionar precisa e seguramente. Ela deve ser manuseada com cuidado. Evite situações em que a SoloStar possa ser danificada. Se estiver preocupado com a possibilidade da caneta estar danificada, descarte-a e use uma nova.
Precauções
Em decorrência da curta duração de ação de Apidra SoloStar, os pacientes diabéticos também necessitam de uma insulina de ação mais prolongada ou de uma terapia com bomba de infusão de insulina para manter o controle adequado da glicose.
Qualquer alteração da insulina deve ser feita com cautela e apenas sob supervisão médica.
As alterações na potência da insulina, no fabricante, no tipo (p. ex., regular, NPH, análogos), na espécie (animal, humana) ou no modo de fabricação (DNA recombinante versus insulina de origem animal) podem resultar na necessidade de alteração da dose.
O tratamento antidiabético oral concomitante pode necessitar ser ajustado.
As necessidades de insulina podem ser alteradas durante condições intercorrentes, como doenças, distúrbios emocionais ou estresse.
Hipoglicemia (diminuição da taxa de açúcar no sangue)
O tempo de ocorrência de hipoglicemia depende do perfil de ação das insulinas usadas e pode, portanto, variar quando o esquema terapêutico é alterado.
Em determinadas condições, como ocorre com todas as insulinas, os sintomas de alerta de hipoglicemia podem ser alterados, menos pronunciados ou ausentes, por exemplo:
- Se o controle da quantidade de glicose no sangue estiver consideravelmente melhor;
- Se a hipoglicemia estiver se desenvolvendo gradativamente;
- Se você for idoso;
- Quando uma neuropatia autônoma (doença que afeta um ou vários nervos) estiver presente;
- Se você tem uma longa história de diabetes;
- Se você está recebendo tratamento concomitante com alguns medicamentos.
Essas situações podem resultar em hipoglicemia severa (e, possivelmente, perda de consciência) antes que você tenha consciência da ocorrência da hipoglicemia.
Bomba de infusão subcutânea contínua
O mau funcionamento da bomba de insulina, do cateter de infusão ou erros de manipulação podem rapidamente levar o paciente a hiperglicemia, cetose e cetoacidose diabética. A rápida identificação e correção da causa da hiperglicemia, cetose ou cetoacidose diabética é necessária.
Injeção subcutânea temporária com Apidra SoloStar pode ser necessária. Pacientes que utilizam a terapia com bomba de infusão subcutânea contínua de insulina devem ser treinados a administrar insulina por injeção e ter um sistema de administração de insulina alternativo disponível.
A monitoração da glicose no sangue é recomendada em todos os pacientes diabéticos.
Reações Adversas
As reações adversas observadas foram as conhecidas para essa classe farmacológica e, consequentemente, comuns às insulinas.
Reação muito comum (ocorre em 10% ou mais dos pacientes que utilizam este medicamento):
Hipoglicemia em geral, a reação adversa mais frequente da terapia com insulina, pode ocorrer se a dose de insulina for muito alta em relação à necessidade de insulina.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento):
Alergia local em pacientes ocorre eventualmente como vermelhidão, inchaço e coceira no local da administração da insulina. Essas reações geralmente desaparecem em alguns dias ou poucas semanas. Em alguns casos, essas reações podem estar relacionadas a fatores diferentes da insulina, como irritantes em agentes de limpeza da pele ou técnica inadequada de administração.
Reações incomuns (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
Reações alérgicas sistêmicas. Essas reações à insulina (incluindo a insulina glulisina) podem, por exemplo, estar associadas à erupção cutânea (incluindo prurido) no corpo todo, falta de ar, chiados, redução da pressão arterial, pulso rápido ou sudorese. Casos severos de alergia generalizada, incluindo reação anafilática (reação alérgica grave e imediata), podem ser potencialmente fatais.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
Como ocorre com qualquer terapia com insulina, pode ocorrer lipodistrofia (alteração da distribuição da gordura no local da injeção) e atraso na absorção da insulina. O rodízio contínuo do local de injeção ou infusão na região de administração pode ajudar a reduzir ou prevenir essas reações.
Misturas acidentais entre insulina glulisina e outras insulinas, particularmente insulinas de ação prolongada, foram relatadas. De modo a evitar erros de medicação entre insulina glulisina e outras insulinas você deve sempre verificar o rótulo da insulina antes de cada injeção.
Informe ao seu médico ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também a empresa através do seu serviço de atendimento.
População Especial
Gravidez
Não existem estudos clínicos bem controlados do uso de Apidra SoloStar em mulheres grávidas.
Uma quantidade limitada de dados em mulheres grávidas (menos de 300 resultados reportados) expostas à insulina glulisina indicou que não há problemas de segurança no uso da insulina glulisina durante a gravidez, no feto e nos recém nascidos.
É primordial às pacientes diabéticas ou com histórico de diabetes durante a gravidez, a manutenção de um bom controle metabólico antes da concepção e durante toda a gravidez.
As necessidades de insulina podem diminuir durante o primeiro trimestre da gravidez, geralmente aumentam durante o segundo e o terceiro trimestres e rapidamente diminuem após o parto.
Seu médico deverá realizar um monitoramento rigoroso do controle da quantidade de açúcar no seu sangue.
As pacientes diabéticas devem informar seus médicos se estiverem grávidas ou planejando engravidar.
Amamentação
Não se sabe ao certo se Apidra SoloStar é eliminada no leite materno.
A dose de insulina e a dieta podem precisar de ajuste em mulheres que estejam amamentando.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Pacientes idosos
A hipoglicemia pode ser difícil de ser reconhecida em idosos.
Crianças
Apidra SoloStar pode ser administrada em crianças com idade igual ou superior a 4 anos. A administração de Apidra SoloStar em crianças menores de 4 anos ainda não foi estudada.
Pacientes com insuficiência dos rins
As necessidades de Apidra SoloStar, como ocorre com todas as insulinas, podem ser menores caso você apresente insuficiência dos rins.
Pacientes com insuficiência do fígado
Caso você tenha insuficiência do fígado, as necessidades de insulina podem ser menores devido a uma menor capacidade de gliconeogênese (produção de glicose pelo fígado) e redução do metabolismo de insulina.
Alterações na capacidade de dirigir veículos e operar máquinas
Sua capacidade de concentração e reação pode estar prejudicada como resultado da hipoglicemia ou hiperglicemia (aumento da taxa de açúcar no sangue) ou, por exemplo, em decorrência de comprometimento visual. Isso pode constituir um risco em situações em que essas habilidades são de especial importância (p. ex., dirigir um carro ou operar máquinas).
Deve-se tomar precauções para evitar a hipoglicemia durante a condução de veículos. Isso é particularmente importante caso você apresente nível de consciência diminuído ou ausente dos sintomas de alerta da hipoglicemia ou se você apresenta episódios frequentes de hipoglicemia. Deve-se considerar se é aconselhável dirigir veículos ou operar máquinas nessas circunstâncias.
Composição
Apidra SoloStar 100 UI/mL contém:
3,49 mg de insulina glulisina equivalente a 100 UI de insulina humana.
Excipientes: metacresol, trometamol, cloreto de sódio, polissorbato 20, hidróxido de sódio, ácido clorídrico concentrado e água para injetáveis.
Superdosagem
Em caso de superdose acidental, procure imediatamente atendimento médico de emergência.
Sintomas
Hipoglicemia pode ocorrer em decorrência de um excesso de insulina em relação à ingestão de alimentos, gasto de energia ou ambos.
Caso tenha sido administrada uma dose muito alta de ApidraSoloStar, poderá ocorrer hipoglicemia. Em geral, para evitar hipoglicemia deve-se ingerir uma quantidade maior de alimentos e monitorar o nível de glicose no sangue.
Tratamento
Os episódios leves/moderados de hipoglicemia podem, em geral, ser tratados com carboidratos orais. Podem ser necessários ajustes na dose do medicamento, nos padrões de refeição ou na atividade física.
Os episódios severos com coma, convulsão ou comprometimento do sistema nervoso podem ser tratados com glucagon intramuscular/subcutâneo ou glicose intravenosa concentrada. Pode ser necessária uma ingestão contínua de carboidratos e observação porque a hipoglicemia pode retornar após a recuperação clínica aparente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Várias substâncias afetam o metabolismo da glicose e podem exigir ajuste na dose da Insulina humana.
As substâncias que podem intensificar o efeito hipoglicemiante e aumentar a susceptibilidade à hipoglicemia são
Agentes hipoglicemiantes orais, inibidores da ECA, disopiramida, fibratos, fluoxetina, inibidores da MAO, pentoxifilina, propoxifeno, salicilatos e antibióticos sulfonamida.
As substâncias que podem reduzir o efeito hipoglicemiante são
Corticosteroides, danazol, diazóxido, diuréticos, glucagon, isoniazida, estrogênios e progestogênios (p. ex., em contraceptivos orais), derivados de fenotiazina, somatropina, agentes simpatomiméticos (p. ex., epinefrina, salbutamol, terbutalina), hormônios tireoideanos, inibidores da protease e medicamentos antipsicóticos atípicos (p. ex., olanzapina e clozapina).
Betabloqueadores, clonidina ou sais de lítio podem tanto potencializar quanto enfraquecer o efeito hipoglicemiante da Insulina (substância ativa). A pentamidina pode causar hipoglicemia, que pode ocasionalmente ser seguida de hiperglicemia.
Além disso, sob a influência de medicamentos simpatolíticos, como betabloqueadores, clonidina, guanetidina e reserpina, os sinais de contrarregulação adrenérgica podem estar reduzidos ou ausentes.
Medicamento - substância química
Nicotina
O efeito do fumo na farmacocinética e farmacodinâmica de Insulina (substância ativa) não foi estudado.
Medicamento - exame laboratorial
Não há dados disponíveis até o momento sobre a interferência de Insulina (substância ativa) glulisina em exames laboratoriais.
Interação Alimentícia
Álcool
Pode tanto potencializar quanto enfraquecer o efeito de diminuição da glicose no sangue, decorrente da Insulina (substância ativa).
Ação da Substância
Resultados de eficácia
Estudos clínicos
A eficácia e a segurança de Insulina (substância ativa) foram estudadas em pacientes adultos com diabetes Tipo 1 e Tipo 2 (n = 2.408). O parâmetro primário de eficácia foi o controle glicêmico, medido pela hemoglobina glicada (GHb) e expresso como equivalentes de hemoglobina A1c (A1C).
Diabetes Tipo 1 – Pacientes adultos
Um estudo controlado por medicamento ativo, randomizado, aberto e de 26 semanas (n = 672) foi conduzido em pacientes com diabetes Tipo 1 para avaliar a segurança e a eficácia de Insulina (substância ativa) em comparação à Insulina (substância ativa) lispro por via SC em até 15 minutos antes de uma refeição. A Insulina (substância ativa) glargina foi administrada uma vez por dia à noite como Insulina (substância ativa) basal. Antes do início do estudo, houve um período de introdução de 4 semanas com a combinação da Insulina (substância ativa) lispro e da Insulina (substância ativa) glargina seguido da randomização.
O controle glicêmico e as taxas de hipoglicemia que necessitaram de intervenção de terceiros foram equivalentes entre os dois regimes terapêuticos. O número de administrações diárias de Insulina (substância ativa) e as doses diárias totais de Insulina (substância ativa) e Insulina (substância ativa) lispro foram semelhantes. Foi observada diminuição da A1C em pacientes tratados com Insulina (substância ativa) sem aumento da dose basal de Insulina (substância ativa) (vide Tabela 1).
Tabela 1: Diabetes Mellitus Tipo 1 – Pacientes adultos:
| Duração do tratamento | 26 semanas | |
| Tratamento em combinação com as seguintes Insulinas (substância ativa) basais | Insulina (substância ativa) glargina | |
| APIDRA | Insulina (substância ativa) lispro | |
| Número de indivíduos tratados | 339 | 333 |
| A1C (%) | ||
| Média ao final do estudo | 7,46 | 7,45 |
| Alteração média ajustada em relação à Fase Basal | -0,14 | -0,14 |
| APIDRA - Insulina (substância ativa) lispro | 0,00 | |
| IC de 95% para diferença entre os tratamentos | (-0,09; 0,10) | |
| Dose da Insulina (substância ativa) basal (UI/dia) | ||
| Média ao final do estudo | 24,16 | 26,43 |
| Alteração média ajustada em relação à Fase Basal | 0,12 | 1,82 |
| Dose de Insulina (substância ativa) de curta duração (UI/dia) | ||
| Média ao final do estudo | 29,03 | 30,12 |
| Alteração média ajustada em relação à Fase Basal | -1,07 | -0,81 |
| Hipoglicemia (eventos/mês/paciente)* | 0,02 | 0,02 |
| Número médio de administrações de Insulina (substância ativa) ação curta por dia | 3,36 | 3,42 |
* Eventos que necessitaram de assistência de terceiros nos últimos 3 meses do estudo.
Diabetes Tipo 1 – Pacientes pediátricos
Um estudo clínico de Fase III controlado por medicamento ativo, aberto e com duração de 26 semanas (n = 572) avaliou a eficácia e segurança da Insulina glulisina em crianças e adolescentes com diabetes mellitus Tipo 1, em comparação com a Insulina (substância ativa) lispro, ambas administradas por via subcutânea pelo menos 15 minutos antes de uma refeição.
Como Insulina (substância ativa) basal, os pacientes receberam Insulina (substância ativa) glargina uma vez ao dia (à noite) ou NPH (protamina neutra de Hagedorn) duas vezes ao dia (de manhã e à noite). O estudo foi constituído por um período de introdução de 4 semanas, no qual os pacientes receberam NPH ou Insulina (substância ativa) glargina combinada com Insulina (substância ativa) lispro, seguido de uma fase de tratamento de 26 semanas.
O controle glicêmico, as taxas de hipoglicemia que necessitaram de intervenções de terceiros, e a frequência de episódios de hipoglicemia relatados como eventos adversos graves, foram comparáveis nos dois regimes de tratamento. Os pacientes que receberam a Insulina glulisina necessitaram de aumentos significativamente menores das doses diárias de Insulina (substância ativa) basal, de ação rápida e total, da fase basal até o desfecho, para alcançar um controle glicêmico similar aos pacientes que receberam a Insulina (substância ativa) lispro (vide Tabela 2).
Tabela 2: Diabetes Mellitus Tipo 1 – Pacientes pediátricos:
| Duração do tratamento | 26 semanas | |
| Tratamento em combinação com | NPH ou Insulina (substância ativa) glargina | |
| APIDRA | Insulina (substância ativa) lispro | |
| HbA1c (%) | ||
| Número de pacientes | 271 | 291 |
| Média na Fase Basal | 8,20 | 8,17 |
| Alteração média ajustada em relação à Fase Basal | 0,10 | 0,16 |
| APIDRA - Insulina (substância ativa) lispro | -0,06 | |
| IC de 95% para diferença entre os tratamentos | (-0,24; 0,12) | |
| Dose de Insulina (substância ativa) basal (UI/dia) | ||
| Média ao final do estudo | 28,41 | 28,86 |
| Alteração média ajustada em relação à Fase Basal | 1,09 | 2,22 |
| Dose de Insulina (substância ativa) de ação rápida (UI/dia) | ||
| Média ao final do estudo | 25,48 | 26,97 |
| Alteração média ajustada em relação à Fase Basal | 1,36 | 2,71 |
| Porcentagem de pacientes com uma média de injeções de Insulina (substância ativa) de ação rápida por dia ? 3 | 77,0 | 80,3 |
Diabetes Tipo 2 – Pacientes adultos
Um estudo controlado por medicamento ativo, randomizado, aberto e de 26 semanas de duração (n = 876) foi conduzido em pacientes com diabetes Tipo 2 tratados com Insulina (substância ativa) para avaliar a segurança e a eficácia de Insulina (substância ativa) administrada em até 15 minutos antes de uma refeição em comparação à Insulina humana regular administrada 30 a 45 minutos antes de uma refeição.
A Insulina humana NPH foi administrada duas vezes por dia como Insulina (substância ativa) basal. Todos os pacientes participaram de um período de introdução de 4 semanas com a combinação da Insulina humana regular com a Insulina humana NPH. O índice de massa corpórea (IMC) médio dos pacientes foi de 34,55 kg/m².
No momento da randomização, 58% dos pacientes estavam recebendo um agente antidiabético oral e foram orientados a continuar o uso na mesma dose. A maioria dos pacientes (79%) misturou uma Insulina (substância ativa) de curta duração com a Insulina humana NPH imediatamente antes da administração. Foi observada uma redução maior em relação à A1C da Fase Basal no grupo recebendo tratamento com Insulina (substância ativa).
Ao final do período de tratamento, os níveis de glicemia pós-prandial no grupo recebendo tratamento com Insulina (substância ativa) foram menores do que no grupo Insulina humana regular.
As taxas de hipoglicemia, que necessitaram de intervenção de terceiros, foram equivalentes entre os dois regimes terapêuticos. Não foram observadas diferenças entre os grupos Insulina (substância ativa) e Insulina humana regular no número de administrações diárias ou doses de Insulina (substância ativa) basal ou de curta duração. (vide Tabela 3).
Tabela 3: Diabetes Mellitus Tipo 2 – Pacientes adultos:
| Duração do tratamento | 26 semanas | |
| Tratamento em associação com as seguintes Insulinas (substância ativa) basais | Insulina humana NPH | |
| APIDRA | Insulina humana regular | |
| A1C (%) | ||
| Número de pacientes | 435 | 441 |
| Média ao final do estudo | 7,11 | 7,22 |
| Alteração média ajustada em relação à Fase Basal | -0,46 | -0,30 |
| APIDRA - Insulina humana regular | -0,16 | |
| IC de 95% para diferença entre os tratamentos | (-0,26; -0,05) | |
| Dose de Insulina (substância ativa) basal (UI/dia) | ||
| Média ao final do estudo | 65,34 | 63,05 |
| Alteração média ajustada em relação à Fase Basal | 5,73 | 6,03 |
| Dose de Insulina (substância ativa) de ação rápida (UI/dia) | ||
| Média ao final do estudo | 35,99 | 36,16 |
| Alteração média ajustada em relação à Fase Basal | 3,69 | 5,00 |
| Hipoglicemia (eventos/mês/paciente)* | 0,00 | 0,00 |
| Número médio de administrações de Insulina (substância ativa) de curta duração por dia | 2,27 | 2,24 |
Administração pré e pós-refeição (Diabetes Tipo 1)
Um estudo controlado por medicamento ativo, randomizado, aberto e de 12 semanas de duração (n = 860) foi conduzido em pacientes com diabetes Tipo 1 para avaliar a segurança e a eficácia de Insulina (substância ativa) administrada em diferentes pontos de tempo em relação a uma refeição. Insulina (substância ativa) foi administrada por via SC em até 15 minutos antes de uma refeição ou imediatamente após uma refeição e a Insulina humana regular foi administrada por via SC 30 a 45 minutos antes de uma refeição.
As comparações realizadas neste estudo foram Insulina (substância ativa) pré-refeição em comparação à Insulina humana regular, Insulina (substância ativa) pós-refeição em comparação à Insulina humana regular e Insulina (substância ativa) pós-refeição em comparação à Insulina (substância ativa) pré-refeição.
A Insulina (substância ativa) glargina foi administrada uma vez por dia ao deitar como Insulina (substância ativa) basal. Antes do início do estudo, houve um período de introdução de 4 semanas com a combinação de Insulina humana regular e Insulina (substância ativa) glargina seguido da randomização. O controle glicêmico e as taxas de hipoglicemia que necessitaram de intervenção de terceiros foram equivalentes para os esquemas terapêuticos.
Foram observadas reduções significativas da A1C em relação à Fase Basal em todos os três esquemas terapêuticos. Não foram observadas alterações em relação à Fase Basal entre os tratamentos no número diário total de administrações de Insulina (substância ativa). Foi observado um aumento da dose diária de Insulina (substância ativa) de curta duração com a Insulina humana regular (vide Tabela 4).
Tabela 4: Diabetes Mellitus Tipo 1 – Pacientes adultos:
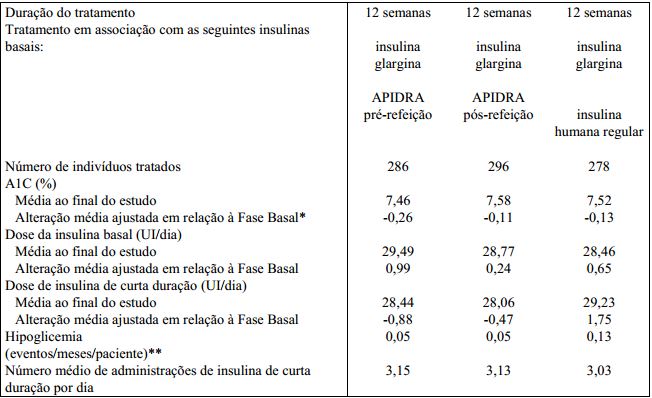 * Diferença entre os tratamentos da alteração média ajustada em relação à Fase Basal (IC de 98,33% para diferença entre os tratamentos): APIDRA pré-refeição versus Insulina humana regular - 0,13 (-0,26; 0,01); APIDRA pós-refeição versus Insulina humana regular 0,02 (-0,11; 0,16); APIDRA pós-refeição versus pré-refeição 0,15 (0,02; 0,29).
* Diferença entre os tratamentos da alteração média ajustada em relação à Fase Basal (IC de 98,33% para diferença entre os tratamentos): APIDRA pré-refeição versus Insulina humana regular - 0,13 (-0,26; 0,01); APIDRA pós-refeição versus Insulina humana regular 0,02 (-0,11; 0,16); APIDRA pós-refeição versus pré-refeição 0,15 (0,02; 0,29).
** Eventos que necessitaram de assistência de terceiros durante toda a fase de tratamento.
Infusão Subcutânea Contínua de Insulina (substância ativa) (ISCI) (Diabetes Tipo 1)
Para avaliar o uso de Insulina (substância ativa) para administração por bomba externa, um estudo randomizado, controlado por medicamento ativo e aberto de 12 semanas de duração (Insulina (substância ativa) versus Insulina (substância ativa) aspart) foi realizado em pacientes com diabetes Tipo 1 (n = 59).
Observou-se uma taxa mensal baixa de oclusão de cateter nos dois grupos de tratamento (Insulina (substância ativa): 0,08 oclusões/mês; Insulina (substância ativa) aspart: 0,15 oclusões/mês). Observou-se incidência semelhante de reações no local da infusão com Insulina (substância ativa) (n = 3/29; 10,3%) e Insulina (substância ativa) aspart (n = 4/30; 13,3%). Insulina (substância ativa) foi estudada nas seguintes bombas e equipamentos de infusão: Disetronic H-Tron plus V100 e D-Tron TM com cateteres Disetronic (Rapid, Rapid C e D e Tender); MiniMed Modelos 506, 507, 507c e 508 com catéteres MiniMed (Sof-set Ultimate QR e Quick-set).
Características farmacológicas
Propriedades farmacodinâmicas
Mecanismo de ação
A atividade principal das Insulinas (substância ativa) e dos análogos de Insulina (substância ativa), incluindo a Insulina glulisina, é a regulação do metabolismo de glicose. As Insulinas (substância ativa) diminuem os níveis de glicemia estimulando a captação periférica de glicose por músculos esqueléticos e gordura e inibindo a produção de glicose hepática. As Insulinas (substância ativa) inibem a lipólise nos adipócitos, inibem a proteólise e aumentam a síntese de proteínas.
Após a administração subcutânea, o efeito de Insulina (substância ativa) apresenta início de ação mais rápido e duração mais curta do que a Insulina humana regular.
As atividades hipoglicemiantes de Insulina (substância ativa) e da Insulina humana regular são equipotentes quando administradas por via intravenosa. Dois estudos de fase I avaliaram a administração intravenosa de Insulina (substância ativa). Nestes estudos este medicamento demonstrou ser seguro e bem tolerado.
Os estudos em voluntários saudáveis e pacientes diabéticos demonstraram que Insulina (substância ativa) apresenta início de ação mais rápido e duração de atividade mais curta do que a Insulina humana regular quando administrada por via subcutânea.
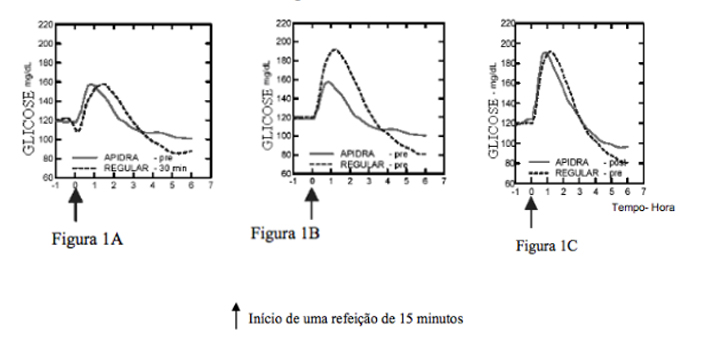
Em um estudo em pacientes com diabetes Tipo 1 (n = 20), os perfis de redução de glicose de Insulina (substância ativa) e da Insulina humana regular, na dose de 0,15 UI/kg, foram avaliados em vários pontos de tempo em relação a uma refeição padrão. (vide Figura 1).
Figura 1 Efeito hipoglicemiante por 6 horas. Insulina (substância ativa) administrada 2 minutos (Insulina-pré) antes do início de uma refeição em comparação à Insulina humana regular administrada 30 minutos (Regular - 30 min.) antes do início da refeição (Figura 1A) e em comparação à Insulina humana regular (Regular-pré) administrada 2 minutos antes de uma refeição (Figura 1B). Insulina (substância ativa) administrada 15 minutos (Insulina-pós) após o início de uma refeição em comparação à Insulina humana regular (Regular-pré) administrada 2 minutos antes de uma refeição (Figura 1C). No eixo X, zero (0) é o início de uma refeição de 15 minutos:
Propriedades farmacocinéticas
Absorção e biodisponibilidade
Os perfis farmacocinéticos em voluntários saudáveis e pacientes diabéticos (Tipo 1 ou 2) demonstraram que a absorção da Insulina glulisina foi cerca de 2 vezes mais rápida com concentração máxima aproximadamente 2 vezes maior do que a da Insulina humana regular.
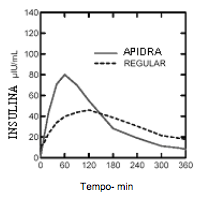
Em um estudo em pacientes com diabetes Tipo 1 (n=20) após a administração SC de 0,15 UI/kg, o Tmáx foi de 55 minutos e a Cmáx de 82 ?UI/mL para Insulina glulisina em comparação a Tmáx de 82 minutos e Cmáx de 46 ?UI/mL para Insulina (substância ativa) humana regular. O tempo médio de residência da Insulina glulisina foi menor (98 min) do que o da Insulina humana regular (161 minutos) (vide Figura 2).
Figura 2 Perfil farmacocinético da Insulina glulisina e da Insulina humana regular em pacientes com diabetes Tipo 1 após uma dose de 0,15 UI/kg:
Quando Insulina (substância ativa) foi administrada por via SC em diferentes regiões do corpo, as curvas de concentração versus tempo foram semelhantes com uma absorção um pouco mais rápida quando administrada no abdome do que no músculo deltoide ou na coxa. A biodisponibilidade absoluta da Insulina glulisina após administração SC é de cerca de 70%, independentemente da região de administração (abdome 73%, deltoide 71%, coxa 68%).
Distribuição e eliminação
A distribuição e a eliminação da Insulina glulisina e da Insulina humana regular após a administração intravenosa são semelhantes com volumes de distribuição de 13 L e 21 L e meias-vidas de 13 e 17 minutos, respectivamente.
Após a administração subcutânea, a Insulina glulisina é eliminada mais rapidamente do que a Insulina humana regular com meia-vida aparente de 42 minutos em comparação a 86 minutos.
Raça e Sexo
Não estão disponíveis informações sobre os efeitos da raça e do sexo sobre a farmacocinética de Insulina (substância ativa). No entanto, em estudos clínicos Fase III em adultos (n=2.408), as análises de subgrupo por sexo não mostraram diferenças de segurança e eficácia entre Insulina (substância ativa) e outras formulações de Insulina (substância ativa) de curta duração.
Pacientes pediátricos
As propriedades farmacocinéticas e farmacodinâmicas de Insulina (substância ativa) e da Insulina humana regular foram avaliadas em um estudo conduzido em pacientes pediátricos com diabetes Tipo 1 ([crianças de 7 - 11 anos, n = 10] e adolescentes [ 12 - 16 anos, n = 10]). As diferenças relativas na farmacocinética e na farmacodinâmica entre Insulina (substância ativa) e Insulina humana regular em pacientes pediátricos com diabetes Tipo 1 foram semelhantes àquelas observadas em adultos saudáveis e adultos com diabetes Tipo 1.
Insuficiência hepática
O efeito da insuficiência hepática sobre a farmacocinética de Insulina (substância ativa) não foi estudado. No entanto, alguns estudos com Insulina humana demonstraram aumento dos níveis circulantes de Insulina (substância ativa) em pacientes com insuficiência hepática.
Obesidade
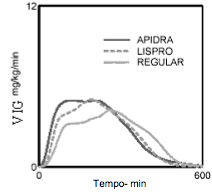
O início de ação mais rápido e a duração da atividade mais curta de Insulina (substância ativa) e da Insulina (substância ativa) lispro em comparação à Insulina humana regular foram mantidos em uma população obesa não diabética. A manutenção do início de ação rápida com a Insulina glulisina foi melhor do que com a Insulina (substância ativa) lispro (vide Figura 3).
Figura 3 Velocidades de infusão da glicose (VIG) após administração SC de 0,3 UI/kg de Insulina (substância ativa), Insulina (substância ativa) lispro ou Insulina humana regular em uma população obesa:
Insuficiência renal
Os estudos com Insulina humana demonstraram aumento dos níveis circulantes de Insulina (substância ativa) em pacientes com insuficiência renal. Em um estudo realizado em 24 indivíduos não diabéticos com uma ampla variedade de função renal (CrCl > 80 mL/min; 30-50 mL/min; <30 mL/min), as propriedades farmacocinéticas de Insulina (substância ativa) foram geralmente mantidas.
Gravidez
O efeito da gravidez sobre a farmacocinética e a farmacodinâmica de Insulina (substância ativa) não foi estudado.
Dados pré-clínicos de segurança
Carcinogênese
Ainda não foram realizados estudos padrão de carcinogenicidade de 2 anos de duração em animais para avaliar o potencial carcinogênico de Insulina (substância ativa).
Em ratos Sprague Dawley, foi realizado um estudo de toxicidade de dose repetida de 12 meses com Insulina glulisina nas doses de 2,5; 5; 20 ou 50 UI/kg duas vezes por dia (dose que resulta em uma exposição equivalente de aproximadamente 26, 54, 258, 662 vezes a Cmáx humana na dose média em seres humanos, respectivamente).
Houve uma incidência não dose dependente maior de tumores da glândula mamária em ratas tratadas com Insulina (substância ativa) em comparação aos controles não tratados.
A incidência de tumores mamários com Insulina (substância ativa) e Insulina humana regular foi semelhante. A importância desses achados para humanos ainda é desconhecida.
Nesse estudo, os efeitos da Insulina glulisina sobre a proliferação celular nas glândulas mamárias foram avaliados por imunohistoquímica para Ki-67. Não houve diferença significativa de proliferação das células mamárias entre a Insulina glulisina, a Insulina humana regular e os grupos controle.
Mutagênese
Insulina (substância ativa) não foi mutagênica nos seguintes testes: teste de Ames, teste in vitro de aberração cromossômica em mamíferos em células V79 e teste in vivo de aberração cromossômica em mamíferos (teste de micronúcleo de eritrócitos).
Teratogenicidade
Foram realizados estudos de teratologia e reprodução por via SC com Insulina glulisina em ratos e coelhos utilizando Insulina humana regular como agente comparador. O medicamento foi administrado a ratas durante toda a gestação até 10 UI/kg uma vez por dia (dose que resulta em uma exposição equivalente a aproximadamente 50 vezes a Cmáx humana na dose média em humanos). A Insulina glulisina não apresentou efeitos tóxicos sobre o desenvolvimento embrio-fetal em ratos.
O medicamento foi administrado a coelhas durante toda a gestação até 1,5 UI/kg/dia. Foram observados efeitos adversos sobre o desenvolvimento embrio-fetal apenas em doses tóxicas maternas indutoras de hipoglicemia. Foi observada maior incidência de perdas pós implantação e defeitos esqueléticos na dose de 1,5 UI/kg uma vez por dia (dose que resulta em uma exposição equivalente a aproximadamente 25 vezes a Cmáx humana na dose média em humanos) que também causou mortalidade em fêmeas.
Foi observada incidência um pouco aumentada de perdas pós implantação no nível de dose mais baixa seguinte de 0,5 UI/kg uma vez por dia (dose que resulta em uma exposição equivalente a aproximadamente 5 vezes a Cmáx humana na dose média em humanos) que também foi associada a hipoglicemia severa, mas não houve defeitos nessa dose. Não foram observados efeitos em coelhos na dose de 0,25 UI/kg uma vez por dia (dose que resulta em uma exposição equivalente a aproximadamente 3 vezes a Cmáx humana na dose média em humanos).
Os efeitos de Insulina (substância ativa) não diferiram daqueles observados com a Insulina humana regular subcutânea nas mesmas doses e foram atribuídos a efeitos secundários da hipoglicemia materna.
Comprometimento da fertilidade
Em estudos de fertilidade em ratos machos e fêmeas nas doses SC até 10 UI/kg uma vez por dia (dose que resulta em uma exposição equivalente a aproximadamente 50 vezes a Cmáx humana na dose média em humanos), não foram observados efeitos adversos sobre a fertilidade masculina e feminina ou no desempenho reprodutivo geral dos animais.
Cuidados de Armazenamento
Apidra SoloStar (fechada) deve ser mantida em sua embalagem original, sob refrigeração em temperatura entre 2 e 8°C e protegida da luz.
Não guardar em freezer. Não congelar. Descartar em caso de congelamento.
Apidra SoloStar aberta (em uso)
Após aberta, Apidra SoloStar deve ser utilizada em até 28 dias (4 semanas). Durante esse período, a caneta pode ser armazenada à temperatura ambiente (temperatura até 25°C), protegida da luz e calor diretos, e não deve ser armazenada em geladeira.
Não utilize a caneta após esse período.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Após aberto, válido por 28 dias (4 semanas).?
Características do medicamento
Solução límpida, incolor, sem nenhuma partícula sólida visível e de consistência aquosa.
Verifique sempre o prazo de validade que se encontra na embalagem do produto e confira o nome para não haver enganos. Não utilize Apidra SoloStar caso haja sinais de violação ou danificações da embalagem.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Mensagens de Alerta
Este medicamento pode causar dopping.
Informe ao seu médico se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde?.
Todo medicamento deve ser mantido fora do alcance das crianças.
Venda sob prescrição médica.
Dizeres Legais
MS 1.1300.0969
Farm. Resp.:
Silvia Regina Brollo
CRF-SP nº 9.815
Registrado por:
Sanofi-Aventis Farmacêutica Ltda.
Av. Mj. Sylvio de M. Padilha, 5200 – São Paulo – SP
CNPJ 02.685.377/0001-57
Indústria Brasileira
Fabricado por:
Sanofi-Aventis Deutschland GmbH
Brüningstrasse 50, Industriepark Höchst 65926
Frankfurt am Main – Alemanha
Importado por:
Sanofi-Aventis Farmacêutica Ltda.
Rua Conde Domingos Papaiz, 413 – Suzano – SP
CNPJ 02.685.377/0008-23
Ou
Registrado por:
Sanofi-Aventis Farmacêutica Ltda.
Av. Mj. Sylvio de M. Padilha, 5200 – São Paulo – SP
CNPJ 02.685.377/0001-57
Indústria Brasileira
Fabricado por:
Sanofi-Aventis Deutschland GmbH
Brüningstrasse 50, Industriepark Höchst 65926
Frankfurt am Main – Alemanha
Embalado e importado por:
Sanofi-Aventis Farmacêutica Ltda.
Rua Conde Domingos Papaiz, 413 – Suzano – SP
CNPJ 02.685.377/0008-23