Comparamos o preço de Irbesartana - E Hidroclorotiazida 300 12,5Mg 30 Comprimidos Euro Eurofarma Genérico, veja o menor preço

R$ 59,99
GGenérico
13
ofertasMelhores preços a partir de R$ 59,99 até R$ 141,45
Menor preço
vendido por Farmácia Super Droga 10
economize
57.59%
R$ 59,99
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Nova Esperança
economize
50.64%
R$ 69,82
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
vendido por Drogão Net
economize
48.53%
R$ 72,81
vendido por Drogaria São Paulo
economize
47.44%
R$ 74,35
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Drogarias Pacheco
economize
47.44%
R$ 74,35
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Pague Menos
economize
45.92%
R$ 76,49
vendido por Panvel Farmácias
economize
43.56%
R$ 79,83
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Farmácia Preço Popular
economize
43.34%
R$ 80,15
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Araújo
economize
40.62%
R$ 83,99
vendido por Farmácia Online Farmagora
economize
37.74%
R$ 88,06
Pagamento em até 6X sem juros. Frete Grátis! Regras no Site.
vendido por Drogaria Catarinense
economize
37.74%
R$ 88,06
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Farmácia Indiana
economize
23.75%
R$ 107,85
vendido por Drogaria Vera Cruz
R$ 141,45
Entregas para todo o Brasil. Clique e confira!
Para que serve
A Irbesartana + Hidroclorotiazida (substância ativa) é indicada no tratamento da hipertensão arterial em pacientes cuja pressão arterial não é controlada adequadamente com monoterapia. Pode ser usada isoladamente ou em associação com outros medicamentos anti-hipertensivos (por exemplo, bloqueadores beta-adrenérgicos, bloqueadores dos canais de cálcio de ação prolongada). A Irbesartana + Hidroclorotiazida (substância ativa) também pode ser usada como tratamento inicial nos casos em que a hipertensão é suficientemente grave de forma que o rápido controle da pressão arterial (dentro de dias ou semanas) é de extrema importância.
Contraindicação
A Irbesartana + Hidroclorotiazida (substância ativa) é contraindicada em pacientes com hipersensibilidade à irbesartana, aos derivados sulfonamídicos (por exemplo, diuréticos tiazídicos) ou a qualquer outro componente da fórmula.
Geralmente as reações de hipersensibilidade ocorrem com maior probabilidade em pacientes com história de alergia ou asma brônquica. A rbesartana + hidroclorotiazida é contraindicada em pacientes com anúria.
A Irbesartana + Hidroclorotiazida (substância ativa) não deve ser coadministrada com medicamentos que contenham alisquireno em pacientes com diabetes ou que apresentem insuficiência renal moderada a severa (taxa de filtração glomerular < 60 mL/min/1,73 m2).
A Irbesartana + Hidroclorotiazida (substância ativa) também não deve ser coadministrada com inibidores da enzima conversora de angiotensina (ECA) em pacientes com nefropatia diabética.
Como usar
Os comprimidos devem ser deglutidos inteiros, sem mastigar, com quantidade suficiente de líquido.
A Irbesartana + Hidroclorotiazida (substância ativa) pode ser administrada com ou sem alimentos.
Posologia
A Irbesartana + Hidroclorotiazida (substância ativa) (300 mg de irbesartana/ 12,5 mg de hidroclorotiazida) pode ser administrada em dose única diária à pacientes cuja pressão arterial não é adequadamente controlada com uso de monoterapia com 300 mg de irbesartana.
A Irbesartana + Hidroclorotiazida (substância ativa) (150 mg de irbesartana/12,5 mg de hidroclorotiazida) pode ser iniciada em pacientes que não estiverem controlados adequadamente com o uso de monoterapia com hidroclorotiazida ou de monoterapia com 150 mg de irbesartana. Os pacientes que não responderem adequadamente à Irbesartana + Hidroclorotiazida (substância ativa) (150 mg de irbesartana/12,5 mg de hidroclorotiazida) podem passar a utilizar a Irbesartana + Hidroclorotiazida (substância ativa) (300 mg de irbesartana/ 12,5 mg de hidroclorotiazida) e, posteriormente, se necessário, utilizar 300 mg de irbesartana / 25 mg de hidroclorotiazida. Doses superiores a 300 mg de irbesartana/25 mg de hidroclorotiazida não são recomendadas. Caso a pressão arterial não seja adequadamente controlada com Irbesartana + Hidroclorotiazida (substância ativa), pode-se associar outro medicamento anti-hipertensivo (p.ex. bloqueador beta adrenérgico, bloqueador do canal de cálcio com ação prolongada).
Terapia inicial (hipertensão arterial grave)
A dose usual do tratamento inicial com Irbesartana + Hidroclorotiazida (substância ativa) é 150 mg/12,5 mg uma vez ao dia. A dose pode ser aumentada após 1 a 2 semanas de tratamento para um máximo de 300 mg/25 mg uma vez ao dia, conforme necessário para o controle da pressão arterial.
Não há estudos dos efeitos de Irbesartana + Hidroclorotiazida (substância ativa) administrada por vias não recomendadas. Portanto, por segurança e para garantir a eficácia deste medicamento, a administração deve ser somente pela via oral.
Populações especiais
Pacientes com depleção de volume intravascular
Em pacientes com depleção acentuada de volume e/ou de sódio, tais como aqueles tratados com doses altas de diuréticos, deve-se corrigir essas condições antes de se administrar Irbesartana + Hidroclorotiazida (substância ativa).
Pacientes idosos e pacientes com comprometimento renal ou hepático
Geralmente não é necessária a redução da posologia em idosos ou em pacientes com disfunção renal leve a moderada (depuração de creatinina > 30 mL/min).
Entretanto, considerando-se a presença de hidroclorotiazida, não se recomenda o uso de Irbesartana + Hidroclorotiazida (substância ativa) em pacientes com insuficiência renal severa (depuração de creatinina ? 30 mL/min).
Geralmente não há necessidade de se reduzir a dose em caso de comprometimento hepático leve ou moderado. Contudo, devido à presença de hidroclorotiazida, recomenda-se cautela no uso de Irbesartana + Hidroclorotiazida (substância ativa) em pacientes com insuficiência hepática severa.
Este medicamento não deve ser partido ou mastigado.
Precauções
Hipotensão - Pacientes com depleção do volume
A Irbesartana + Hidroclorotiazida (substância ativa) tem sido raramente associada à hipotensão em pacientes hipertensos sem outros fatores de risco para a hipotensão. Deve ser prevista a possibilidade de ocorrer hipotensão sintomática em pacientes que desenvolvam depleção de sódio ou volume. A depleção de sódio e/ou volume deve ser corrigida antes de se iniciar o tratamento com Irbesartana + Hidroclorotiazida (substância ativa). Diuréticos tiazídicos podem potencializar a ação de outros medicamentos anti-hipertensivos.
Morbidade e mortalidade fetal / neonatal
Embora não haja experiência com o uso de Irbesartana + Hidroclorotiazida (substância ativa) em mulheres grávidas, foi relatado que a exposição em útero de inibidores da ECA administrados a mulheres no segundo e terceiro trimestres da gravidez pode provocar lesões e morte no feto em desenvolvimento. Portanto, assim como para qualquer medicamento que atua diretamente no sistema renina-angiotensina-aldosterona, Irbesartana + Hidroclorotiazida (substância ativa) não deve ser utilizada durante a gravidez. Uma vez detectada a gravidez durante o tratamento, Irbesartana + Hidroclorotiazida (substância ativa) deve ser interrompida logo que possível.
Os diuréticos tiazídicos atravessam a barreira placentária e passam ao sangue do cordão umbilical. O uso rotineiro de diuréticos em grávidas saudáveis não é recomendado e expõe a mãe e o feto a riscos desnecessários, incluindo icterícia fetal ou neonatal, trombocitopenia e possivelmente outras reações adversas que têm ocorrido em adultos.
Insuficiência Hepática e Função Renal
A Irbesartana + Hidroclorotiazida (substância ativa) não é recomendado para pacientes com insuficiência renal grave (clearance de creatinina ?30 mL / min). Em pacientes com insuficiência renal pode ocorrer azotemia (excesso de ureia e outros componentes nitrogenados no sangue) associada à hidroclorotiazida.
A Irbesartana + Hidroclorotiazida (substância ativa) deve ser usado com precaução em pacientes com insuficiência hepática ou doença hepática progressiva, uma vez que pequenas alterações no equilíbrio de fluidos e eletrólitos podem levar a um quadro de coma hepático.
Bloqueio duplo do sistema renina-angiotensina-aldosterona
O bloqueio duplo do sistema renina-angiotensina-aldosterona através da combinação de Irbesartana + Hidroclorotiazida (substância ativa) com inibidores da ECA ou com alisquireno não é recomendado uma vez que existe um aumento do risco de hipotensão, hipercalemia e alterações na função renal. O uso de Irbesartana + Hidroclorotiazida (substância ativa) em combinação com alisquireno é contraindicado em pacientes com diabetes mellitus ou insuficiência renal (filtração glomerular < 60 mL/min/1,73 m2).
O uso de Irbesartana + Hidroclorotiazida (substância ativa) em combinação com inibidores da ECA é contraindicado em pacientes com nefropatia diabética.
Gerais
Como consequência da inibição do sistema renina-angiotensina-aldosterona, alterações na função renal durante o tratamento com Irbesartana + Hidroclorotiazida (substância ativa), podem ser esperadas em pacientes susceptíveis. Em pacientes cuja função renal depende da atividade do sistema renina-angiotensina-aldosterona (pacientes hipertensos com estenose de artéria renal em um ou ambos os rins, ou pacientes com insuficiência cardíaca congestiva severa), o tratamento com outros fármacos que afetam este sistema tem sido associado com oligúria e/ou azotemia progressiva e, raramente, com insuficiência renal aguda e/ou óbito. A possibilidade de ocorrer um efeito similar com o uso de um antagonista do receptor de angiotensina II, incluindo Irbesartana + Hidroclorotiazida (substância ativa), não pode ser excluída. Os efeitos anti-hipertensivos dos diuréticos tiazídicos podem estar aumentados em pacientes submetidos à simpatectomia.
Desequilíbrio eletrolítico e metabólico
Os diuréticos tiazídicos, inclusive a hidroclorotiazida, podem causar desequilíbrio hídrico ou de eletrólitos (hipocalemia, hiponatremia e alcalose hipoclorêmica). Embora o uso isolado de tiazídicos, especialmente em doses altas, possa provocar hipocalemia, sua associação com irbesartana reduz a frequência de hipocalemia induzida por diuréticos. A deficiência de cloretos é geralmente leve e usualmente não requer tratamento. A excreção de cálcio é diminuída pelos tiazídicos, que podem provocar aumento discreto e intermitente do cálcio sérico. Uma hipercalcemia acentuada sugere a possibilidade de hiperparatireoidismo. O uso de tiazídicos deve ser suspenso antes de se efetuar testes funcionais das paratireoides. Os tiazídicos demonstraram aumentar a excreção urinária de magnésio, resultando em hipomagnesemia.
Alguns pacientes tratados com diuréticos tiazídicos podem apresentar hiperuricemia e crise aguda de gota. A administração de tiazídicos pode aumentar a necessidade de insulina em diabéticos e pode tornar manifesto um diabetes mellitus latente. O uso de tiazídicos tem sido associado a um aumento dos níveis de colesterol e triglicerídeos; entretanto, a dose de 12,5 mg hidroclorotiazida contida no Irbesartana + Hidroclorotiazida (substância ativa) foi relacionada a efeitos mínimos ou ausentes.
Em pacientes sob risco de alterações eletrolíticas ou metabólicas, pode ser necessária a monitoração de parâmetros laboratoriais.
Lúpus eritematoso sistêmico
Foi relatado agravamento ou ativação de lúpus eritematoso sistêmico com o uso de diuréticos tiazídicos.
Glaucoma agudo de ângulo fechado secundário e/ou Miopia aguda
A hidroclorotiazida é uma sulfonamida. A sulfonamida ou derivados de sulfonamida são medicamentos que podem causar uma reação idiossincrática, que podem resultar em glaucoma agudo de ângulo fechado secundário e/ou miopia aguda. Os sintomas incluem início agudo de diminuição da acuidade visual ou dor ocular e, geralmente, ocorrem dentro de horas ou semanas após o início do uso do medicamento. Se não for tratado, o glaucoma agudo de ângulo fechado pode levar à perda permanente da visão. O tratamento primário é descontinuar a administração do medicamento o mais rápido possível. Podem ser considerados tratamentos médicos ou cirúrgicos imediatos se a pressão intraocular permanecer descontrolada. O fator de risco para o desenvolvimento do glaucoma agudo de ângulo fechado pode incluir uma história de alergia à sulfonamida ou penicilina.
Gravidez e lactação
A Irbesartana + Hidroclorotiazida (substância ativa) deve ser descontinuada, logo que possível, quando for detectada gravidez.
Categoria de risco na gravidez: D.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez.
A irbesartana é excretada no leite de ratas lactantes. Não está determinado se a irbesartana ou seus metabólitos são excretados no leite humano. A hidroclorotiazida é excretada no leite humano. Os tiazídicos em altas doses causam diurese intensa podendo inibir a produção de leite. Não é recomendado o uso de Irbesartana + Hidroclorotiazida (substância ativa) durante a amamentação. Considerando-se o risco potencial para a criança, deve-se avaliar a descontinuação do tratamento ou da amamentação levando-se em conta a importância da Irbesartana + Hidroclorotiazida (substância ativa) no tratamento da mãe.
Alterações na capacidade de dirigir veículos e operar máquinas
Os efeitos de Irbesartana + Hidroclorotiazida (substância ativa) na habilidade de dirigir veículos ou operar máquinas não foram especificamente estudados, mas com base em suas propriedades farmacodinâmicas, é improvável que Irbesartana + Hidroclorotiazida (substância ativa) afete esta habilidade. Quando dirigir ou operar máquinas, deve-se levar em consideração que durante o tratamento da hipertensão, podendo ocorrer tontura ocasional.
Este medicamento pode causar doping.
Reações Adversas
- Reação muito comum ?1/10);
- Reação comum ?1/100 e < 1/10);
- Reação incomum (?1/1.000 e < 1/100);
- Reação rara (?1/10.000 e < 1/1.000);
- Reação muito rara (< 1/10.000).
A associação de irbesartana e hidroclorotiazida foi avaliada quanto à sua segurança em cerca de 2.750 pacientes em estudos clínicos, incluindo 1.540 hipertensos tratados por mais de 6 meses e cerca de 960 tratados por 1 ano ou mais. Os eventos adversos em pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) foram geralmente leves e transitórios, sem relação com a dose. A incidência das reações adversas não foi relacionada à idade, sexo ou raça.
A descontinuação do tratamento devido a qualquer evento adverso clínico ou laboratorial ocorreu em 3,6% nos pacientes tratados com a associação e em 6,8% naqueles que receberam placebo (p=0,023), em estudos clínicos controlados com placebo envolvendo 898 pacientes tratados com o Irbesartana + Hidroclorotiazida (substância ativa) (com duração usual do tratamento de 2 a 3 meses).
Reações adversas (eventos adversos clínicos provável ou possivelmente relacionados ao tratamento, ou com relação incerta) que ocorreram em pelo menos 1% dos pacientes tratados com irbesartana/ hidroclorotiazida, irbesartana, hidroclorotiazida ou placebo em estudos controlados estão listadas na tabela a seguir

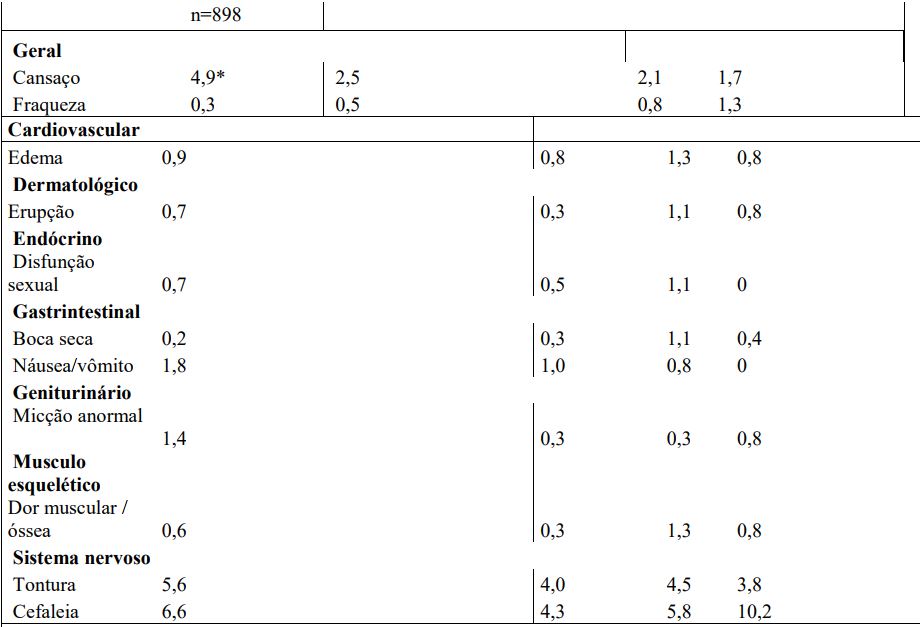
*Diferenças estatisticamente significativas entre Irbesartana + Hidroclorotiazida (substância ativa) e placebo nos grupos tratados (p=0,03).
Outras reações adversas
Outras reações adversas (evento clínico de relação provável, possível ou incerta com o tratamento), que ocorreram com frequência entre 0,5% e <1% e que tiveram incidência ligeiramente maior nos pacientes tratados com a associação do que com placebo, incluem: diarreia, tontura (ortostática), rubor, alterações da libido, taquicardia, edema das extremidades. Em nenhum dos eventos houve diferença estatisticamente significativa entre os pacientes tratados com a associação e o placebo.
As reações adversas que ocorreram com incidência levemente maior em pacientes tratados com monoterapia de irbesartana em comparação aos tratados com placebo, e com frequência entre 0,5% e <1% mas sem significância estatística, foram
Anormalidades do ECG, prurido, dor abdominal e fraqueza nas extremidades.
Outras reações adversas de interesse clínico com frequência menor que 0,5% e que tiveram incidência ligeiramente maior nos pacientes tratados com a associação do que com o grupo placebo foram hipotensão e síncope.
Terapia inicial
As reações adversas nos estudos de hipertensão severa e moderada descritas abaixo são similares às reações adversas nos estudos de hipertensão descritas acima.
Em estudo de hipertensão arterial moderada (PADSe entre 90 e 110 mm Hg) os tipos e a incidência de reações adversas reportadas pelos pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) como terapia inicial foram semelhantes às reportadas por pacientes tratados inicialmente com irbesartana ou hidroclorotiazida em monoterapia. Não houve caso de síncope no grupo tratado com Irbesartana + Hidroclorotiazida (substância ativa), e foi reportado um caso de síncope no grupo tratado com monoterapia de hidroclorotiazida.
A incidência das reações adversas pré-determinadas para Irbesartana + Hidroclorotiazida (substância ativa), irbesartana e hidroclorotiazida foram, respectivamente: hipotensão 0,9%, 0% e 0%; tontura 3,0%, 3,8% e 1,0%; dor de cabeça 5,5%, 3,8% e 4,8%; hipercalemia 1,2%, 0% e 1,0%; hipocalemia 0,9%, 0% e 0%. A taxa de descontinuação do tratamento em razão das reações adversas foram, respectivamente, 6,7%, 3,8% e 4,8%.
Em um estudo de hipertensão arterial severa (PADs ? 110 mm Hg), o padrão geral das reações adversas reportadas durante 7 semanas de acompanhamento foi semelhante em pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) como terapia inicial e irbesartana como terapia inicial. A incidência das reações adversas pré- determinadas foi, para Irbesartana + Hidroclorotiazida (substância ativa) e irbesartana, respectivamente, síncope 0% e 0%, hipotensão 0,6% e 0%, tontura 3,6% e 4,0%, dor de cabeça 4,3% e 6,6%, hipercalemia 0,2% e 0%, hipocalemia 0,6% e 0,4%. A taxa de descontinuação do tratamento em razão das reações adversas foi, respectivamente, 2,1% e 2,2%.
Experiência pós-comercialização
Casos muito raros de reações de hipersensibilidade (angioedema, urticária) foram relatados a partir da comercialização da irbesartana em monoterapia, assim como ocorre com outros antagonistas do receptor da angiotensina II. Os seguintes eventos adversos foram relatados durante o período de pós-comercialização sem, entretanto, ser estabelecida necessariamente, uma relação causal: vertigem, astenia, hipercalemia, mialgia, icterícia, elevação dos testes de função hepática, hepatite e diminuição da função renal, incluindo casos de falência renal em pacientes de risco.
Outras reações adversas clínicas relatadas com o uso isolado de hidroclorotiazida
Outras reações adversas clínicas relatadas com o uso isolado de hidroclorotiazida (relacionadas ou não ao tratamento) incluem: anorexia, irritação gástrica, diarreia, constipação, icterícia (colestática intra-hepática), pancreatite, sialoadenite, vertigem, parestesia, xantopsia, leucopenia, neutropenia/agranulocitose, trombocitopenia, anemia aplástica, anemia hemolítica, reações de fotossensibilidade, febre, urticária, angeíte necrosante (vasculite, vasculite cutânea), distúrbios respiratórios (incluindo pneumonite e edema pulmonar), reações anafiláticas, necrólise epidérmica tóxica, hiperglicemia, glicosúria, hiperuricemia, distúrbios eletrolíticos (incluindo hiponatremia e hipocalemia), disfunção renal, nefrite intersticial, espasmo muscular, fraqueza, inquietação, distúrbios oculares (visão turva transitória, glaucoma agudo de ângulo fechado secundário e/ou miopia aguda).
Não se verificaram alterações clinicamente significativas em exames laboratoriais, nos estudos clínicos controlados com Irbesartana + Hidroclorotiazida (substância ativa).
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária - NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
Interação Medicamentosa
Com base nos dados in vitro não se esperam interações entre a irbesartana e medicamentos cujo metabolismo depende das isoenzimas do citocromo P450, CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2D6, CYP2E1 e CYP3A4. A irbesartana é metabolizada principalmente pelo CYP2C9, no entanto, durante estudos de interação clínica não foram observadas interações farmacodinâmicas e farmacocinéticas significativas com o uso concomitante de irbesartana e varfarina (fármaco metabolizado pelo CYP2C9). A irbesartana não afeta a farmacocinética da digoxina ou da sinvastatina. A coadministração de nifedipina ou de hidroclorotiazida não afeta a farmacocinética da irbesartana.
A combinação de Irbesartana + Hidroclorotiazida (substância ativa) com medicamentos que contenham alisquireno é contraindicada em pacientes com diabetes mellitus ou com insuficiência renal moderada a severa (taxa de filtração glomerular < 60 mL/min/1,73 m2) e não é recomendada em outros pacientes.
Inibidores da ECA
A combinação de Irbesartana + Hidroclorotiazida (substância ativa) com os inibidores da ECA é contraindicada em pacientes com nefropatia diabética e não é recomendada para os demais pacientes. Com base na experiência com o uso de outros medicamentos que afetam o sistema renina angiotensina, pode-se esperar que a irbesartana leve a um aumento do potássio sérico, quando administrada concomitantemente com diuréticos poupadores de potássio, suplementos de potássio ou substitutos salinos contendo potássio. O uso concomitante com hidroclorotiazida pode reduzir a frequência desse efeito.
Em pacientes idosos, com depleção de volume (incluindo aqueles em tratamento com diuréticos) ou com comprometimento da função renal, a administração concomitante de agentes anti-inflamatórios não esteroidais (AINEs) incluindo inibidores seletivos da ciclooxigenase-2 (COX-2), com os antagonistas dos receptores da angiotensina II, incluindo a irbesartana, pode resultar em deterioração da função renal, incluindo possível insuficiência renal aguda. Estes efeitos são normalmente reversíveis. Monitorar periodicamente a função renal dos pacientes sob tratamento com irbesartana e AINE. O efeito anti-hipertensivo dos antagonistas do receptor da angiotensina II, incluindo a irbesartana, pode ser atenuado pelos AINEs, incluindo inibidores seletivos da COX- 2.
Diuréticos tiazídicos podem ser potencializados por álcool, barbitúricos e narcóticos, com possibilidade de surgir hipotensão ortostática.
Os tiazídicos podem aumentar a glicemia e, portanto, pode ser necessário ajustar a dose de antidiabéticos orais e insulina, em pacientes diabéticos.
A hidroclorotiazida pode elevar o nível sanguíneo de ácido úrico, tornando necessário o ajuste posológico de medicação antigotosa.
A hipocalemia induzida por diuréticos pode acentuar arritmias cardíacas com glicosídeos cardíacos (por exemplo, a digoxina) e outros medicamentos antiarrítmicos (por exemplo, o sotalol).
Os diuréticos tiazídicos podem aumentar os níveis de cálcio sérico devido à redução da sua excreção. Caso seja prescrito cálcio ou medicamentos poupadores de cálcio (por exemplo, na terapia com vitamina D), deve-se monitorar os níveis plasmáticos de cálcio e ajustar a dosagem de cálcio adequadamente.
A resina colestiramina e o cloridrato de colestipol podem retardar ou diminuir a absorção da hidroclorotiazida. A Irbesartana + Hidroclorotiazida (substância ativa) deve ser administrada pelo menos 1 hora antes ou 4 horas após estes medicamentos.
Aumentos nas concentrações séricas de lítio e intoxicação por lítio têm sido reportados com o uso concomitante com irbesartana. Monitorar os níveis de lítio em pacientes recebendo irbesartana e lítio.
Os diuréticos reduzem a depuração renal de lítio e aumentam o risco de toxicidade desse composto. A administração concomitante de Irbesartana + Hidroclorotiazida (substância ativa) e lítio deve ser feita com cautela e recomenda-se monitorização frequente dos níveis séricos de lítio.
Em alguns pacientes, os inibidores da síntese de prostaglandinas endógena (p.ex. os anti-inflamatórios não esteroidais - AINES) podem reduzir os efeitos dos diuréticos tiazídicos.
O componente tiazídico de Irbesartana + Hidroclorotiazida (substância ativa) pode potencializar a ação de outros anti-hipertensivos, especialmente dos bloqueadores adrenérgicos periféricos ou ganglionares. A hidroclorotiazida pode interagir com diazóxido; deve-se monitorizar a glicemia, os níveis séricos de ácido úrico e a pressão arterial.
Os efeitos de relaxantes musculares não-despolarizantes, pré-anestésicos e anestésicos usados em cirurgia (por exemplo, a tubocurarina) podem ser potencializados pela hidroclorotiazida; pode ser necessário o ajuste de dose. Os pré-anestésicos e anestésicos devem ser administrados em doses reduzidas, e se possível, descontinuar a terapia com hidroclorotiazida uma semana antes da cirurgia.
O uso concomitante de carbamazepina e hidroclorotiazida está associado com o risco de hiponatremia sintomática. Durante o uso concomitante os eletrólitos devem ser monitorados. Se possível, uma outra classe de diuréticos deve ser usada.
Interações medicamento-exame laboratorial
Não houve alterações clinicamente significativas nos testes laboratoriais que ocorreram nos estudos clínicos com Irbesartana + Hidroclorotiazida (substância ativa).
Interação Alimentícia
Não há dados disponíveis até o momento sobre a interferência de alimentos na ação de Irbesartana + Hidroclorotiazida (substância ativa).
Ação da Substância
Resultados de eficácia
Os antagonistas dos receptores AT1 da angiotensina II têm se tornado uma classe estabelecida para o tratamento da hipertensão arterial e sua larga utilização está relacionada à reconhecida eficácia anti-hipertensiva, combinada a um perfil de tolerabilidade semelhante ao placebo).
Diferenças entre as propriedades farmacodinâmicas e farmacocinéticas das moléculas desta classe podem levar a diferenças significativas nas suas potências anti-hipertensivas.
A irbesartana é um potente bloqueador dos receptores AT1 da angiotensina II (BRA) e altamente seletivo para esses receptores do subtipo 1.
O Estudo COSIMA teve como desfechos primário e secundário avaliar a eficácia anti- hipertensiva, aferida pela redução da pressão arterial sistólica (PAS) e pressão arterial diastólica (PAD), quando comparadas ao basal, bem como avaliar o percentual de normalização da pressão arterial (PA), após 8 semanas de tratamento.
Como parte dos resultados do estudo, a irbesartana na dose de 150 mg combinada com hidroclorotiazida 12,5 mg, nos 222 pacientes incluídos na análise de intenção de tratamento com hipertensão arterial essencial leve à moderada, mostrou uma redução de 13,0 e de 9,5 mm Hg na PAS e PAD, respectivamente, quando avaliadas pela monitoração residencial da pressão arterial (MRPA); e uma redução de 15,0 e de 8,6 mm Hg na PAS e PAD, respectivamente, quando aferidas no consultório, bem como uma taxa de normalização da PA de 50,2 e de 51,4% quando avaliadas pela MRPA e no consultório, respectivamente.
O Estudo INCLUSIVE buscou avaliar a eficácia e segurança do uso da associação fixa da irbesartana com a hidroclorotiazida (HCTZ) em pacientes com pressão arterial não controlada. O tratamento, envolvendo 1005 pacientes, apresentava um perfil sequencial e distribuído da seguinte forma: placebo (4 - 5 semanas), HCTZ 12,5mg (2 semanas), irbesartana / HCTZ 150 mg / 12, 5 mg (8 semanas) e irbesartana / HCTZ 300 mg / 25 mg (8 semanas).
Os objetivos definidos de redução das pressões arteriais sistólica e diastólica eram consistentes com as diretrizes internacionais de tratamento da hipertensão arterial: PAS < 140 mm Hg (<130mmHg para pacientes com diabetes tipo 2) e PAD < 90mm Hg (< 80 mmHg para pacientes com diabetes tipo 2).
Os resultados do estudo mostraram uma redução média da PAS de 21,5 mm Hg (p < 0,001) e da PAD foi de 10,4 mm Hg (p < 0,001). Um percentual de 77% e 83% dos pacientes atingiram o objetivo do estudo de redução da PAS e PAD, respectivamente, e 69% dos pacientes atingiram ambos os objetivos das PAS/PAD, de acordo com o JNC 7.
O Estudo CV131176 (Study CV131176, 2000) teve como objetivo avaliar a eficácia e segurança da associação irbesartana/HCTZ, como uma terapia de primeira linha na hipertensão arterial grave. O tratamento, com duração de sete semanas, envolveu pacientes hipertensos não tratados, não controlados (pressão arterial diastólica sentada [PADSe] ?110 mm Hg) e pacientes com hipertensão arterial não controlada com monoterapia anti-hipertensiva. As doses utilizadas no grupo irbesartana/HCTZ foram de 150 mg /12,5 mg e 300 mg / 25 mg.
Como parte dos resultados do estudo, na quinta semana (desfecho primário de eficácia), 47,2% dos pacientes do grupo irbesartana/HCTZ atingiram o objetivo de controle da PADSe (< 90mm Hg), atingindo um máximo de 51,9%, na sétima semana. Uma redução média ajustada em relação ao basal da PADSe e PASSe, para o grupo irbesartana/HCTZ de -21,2 mmHg e 27,1 mmHg, respectivamente, foram observadas precocemente no tratamento (semana 3).
Características farmacológicas
Mecanismo de ação
A irbesartana é um antagonista específico não-competitivo dos receptores da angiotensina II (subtipo AT1). A angiotensina II é um componente importante do sistema renina-angiotensina e está envolvida na fisiopatologia da hipertensão e na homeostase do sódio. A irbesartana não necessita de ativação metabólica para exercer sua atividade.
A irbesartana bloqueia os potentes efeitos de vasoconstrição e de secreção de aldosterona produzidos pela angiotensina II, graças à sua ação de antagonismo seletivo nos receptores da angiotensina II (subtipo AT1), localizados nas células da musculatura lisa vascular e no córtex suprarrenal.
A irbesartana não tem efeito agonista nos receptores AT1, e possui muito mais afinidade (superior a 8500 vezes) para os receptores AT1, do que para os receptores AT2 (que não parecem estar associados à homeostasia cardiovascular).
A irbesartana não inibe as enzimas envolvidas no sistema renina-angiotensina (isto é, renina, enzima conversora da angiotensina [ECA]), nem afeta outros receptores hormonais ou canais de íons que participam da regulação da pressão arterial e da homeostase do sódio. O bloqueio dos receptores AT1 pela irbesartana interrompe o mecanismo da retroalimentação do sistema renina-angiotensina, resultando no aumento dos níveis plasmáticos de renina e de angiotensina II. No entanto, o resultante aumento dos níveis plasmáticos de renina e de angiotensina II não superam os efeitos da irbesartana na redução da pressão arterial. A concentração plasmática de aldosterona diminui após administração da irbesartana, mas os níveis séricos de potássio não sofrem alteração significativa (aumento médio < 0,1 mEq/L), na posologia recomendada. A irbesartana não tem efeito significativo sobre as concentrações séricas de triglicerídios, colesterol ou glicose. Não há efeito nos níveis séricos nem na excreção urinária de ácido úrico.
A hidroclorotiazida é um diurético do grupo das benzotiazidinas (tiazídico), com efeitos diurético, natriurético e anti-hipertensivo. O mecanismo do efeito anti-hipertensivo dos diuréticos tiazídicos, bem como a hidroclorotiazida, ainda não está completamente esclarecido. As tiazidas afetam o mecanismo de reabsorção de eletrólitos pelos túbulos renais, aumentando a excreção de sódio e cloreto em quantidades aproximadamente equivalentes. A natriurese provoca uma perda secundária de potássio e bicarbonato. A hidroclorotiazida aumenta a atividade da renina plasmática, aumenta a secreção de aldosterona e reduz o nível sérico de potássio. A perda de potássio associada ao uso de diuréticos tiazídicos pode ser neutralizada pela coadministração de um antagonista do receptor da angiotensina II.
Propriedades farmacodinâmicas
Com base nos dados de estudos clínicos controlados com placebo, os seguintes efeitos foram observados.
O efeito redutor sobre a pressão arterial da associação de irbesartana e hidroclorotiazida foi aparente após a primeira administração e substancialmente evidente dentro de 1 a 2 semanas, com o efeito máximo ocorrendo entre a 6a e 8a semanas. O efeito da associação foi mantido por mais de um ano, em estudos de acompanhamento prolongado.
A associação de hidroclorotiazida e irbesartana proporciona efeito aditivo na redução da pressão arterial, relacionado às doses administradas. A administração de 12,5 mg de hidroclorotiazida e 300 mg de irbesartana, uma vez ao dia, a pacientes não adequadamente controlados com monoterapia de 300 mg de irbesartana resultou em redução adicional (com correção do efeito placebo) de 6,1 mmHg na pressão arterial diastólica na fase de vale (24 horas após a administração do medicamento). As reduções globais nas pressões arteriais sistólica/diastólica com essa associação foram de até 13,6/11,5 mmHg, após subtração do efeito placebo. Uma dose de 150 mg de irbesartana e 12,5 mg de hidroclorotiazida uma vez ao dia causou redução média de 12,9/6,9 mmHg na pressão arterial sistólica/diastólica ajustada pelo placebo, na fase de vale (24 horas após a administração do medicamento). O efeito máximo ocorre entre 3 e 6 horas. Avaliações através do método de monitoração ambulatorial da pressão arterial (MAPA) mostram que Irbesartana + Hidroclorotiazida (substância ativa) 150/ 12,5 mg uma vez ao dia leva a uma redução média consistente de 15,8/10,0 mm Hg da pressão arterial com subtração do efeito placebo durante o período de 24 horas. Os efeitos “vale-pico” observados foram de, pelo menos, 68% das respostas nos picos sistólico e diastólico com subtração do efeito do placebo correspondente.
A adição de irbesartana à hidroclorotiazida em um estudo clínico em pacientes não controlados adequadamente com 25mg de hidroclorotiazida isolada proporcionou reduções adicionais médias de 11,1/7,2 mm Hg na pressão arterial sistólica/diastólica em relação à hidroclorotiazida isolada.
A redução da pressão arterial foi semelhante tanto na posição supina como na ortostática. Efeitos ortostáticos foram pouco frequentes, mas podem ser esperados em pacientes que desenvolvam intercorrência de depleção de sódio e/ou volume.
A eficácia da associação Irbesartana + Hidroclorotiazida (substância ativa) não sofreu influência da idade, raça ou gênero. A resposta anti-hipertensiva global da associação foi similar nos pacientes de raça negra e de outras etnias.
A pressão arterial retornou gradualmente aos valores basais após suspensão da irbesartana. Não se observou hipertensão rebote com irbesartana ou hidroclorotiazida.
Para a hidroclorotiazida, o início da diurese ocorreu em 2 horas, com efeito máximo ocorrendo em torno de 4 horas, enquanto a duração persistiu cerca de 6 a 12 horas.
Terapia inicial
Dois estudos clínicos avaliaram Irbesartana + Hidroclorotiazida (substância ativa) como terapia inicial.
O primeiro estudo foi realizado com pacientes com pressão arterial basal média de 162/98 mm Hg (hipertensão moderada) e, após 8 semanas de tratamento, comparou a variação da pressão arterial sistólica a partir da linha basal entre o grupo da associação (Irbesartana + Hidroclorotiazida (substância ativa) 150 mg + 12,5 mg), irbesartana (150 mg) ou hidroclorotiazida (12,5 mg). Após 2 semanas de tratamento os regimes iniciais do estudo foram aumentados para Irbesartana + Hidroclorotiazida (substância ativa) 300 mg/ 25 mg, irbesartana 300 mg ou hidroclorotiazida 25 mg, respectivamente. Após 8 semanas, as reduções médias da pressão arterial diastólica e sistólica a partir do basal no vale foram de 14,6 mm Hg e 27,1 mmHg nos pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa), 11,6 mm Hg e 22,1 mmHg nos pacientes tratados com irbesartana e 7,3 mmHg e 15,7 mmHg nos pacientes tratados com hidroclorotiazida, respectivamente. Nos pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) a variação média da PADSe a partir do basal foi 3,0 mmHg menor (p = 0,0013) e a variação média da PASSe a partir da linha basal foi 5,0 mmHg menor (p = 0,0016) em comparação com pacientes tratados com irbesartana e 7,4 mmHg menor (p < 0,0001) e 11,3 mmHg menor (p < 0,0001) em comparação com pacientes tratados com hidroclorotiazida, respectivamente.
O segundo estudo clínico foi conduzido em pacientes com pressão arterial basal média de 172/113 mm Hg (hipertensão severa) e comparada à variação através do PADSe após 5 semanas entre os grupos Irbesartana + Hidroclorotiazida (substância ativa) (150 mg + 12,5 mg) e irbesartana (150 mg). Estas posologias iniciais do estudo foram aumentadas, na Semana 1, para irbesartana / hidroclorotiazida 300 mg/25 mg ou irbesartana 300 mg, respectivamente.
Após 5 semanas, as reduções médias a partir do basal para a pressão arterial diastólica e sistólica foram de 24,0 mmHg e 30,8 mmHg nos pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) e 19,3 mmHg e 21,1 mm Hg nos pacientes tratados com irbesartana, respectivamente. A média de PADSe foi 4,7 mmHg menor (p < 0,0001) e a média de PASSe foi 9,7 mm Hg menor (p < 0,0001) no grupo tratado com Irbesartana + Hidroclorotiazida (substância ativa) em comparação ao grupo tratado com irbesartana. Os pacientes tratados com Irbesartana + Hidroclorotiazida (substância ativa) atingiram o controle de pressão arterial mais rapidamente com redução significante de PADS e PAS e maior controle de pressão arterial em cada avaliação (Semana 1, Semana 3, Semana 5 e Semana 7). Os efeitos máximos foram vistos na Semana 7.
Propriedades farmacocinéticas
A administração concomitante de hidroclorotiazida e irbesartana não afeta as características farmacocinéticas desta última.
Absorção
A irbesartana e a hidroclorotiazida são substâncias ativas por via oral que não necessitam de biotransformação para exercer sua atividade. Após administração oral de Irbesartana + Hidroclorotiazida (substância ativa), a biodisponibilidade absoluta oral é de 60-80% para a irbesartana e 50-80% para a hidroclorotiazida.
Os alimentos não alteram a biodisponibilidade da Irbesartana + Hidroclorotiazida (substância ativa). Concentrações plasmáticas máximas são alcançadas de 1,5 a 2 horas para irbesartana e de 1 a 2,5 horas para hidroclorotiazida, após administração por via oral.
Distribuição
A irbesartana tem uma taxa de ligação às proteínas plasmáticas de cerca de 96% e sua ligação às células sanguíneas é desprezível. O volume de distribuição da irbesartana está entre 53 e 93 litros (0,72-1,24 L/kg). A taxa de ligação da hidroclorotiazida às proteínas plasmáticas é de 68% e seu volume aparente de distribuição é de 3,6-7,8 L/kg.
Metabolismo
A irbesartana é metabolizada pelo fígado através da via de conjugação glicurônica e oxidação, após administração oral ou intravenosa da irbesartana marcada com C14, 80% a 85% da radioatividade circulante no plasma corresponde ao composto inalterado. O principal metabólito circulante é a irbesartana-glucuronídeo (aproximadamente 6%).
A irbesartana é oxidada principalmente através das isoenzimas CYP 2C9 do citocromo P450; a isoenzima CYP 3A4 possui efeito desprezível. A irbesartana não foi metabolizada pela maior parte das isoenzimas comumente associadas com o metabolismo de fármacos (CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2D6 ou CYP2E1) nem induziu ou inibiu estas enzimas. A irbesartana também não induziu nem inibiu a isoenzima CYP 3A4.
Eliminação
A irbesartana e seus metabólitos são excretados tanto por via biliar quanto renal. Cerca de 20% da radioatividade, após administração de uma dose oral ou intravenosa de irbesartana marcada com C14, é recuperada na urina e o restante nas fezes. Menos de 2% da dose de irbesartana administrada são excretados na urina sob forma inalterada. A hidroclorotiazida não é metabolizada, sendo eliminada por via renal. A meia-vida plasmática média da hidroclorotiazida é estimada entre 5 a 15 horas.
A meia-vida de eliminação terminal (t1?2) da irbesartana é de 11 a 15 horas. A depuração total do organismo após administração intravenosa é de 157 a 176 mL/min, dos quais 3,0 a 3,5 mL/min constituem depuração renal. A irbesartana tem farmacocinética linear, dentro dos limites da posologia terapêutica. O estado de equilíbrio no plasma é alcançado dentro de 3 dias do início de um regime de dose única diária. Observa-se acúmulo limitado (< 20%) no plasma após administração repetida de doses diárias únicas.
Populações especiais
Insuficiência renal
A farmacocinética da irbesartana não é significativamente alterada em pacientes com insuficiência renal (independentemente do grau) ou sob hemodiálise. A irbesartana não é removida por hemodiálise. Relatou-se um aumento da meia-vida de eliminação da hidroclorotiazida para 21 horas, em pacientes com insuficiência renal severa (depuração de creatinina < 20 mL/min).
Insuficiência hepática
A farmacocinética da irbesartana não é significativamente alterada em pacientes com insuficiência hepática devida a cirrose leve ou moderada.
Idosos
Em indivíduos idosos normotensos de ambos os sexos (65 a 80 anos), com funções hepática e renal clinicamente normais, a área sob a curva (ASC) da concentração plasmática e as concentrações plasmáticas máximas (Cmáx) da irbesartana foram, aproximadamente, 20 a 50% maiores que aquelas verificadas em pessoas mais jovens (18 a 40 anos). A meia-vida de eliminação é comparável nos diversos grupos etários. Não foram observadas diferenças significativas nos efeitos clínicos relacionadas à idade. A ASC da concentração plasmática da hidroclorotiazida foi mais elevada nos pacientes idosos após administração repetida, resultado consistente com dados de publicações anteriores.
Sexo
Em homens e mulheres hipertensos, observaram-se concentrações plasmáticas de irbesartana mais elevadas (11- 44%) no sexo feminino, se bem que não há diferenças entre homens e mulheres quanto ao acúmulo e à meia-vida de eliminação, após doses repetidas. Não se observaram diferenças de efeito clínico nos dois sexos.
Raça
Em indivíduos normotensos da raça negra e branca, os valores da ASC plasmática e do tempo de meia-vida (t1?2) da irbesartana foram aproximadamente 20-25% maiores em indivíduos da raça negra em comparação com os da raça branca. O pico das concentrações plasmáticas (Cmáx) da irbesartana foram essencialmente equivalentes.
Dados de segurança pré-clínica
Carcinogênese, mutagênese, comprometimento da fertilidade
O potencial carcinogênico da associação irbesartana e hidroclorotiazida não foi avaliado em estudos em animais. Entretanto, não se observou evidência de carcinogenicidade com a administração isolada de irbesartana em ratos com doses de 500/1000 mg/kg/dia, respectivamente em machos/fêmeas e em camundongos 1.000 mg/kg/dia durante 2 anos. As doses referidas correspondem a uma exposição sistêmica 4 a 25 vezes (em ratos) e 4 a 6 vezes (em camundongos) maior do que a exposição em humanos recebendo 300 mg diários. Paralelamente, sabe-se que a vasta experiência de uso da hidroclorotiazida em humanos não demonstrou qualquer associação entre o seu uso e o aumento de neoplasias. Portanto, não há razões de preocupação quanto ao potencial de efeitos carcinogênicos da Irbesartana + Hidroclorotiazida (substância ativa) na espécie humana.
A associação de irbesartana e hidroclorotiazida não se mostrou mutagênica no teste de Ames ou no teste de mutação genética HGPRT em células de ovário de hamsters chineses, e não foi clastogênica em um teste citogenético in vitro em linfócitos humanos ou em um ensaio de micronúcleo em células da mucosa oral em camundongos.
Não se avaliou o efeito da associação de irbesartana e hidroclorotiazida sobre a fertilidade em estudos animais. Sabe-se, entretanto que a fertilidade e o desempenho reprodutor de ratos não foram afetados pela irbesartana isolada em doses capazes de causar algum grau de toxicidade parenteral (até 650 mg/kg/dia). Não foram observados efeitos significativos quanto ao número de corpos lúteos, implantação do ovo e fetos vivos. Além disso, a irbesartana não teve influência na sobrevida, no desenvolvimento ou na reprodução da ninhada. Quanto à hidroclorotiazida, a larga experiência em humanos não revelou qualquer relação entre o seu uso e alteração da fertilidade.
Consequentemente, não há razão de preocupação quanto ao potencial de reações adversas na fertilidade com o uso de Irbesartana + Hidroclorotiazida (substância ativa).
Não foram observados efeitos teratogênicos em ratas que receberam a associação de irbesartana / hidroclorotiazida em doses de até 150 / 150 mg/kg/dia (nível de dose que causou toxicidade materna).