Comparamos o preço de Protopic - 0,01% Pomada 10G, veja o menor preço

R$ 101,06
RReferência
1
ofertasMelhores preços a partir de R$ 101,06 até R$ 101,06
Menor preço
vendido por Drogaria Nova Esperança
R$ 101,06
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
Para que serve
Protopic possui efeito nas células do sistema imune e está indicado para
- Tratamento de dermatite atópica (também chamada de eczema) em pacientes que não apresentam boa resposta ou são intolerantes aos tratamentos convencionais;
- Promover alívio dos sintomas e controlar os surtos;
- Manutenção do tratamento de dermatite atópica para prevenção de surtos dos sintomas e para prolongar os intervalos livres de surtos em pacientes que possuem alta frequência de piora da doença (isto é, que ocorra 4 ou mais vezes por ano) e que tiveram uma resposta inicial a um tratamento máximo de 6 semanas, 2 vezes ao dia, com tacrolimo pomada (lesões que desapareceram, lesões que quase desapareceram ou áreas levemente afetadas);
Protopic 0,03% está indicado para uso em crianças de 2 a 15 anos e adultos.
Protopic 0,1% está indicado para uso em indivíduos acima de 16 anos.
Como Protopic funciona?
Na dermatite atópica, uma reação anormal do sistema imune da pele causa inflamação caracterizada por coceira, vermelhidão e ressecamento. Protopic altera a resposta imune anormal e alivia as inflamações na pele e a coceira. A melhora é geralmente verificada dentro de uma semana.
Contraindicação
Não use Protopic se você for alérgico (hipersensível) ao tacrolimo ou qualquer um dos componentes da fórmula ou à antibióticos macrolídeos (tais como, azitromicina, claritromicina, eritromicina).
Este medicamento é contraindicado para menores de 2 anos.
Este medicamento não deve ser utilizado por mulheres que estão amamentando sem orientação médica ou do cirurgião-dentista.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Como usar
Sempre utilize Protopic exatamente como seu médico prescreveu. Em caso de qualquer dúvida, verifique com seu médico ou farmacêutico.
Protopic pode ser utilizado na maioria das partes do corpo, incluindo a face, pescoço, nas dobras do cotovelo e joelhos.
Evite utilizar a pomada dentro de seu nariz ou boca ou dentro dos olhos. Se a pomada atingir qualquer uma dessas áreas, ela deve ser retirada imediatamente e/ou enxaguada com água.
Não cubra a pele que está sendo tratada com bandagens ou qualquer tipo de envoltório. Lave suas mãos após aplicar Protopic, a menos que suas mãos também estejam em tratamento.
Antes de aplicar Protopic após o banho, certifique-se que sua pele está completamente seca.
Posologia
Aplique Protopic como uma fina camada nas áreas afetadas de sua pele.
Tratamento inicial
Crianças de 2 anos a 15 anos
Aplique Protopic 0,03% duas vezes ao dia durante 3 semanas, uma vez pela manhã e uma vez à noite.
Após este período, a pomada deve ser utilizada uma vez ao dia em cada região afetada da pele até que o eczema tenha desaparecido.
Adultos (16 anos de idade ou mais)
Duas concentrações de Protopic (Protopic 0,03% e Protopic 0,1% pomada) estão disponíveis para pacientes adultos. Seu médico irá decidir qual a melhor concentração para você.
Geralmente, o tratamento é iniciado com Protopic 0,1% pomada duas vezes ao dia, uma vez pela manhã e uma vez à noite, até que o eczema desapareça. Se os sintomas reaparecerem, o tratamento com Protopic 0,1% deve ser reiniciado.
Dependendo da resposta de seu eczema, seu médico irá decidir pela redução da frequência das aplicações ou pela utilização da menor concentração, Protopic 0,03%, pode ser utilizado.
Trate cada região afetada de sua pele até que o eczema tenha desaparecido. A melhora é geralmente verificada dentro de uma semana. Se você não notar nenhuma melhora após 2 semanas, verifique com seu médico sobre outras possibilidades de tratamento. O tratamento com Protopic pode ser repetido se os sintomas reaparecerem.
Estudos específicos não foram conduzidos em pacientes idosos. Entretanto, a experiência clínica disponível nesta população de pacientes não demonstra necessidade de qualquer ajuste de dosagem.
Indicação de manutenção
Você pode ser orientado pelo seu médico a utilizar Protopic pomada 2 vezes por semana, desde que o surto de sua dermatite atópica tenha desaparecido ou quase desaparecido (Protopic 0,03% para adultos e crianças e 0,1% para adultos). Protopic pomada deve ser aplicado uma vez ao dia duas vezes por semana (por exemplo, segunda e quinta-feira) nas áreas de seu corpo comumente afetadas pela dermatite atópica. Entre as aplicações deve haver 2 a 3 dias sem o tratamento com Protopic. Se os sintomas reaparecerem, você deve voltar a utilizar Protopic duas vezes ao dia, conforme indicado acima, e consultar seu médico para revisar seu tratamento.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
O que devo fazer quando eu me esquecer de usar Protopic?
Caso você esqueça de aplicar a pomada no horário determinado, aplique assim que você lembrar e então continue conforme prescrito.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico ou cirurgião-dentista.
Precauções
A segurança de uso de Protopic por um logo período não é conhecida. Um pequeno número de pessoas que utilizaram Protopic pomada desenvolveu câncer (tais como, de pele ou linfoma). Entretanto, não foi estabelecida uma relação direta com o uso de Protopic pomada.
Se você possui lesões infecciosas, não aplique a pomada na pele lesionada.
Se você possui insuficiência hepática, consulte seu médico antes de fazer uso de Protopic.
Converse com seu médico antes de utilizar Protopic se você tiver qualquer câncer de pele (tumor) ou se você possui um sistema imune fraco (imunocomprometimento) por algum motivo.
Se você possui uma doença hereditária que comprometa a barreira de sua pele, tal como síndrome de Netherton, ou se você sofre de eritroderma generalizado (inflamação com vermelhidão e descamação de toda a pele), converse com seu médico antes de utilizar Protopic.
Você deve informar seu médico se você apresentar íngua (inchaço nos linfonodos) no início do tratamento. Se os seus linfonodos incharem ao longo do tratamento com Protopic, consulte seu médico.
Antes de tomar uma vacina, informe seu médico que você está fazendo uso de Protopic. Vacinas não devem ser aplicadas durante o tratamento e por um certo período após o tratamento com Protopic.
Para vacinas atenuadas (tais como, sarampo, caxumba, rubéola ou poliomielite oral) o período de espera deve ser de 28 dias após a vacinação; para vacinas inativadas (tais como tétano, difteria, coqueluche ou gripe) é de 14 dias após a vacinação.
Evite exposição da pele por longos períodos ao sol ou luz artificial, tal como, câmara de bronzeamento. Se você ficar muito tempo exposto em lugares abertos após aplicar Protopic, use protetor solar e roupas soltas que protejam a pele do sol. Além disso, peça conselhos ao seu médico sobre outros métodos de proteção solar apropriados. Se for prescrita a você terapia de luz, informe seu médico que você está fazendo uso de Protopic, já que não é recomendada esta terapia e o uso do medicamento ao mesmo tempo.
Evite o contato com olhos e mucosas (dentro do nariz ou boca).
Se o seu médico indicar Protopic duas vezes por semana para manter sua dermatite atópica controlada, sua condição deve ser revista pelo seu médico a cada 12 meses, mesmo que a doença permaneça sob controle.
Uso pediátrico
Este medicamento é contraindicado para menores de 2 anos.
Gravidez e amamentação
Este medicamento não deve ser utilizado por mulheres que estão amamentando sem orientação médica ou do cirurgião-dentista.
Durante o período de aleitamento materno ou doação de leite humano, só utilize medicamentos com o conhecimento do seu médico ou cirurgião-dentista, pois alguns medicamentos podem ser excretados no leite humano, causando reações indesejáveis no bebê.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Durante o uso de Protopic, a ingestão de bebidas alcoólicas pode causar rubor, vermelhidão ou calor na pele ou face.
Você deve utilizar cremes e loções hidratantes durante o tratamento com Protopic, mas estes produtos não devem ser utilizados dentro de duas horas após a aplicação de Protopic.
O uso de Protopic concomitantemente a outras preparações para serem utilizadas na pele ou durante o uso de corticosteroides via oral (como cortisona) ou medicamentos que afetem o sistema imune, não foi estudado.
Informe seu medico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento de seu médico. Pode ser perigoso para sua saúde.
Não use medicamento sem o conhecimento de seu médico. Pode ser perigoso para sua saúde
Reações Adversas
Assim como todos os medicamentos, Protopic pode causar efeitos colaterais, embora nem todas as pessoas os manifestem. Aproximadamente metade dos pacientes que utilizaram Protopic apresentou algum tipo de irritação na pele onde eles aplicaram a pomada.
Reações muito comuns (ocorre em mais que 10% dos pacientes que utilizaram o medicamento)
Sensação de queimação e coceira no local da aplicação. Estes sintomas são comumente leves a moderados e geralmente desaparecem após uma semana de uso de Protopic.
Reações comuns (ocorrem entre 1% a 10% dos pacientes que utilizaram o medicamento)
As seguintes reações ocorreram no local de aplicação
Aquecimento, vermelhidão, dor, irritação, parestesia (aumento da sensibilidade da pele ao frio, calor, sensação de formigamento e/ou pressão), dermatite (inflamação da pele), infecção incluindo, mas não limitado a, eczema herpético (lesão de pele causada por herpes), foliculite, herpes simples, lesão similar à varicela, impetigo (infecção superficial de pele).
Prurido (coceira), hiperestesia e disestesia (distúrbios neurológicos caracterizados pela alteração na sensibilidade de um sentido ou órgão a estímulos), sensação de queimação, intolerância ao álcool (rubor facial ou irritaçãona pele após o consumo de bebida alcoólica).
Reações incomuns (ocorre entre 0,1% a 1% dos pacientes que utilizam o medicamento)
Acne.
Reação com incidência desconhecida
Rosácea (doença de pele localizada na face e que se caracteriza por manchas avermelhadas e inflamações do tecido vascular do rosto). Para pacientes que fazem uso sistêmico de tacrolimo e possuem algum defeito na barreira da pele, foi observado aumento dos níveis de tacrolimo no sangue.
Tratamento de manutenção
Seguindo um tratamento de duas vezes por semana em crianças e adultos, foram relatadas infecções superficiais de pele no local de aplicação.
Desde a liberação ao comércio, uma pequena quantidade de pessoas que tem utilizado Protopic pomada desenvolveu câncer (por exemplo, pele e linfoma). Entretanto, não foi estabelecida uma relação direta desta doença com o uso de Protopic pomada.
Se alguns desses efeitos colaterais se tornarem graves, ou se você notar qualquer efeito colateral não informado nesta bula, por favor, entre em contato com seu médico ou farmacêutico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através de seu serviço de atendimento.
Atenção: Este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
Composição
Cada g de Protopic 0,03% contém:
0,3 mg de tacrolimo (equivalente a 0,306 mg de tacrolimo monoidratado).
Cada g de Protopic 0,1% contém:
1,0 mg de tacrolimo (equivalente a 1,02 mg tacrolimo monoidratado).
Excipientes
Petrolato branco, petrolato líquido, carbonato de propileno, cera branca, parafina sólida.
Superdosagem
Se você engolir acidentalmente a pomada, consulte um médico ou farmacêutico assim que possível. Não tente induzir o vômito.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
O uso concomitante de tacrolimo com medicamentos cujo efeito nefrotóxico ou neurotóxico é conhecido pode aumentar o nível de toxicidade. Já que o tratamento com tacrolimo pode ser associado com hiperpotassemia ou pode aumentar a hiperpotassemia preexistente, deve-se evitar o consumo elevado de potássio ou diuréticos poupadores de potássio.
Devido ao potencial para insuficiência renal aditiva ou sinérgica, é preciso cautela ao administrar tacrolimo com medicamentos que possam estar relacionados com disfunção renal. Esses medicamentos incluem, mas não estão limitados a, aminoglicosídeos, anfotericina B ou ibuprofeno e cisplatina.
Experimentos clínicos iniciais com a coadministração de tacrolimo e ciclosporina resultaram em nefrotoxicidade aditiva/sinérgica. Os pacientes que trocarem o tratamento com ciclosporina por tacrolimo só devem receber a primeira dose de tacrolimo 24 horas após a última dose de ciclosporina. A administração de tacrolimo deve ser adiada na presença de níveis elevados de ciclosporina.
Medicamentos que podem alterar as concentrações de tacrolimo
A terapia sistêmica com tacrolimo exige monitoramento atento quando coadministrada com medicamentos com interação potencial e, quando necessário, deve-se interromper ou ajustar a dose de tacrolimo.
Como tacrolimo é metabolizado principalmente pelo sistema enzimático CYP3A, substâncias que inibem estas enzimas podem reduzir o metabolismo ou aumentar a biodisponibilidade de tacrolimo, resultando em aumento nas concentrações plasmáticas ou no sangue total. Os fármacos que induzem estes sistemas enzimáticos podem aumentar o metabolismo ou diminuir a biodisponibilidade de tacrolimo, resultando em redução das concentrações no sangue total ou plasma. Monitoramento das concentrações sanguíneas e ajustes de dose são essenciais quando tais drogas são usadas concomitantemente:
Fármacos que podem aumentar as concentrações de tacrolimo no sangue
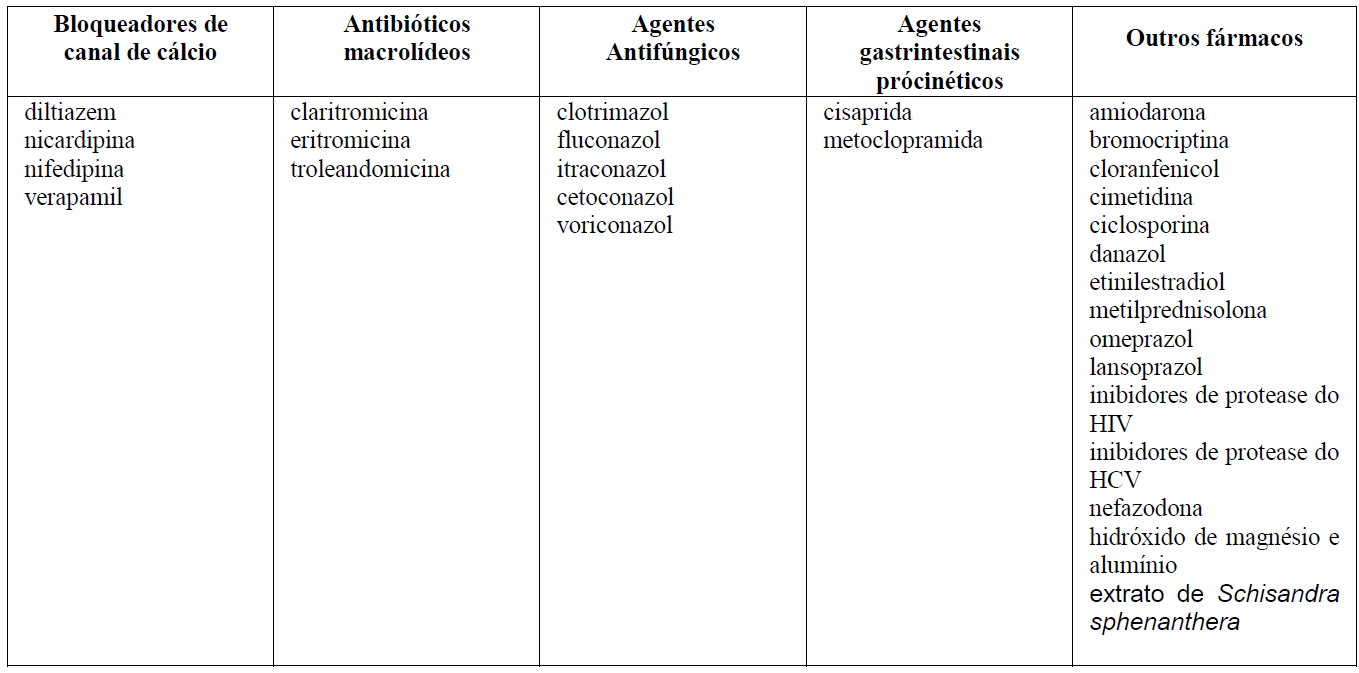
O tacrolimo também demonstrou efeito inibidor amplo e forte sobre o metabolismo dependente de CYP3A4. Assim, o uso concomitante de tacrolimo com fármacos conhecidamente metabolizados por vias dependentes de CYP3A4 pode afetar o metabolismo desses fármacos. O tacrolimo se liga de forma extensa à proteínas plasmáticas. Possíveis interações com outros fármacos com alta afinidade conhecida para proteínas plasmáticas devem ser consideradas.
O suco de toranja (grapefruit) afeta o metabolismo mediado por CPY3A, resultando em aumento da concentração de tacrolimo no sangue; portanto, deve ser evitado.
Reduções significativas da dose de tacrolimo e o prolongamento do intervalo de administração podem ser necessários quando coadministrado com fortes inibidores de CYP3A4, especialmente telaprevir. O monitoramento atento dos níveis de tacrolimo no sangue, além do monitoramento do prolongamento do intervalo QT com ECG, função renal e outros efeitos colaterais são fortemente recomendados.
O lansoprazol e omeprazol (CYP2C19, substrato de CYP3A4) tem o potencial de inibir o metabolismo do tacrolimo mediado por CYP3A4 e, portanto, aumentar consideravelmente as concentrações de tacrolimo no sangue total, especialmente em pacientes transplantados que são metabolizadores deficientes ou intermediários de CYP2C19, em comparação aos pacientes que metabolizam CYP2C19 de forma eficiente.
A cimetidina também pode inibir o metabolismo do CYP3A4 de tacrolimo e, assim, aumentar substancialmente as concentrações de tacrolimo no sangue total.
A maioria dos inibidores de protease inibe as enzimas de CYP3A e pode aumentar as concentrações de tacrolimo no sangue total. Recomenda-se evitar o uso concomitante de tacrolimo com nelfinavir, a menos que os benefícios justifiquem os riscos. As concentrações de tacrolimo no sangue total são acentuadamente elevadas quando há coadministração de telaprevir ou boceprevir.
Recomenda-se o monitoramento das concentrações de tacrolimo no sangue total e das reações adversas associadas ao tacrolimo, além de ajustes adequados no esquema de dose de tacrolimo quando tacrolimo e inibidores de protease (por exemplo, ritonavir, telaprevir, boceprevir) são usados concomitantemente.
Telaprevir:
Em um estudo de dose única com 9 voluntários saudáveis, a coadministração de tacrolimo (dose única de 0,5 mg) com telaprevir (750 mg três vezes por dia por 13 dias) elevou a Cmáx de tacrolimo normalizado por dose em 9,3 vezes e a AUC em 70 vezes em comparação ao tacrolimo isolado.
Boceprevir:
Em um estudo de dose única com 12 sujeitos de estudo, a coadministração de tacrolimo (dose única de 0,5 mg) com boceprevir (800 mg três vezes por dia por 11 dias) elevou a Cmáx de tacrolimo em 9,9 vezes e a AUC em 17 vezes em comparação ao tacrolimo em monoterapia.
Nelfinavir:
Com base em um estudo clínico com 5 receptores de transplante hepático, a coadministração de tacrolimo e nelfinavir aumentou as concentrações de tacrolimo no sangue de forma significativa e, como resultado, uma redução de 16 vezes, em média, da dose de tacrolimo foi necessária para manter as concentrações médias de vale de tacrolimo de 9,7 ng/mL. Recomenda-se evitar o uso concomitante de tacrolimo com nelfinavir, a menos que os benefícios justifiquem os riscos.
Hidróxido de Alumínio/Magnésio:
Em um estudo cruzado de dose única em pacientes sadios com coadministração oral de tacrolimo e hidróxido de alumínio e magnésio resultou em um aumento de 21% na AUC média do tacrolimo, e numa redução de 10% na Cmáx média de tacrolimo com relação a sua administração oral isolado.
Fármacos que podem diminuir a concentração do tacrolimo no sangue

A Erva de São João (Hypericum perforatum) induz o citocromo CYP3A4 e a glicoproteína P. Uma vez que o tacrolimo é substrato para o citocromo CYP3A4, há um potencial de que o uso da Erva de São João em pacientes recebendo tacrolimo possa resultar na redução dos níveis de tacrolimo.
Rifampicina:
Em um estudo com 6 voluntários normais observou-se uma significante redução na biodisponibilidade oral de tacrolimo (de 14 ± 6% para 7 ± 3%) quando administrado concomitantemente com rifampicina (600 mg). Além disso, houve um aumento significante da depuração do tacrolimo (de 0,036 ± 0,008 L/h/kg para 0,053 ± 0,010 L/h/kg) em administração concomitante com rifampicina.
O suco de toranja (grapefruit) afeta o metabolismo mediado por CPY3A, resultando em aumento da concentração de tacrolimo no sangue, portanto deve ser evitado.
Após a administração concomitante de tacrolimo e sirolimo (2 ou 5 mg/dia) em pacientes receptores de transplante renal estáveis, a AUC0-12 média e a Cmín reduziram em aproximadamente 30% com relação ao tacrolimo administrado isoladamente. Após a administração concomitante de tacrolimo e 1 mg/dia de sirolimo, a AUC0-12 média e a Cmín reduziram em aproximadamente 3% e 11%, respectivamente. A segurança e eficácia do uso do tacrolimo em combinação com o sirolimo para prevenção da rejeição a enxerto não foram estabelecidas, e seu uso não é recomendado.
Outras Interações Medicamentosas
Os imunossupressores podem afetar a vacinação. Portanto, durante o tratamento com tacrolimo, a vacinação pode ser menos eficaz. O uso de vacinas vivas deve ser evitado; vacinas vivas incluem, mas não são limitadas a vacina intranasal contra gripe, sarampo, caxumba, rubéola, poliomielite, BCG, febre amarela, varicela e tifoide TY21a.
Informe a seu paciente que, durante tratamento, o uso de vacinas exige avaliação do profissional de saúde.
Interação Alimentícia
A presença de alimentos afeta a absorção de tacrolimo. A taxa e a extensão da absorção de tacrolimo são maiores em condições de jejum.
A presença e a composição do alimento diminuíram tanto a taxa como a extensão da absorção de tacrolimo quando administrado em 15 voluntários sadios.
O efeito foi mais pronunciado com uma refeição rica em lipídios (848 kcal, 46% de lipídios): a AUC e a Cmáx médias diminuíram 37% e 77%, respectivamente; o Tmáx se prolongou 5 vezes.
Uma refeição rica em carboidratos (668 kcal, 85% de carboidratos) fez com que a AUC e a Cmáx médias fossem diminuídas em 28% e 65%, respectivamente.
Em voluntários sadios (n=16), o tempo da refeição também afetou a biodisponibilidade de tacrolimo. Quando administrado imediatamente após a refeição, a Cmáx média foi reduzida em 71% e a AUC média foi reduzida em 39% em relação às condições de jejum. Quando administrado 1,5 horas após a refeição, a Cmáx média foi reduzida em 63% e a AUC média foi reduzida em 39% em relação às condições de jejum.
Em 11 pacientes receptores de transplante hepático, tacrolimo administrado 15 minutos após um café da manhã rico em lipídios (400 kcal, 34% de lipídios), resultou em decréscimo da AUC (27 ± 18%) e da Cmáx (50 ± 19%), quando comparado às condições de jejum.
Ação da Substância
Resultados de eficácia
Transplante Hepático
A segurança e eficácia da imunossupressão baseada em tacrolimo após transplante ortotópico de fígado foram avaliadas em dois estudos prospectivos, multicêntricos, abertos e randomizados. O grupo controle ativo foi tratado com regime de imunossupressão baseado em ciclosporina. Ambos os estudos utilizaram concomitantemente corticosteroides adrenais como parte do regime imunossupressor. Tais estudos foram desenhados com o objetivo de avaliar se os regimes imunossupressores eram equivalentes, tendo como desfecho primário a sobrevida de 12 meses após o transplante do paciente e do enxerto. A terapia de imunossupressão baseada em tacrolimo se mostrou equivalente ao regime imunossupressor baseado em ciclosporina.
Em um ensaio envolvendo 529 pacientes em 12 centros nos Estados Unidos, antes da cirurgia 263 pacientes foram randomizados para o tratamento baseado em tacrolimo, enquanto 266 para o regime imunossupressor baseado em ciclosporina (CBIR). Em 10 dos 12 centros o mesmo protocolo de CBIR foi utilizado, enquanto 2 centros utilizaram protocolos diferentes. Este ensaio clínico excluiu pacientes com disfunção renal, falência hepática fulminante com encefalopatia estágio IV e câncer. Foi permitida a inclusão de pacientes pediátricos (idade ?12 anos).
Em um segundo ensaio clínico, 545 pacientes foram incluídos em 8 centros na Europa, antes da cirurgia 270 pacientes foram randomizados para o tratamento baseado em tacrolimo, enquanto 275 para CBIR. Neste estudo cada centro utilizou o próprio protocolo padrão de CBIR no braço controle-ativo. Não foram incluídos pacientes pediátricos, mas permitia a inclusão de indivíduos com disfunção renal, falência hepática fulminante com encefalopatia estágio IV e outros cânceres com metástases além do primário hepático.
As sobrevidas do paciente e do enxerto após 1 ano do transplante no grupo com regime imunossupressor baseado em tacrolimo são equivalentes àquelas observadas nos grupos tratados com CBIR em ambos os estudos. A sobrevida geral do paciente (grupos recebendo regime imunossupressor baseado em tacrolimo e CBIR combinados) foi de 88% no estudo americano e 78% no estudo europeu.
A sobrevida geral do enxerto após 1 ano do transplante (grupos recebendo regime imunossupressor baseado em tacrolimo e CBIR combinados) foi de 81% no estudo americano e 73% no estudo europeu. Nos dois estudos a mediana de tempo de conversão da via de administração do tacrolimo de IV para oral foi de 2 dias.
Devido a natureza e desenho dos estudos, a comparação de desfechos secundários, como incidência de rejeição aguda, rejeição refratária ou uso de OKT3 para rejeição esteroide-resistente, não pôde ser realizada adequadamente.
Transplante Renal
Foi realizado um estudo clínico de fase III, prospectivo, randomizado, aberto, multicêntrico, com imunossupressão baseada em tacrolimo após transplante renal. Foram incluídos 412 pacientes receptores de transplante renal em 19 centros de estudo nos Estados Unidos. A terapia iniciou-se assim que a função renal foi estabelecida, como indicado pela creatinina sérica < 4 mg/dL (mediana de 4 dias após o transplante, intervalo de 1 a 14 dias). Pacientes com menos de 6 anos de idade foram excluídos do ensaio.
Neste estudo foram incluídos 205 pacientes no grupo que recebeu imunossupressão baseada em tacrolimo, enquanto 207 pacientes foram randomizados para o grupo recebendo regime de imunossupressão com ciclosporina. Todos os pacientes receberam terapia de indução profilática, composta de uma preparação de anticorpos antilinfócito, corticosteroides e azatioprina.
As sobrevidas gerais de 1 ano dos pacientes e do enxerto foi de 96,1% e 89,6%, respectivamente, e foi equivalentes entre os dois tratamentos do estudo.
Devido a natureza do desenho dos estudos, a comparação de desfechos secundários, como incidência de rejeição aguda, rejeição refratária ou uso de OKT-3 para rejeição esteroide-resistente, não pôde ser realizada adequadamente.
Características farmacológicas
Propriedades Farmacodinâmicas
O tacrolimo prolonga a sobrevivência do hospedeiro e órgãos transplantados em modelos animais de transplantes de fígado, rins, coração, medula óssea, intestino delgado e pâncreas, pulmão e traqueia, pele, córnea e membros.
Em animais, demonstrou-se que tacrolimo causa supressão da imunidade humoral e, com maior extensão, as reações mediadas por células tais como a rejeição alográfica, hipersensibilidade do tipo tardia, artrite induzida por colágeno, encefalomielite alérgica experimental e doença do enxerto contra hospedeiro.
Mecanismo de ação
À nível molecular, os efeitos do tacrolimo parecem ser mediados através da ligação à uma proteína citosólica (FKBP12), responsável pelo acúmulo intracelular do composto. O complexo FKBP12-tacrolimo liga-se especificamente competitivamente à calcineurina inibindo-alevando a uma inibição dependente de cálcio das vias de transdução de sinal das células Ta transcrição de um conjunto distinto de genes de citocinae. Dessa forma, evita-se. a transcrição de um conjunto distinto de genes de citocina.
Tacrolimo é um agente imunossupressor altamente potente e que demonstra sua atividade tanto in vitro quanto in vivo.
Em particular, o tacrolimo inibe a formação de linfócitos citotóxicos que são principalmente responsáveis pela rejeição do enxerto.
O tacrolimo suprime a ativação das células T, a proliferação de células T-helper dependentes de células B, bem como a formação de linfoquinas (tais como interleucinas-2, -3 e e a expressão do receptor de interleucina-2. interferon gama) e a expressão do receptor de interleucina-2.
Propriedades Farmacocinéticas
A atividade do tacrolimo é devida, principalmente, ao fármaco-mãe. Os parâmetros farmacocinéticos do tacrolimo foram determinados após administração intravenosa e oral em voluntários sadios, em pacientes receptores de transplante renal e em pacientes receptores de transplante hepático.
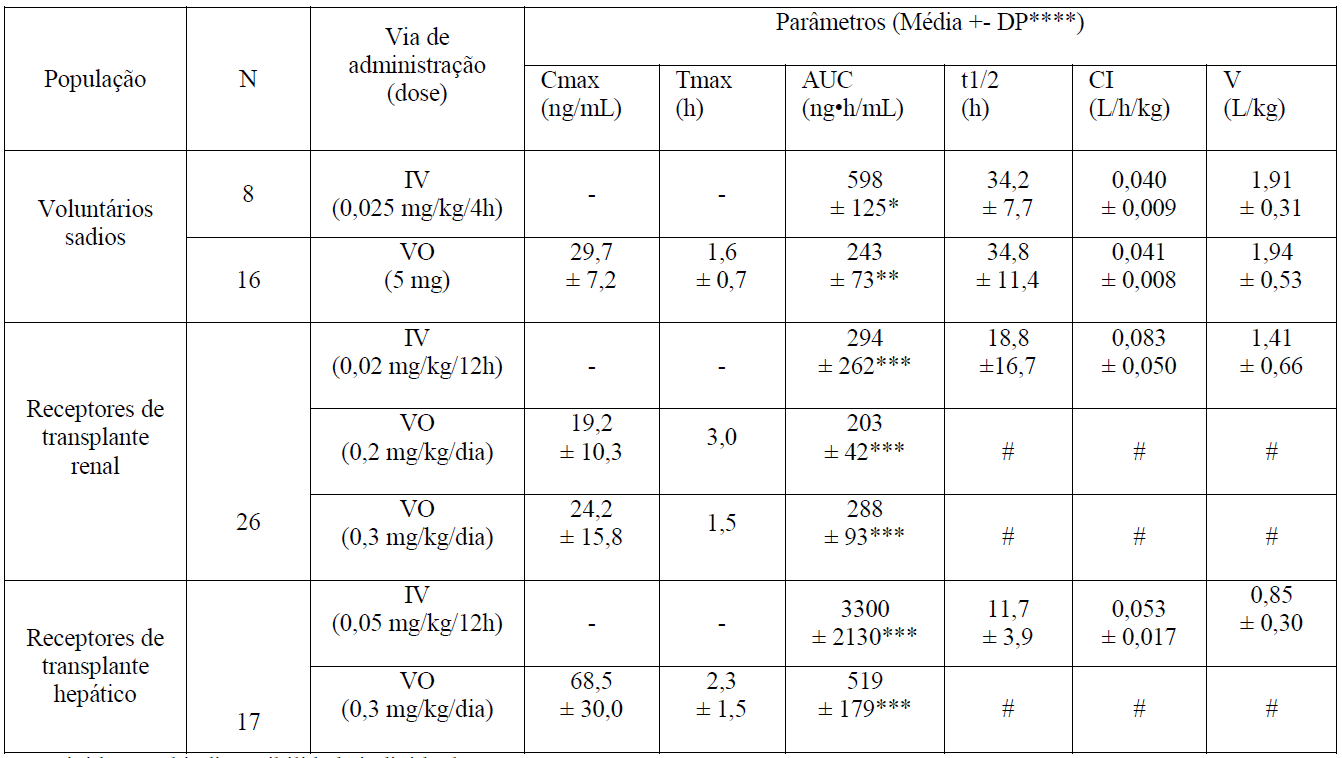
Corrigido para biodisponibilidade individual.
*AUC0-120.
**AUC0-72.
***AUC0-inf.
****DP = Desvio Padrão.
- Não aplicável.
#Dado indisponível.
Devido à variabilidade inter-sujeitos na farmacocinética do tacrolimo, é necessária a individualização da posologia para a otimização da terapia. Os dados farmacocinéticos indicam que as concentrações no sangue total, e não as concentrações plasmáticas, representam o compartimento de amostragem mais apropriado para descrever a farmacocinética do tacrolimo.
Absorção
No homem, o tacrolimo demonstrou ser absorvido ao longo do trato gastrointestinal.
Após a administração oral de tacrolimo cápsulas, as concentrações máximas (Cmáx) de tacrolimo no sangue são atingidas em cerca de 1 - 3 horas. Em alguns pacientes, o tacrolimo parece ser absorvido continuamente durante um período prolongado, originando um perfil de absorção relativamente estável. A biodisponibilidade oral média do tacrolimo varia entre 20% - 25%.
Após a administração oral (0,30 mg/kg/dia) em pacientes submetidos à transplante de fígado, as concentrações de estado equilíbrio de tacrolimo foram atingidas dentro de 3 dias na maioria dos pacientes.
Em voluntários sadios, as cápsulas tacrolimo 0,5 mg, tacrolimo 1 mg e tacrolimo 5 mg mostraram-se bioequivalentes, quando administradas em doses equivalentes.
A taxa e extensão da absorção de tacrolimo é maior sob condições de jejum. A presença de alimentos diminui a taxa e a extensão da absorção do tacrolimo, o efeito é mais pronunciado após uma refeição rica em lipídios. O efeito de uma refeição rica em carboidratos é menos pronunciado.
Em pacientes estáveis submetidos ao transplante de fígado, a biodisponibilidade oral de tacrolimo foi reduzida quando administrado após uma refeição com uma quantidade moderada de lipídios (34% de calorias). Diminuições da AUC (27%) e da Cmáx (50%) e um aumento do Tmáx (173%) no sangue total foram evidentes.
Em um estudo com pacientes estáveis submetidos ao transplante renal e que receberam tacrolimo imediatamente após um café da manhã habitual, o efeito na biodisponibilidade oral foi menos pronunciado. Diminuições da AUC (2 a 12%) e da Cmáx (15 a 38%), e um aumento do Tmáx (38 a 80%) no sangue total foram evidentes.
O fluxo biliar não influencia a absorção de tacrolimo.
Existe forte correlação entre a AUC e os níveis mínimos no sangue total no estado de equilíbrio. Monitoramento dos níveis no sangue total fornece uma boa estimativa da exposição sistêmica.
Distribuição e eliminação
No homem, a distribuição de tacrolimo após infusão intravenosa pode ser descrita como bifásica.
Na circulação sistêmica, o tacrolimo liga-se fortemente aos eritrócitos, resultando em uma proporção de distribuição das concentrações de sangue total / plasma de aproximadamente 20:1.
No plasma, o tacrolimo é altamente ligado às proteínas plasmáticas (> 98,8%), principalmente à albumina sérica e à ?-1-glicoproteína ácida.
O tacrolimo é amplamente distribuído no organismo. O volume de distribuição no estado de equilíbrio, com base nas concentrações plasmáticas, é de aproximadamente 1.300 L (indivíduos sadios). Dados correspondentes derivados do sangue total foram em média de 47,6 L.
O tacrolimo é uma substância com baixa depuração. Em indivíduos sadios, a média da depuração corporal total, estimada a partir de concentrações no sangue total, foi de 2,25 L/h. Em pacientes adultos submetidos ao transplante de fígado, rim e de coração, foram observados os valores de 4,1 L/h, 6,7 L/h e 3,9 L/h, respectivamente.
Receptores pediátricos de transplante de fígado apresentaram uma depuração corporal total aproximadamente duas vezes maior que aquela apresentada por pacientes adultos submetidos ao transplante de fígado. Fatores como baixos níveis de hematócrito e de proteínas, que resultam em um aumento na fração não ligada de tacrolimo, ou aumento do metabolismo induzido por corticosteroides, são considerados como responsáveis pelas taxas de depuração superiores observadas após o transplante.
A meia-vida do tacrolimo é longa e variável. Em indivíduos saudáveis, a meia-vida média no sangue total é de aproximadamente 43 horas. Em pacientes adultos e pediátricos submetidos ao transplante de fígado, a média foi de 11,7 horas e de 12,4 horas, respectivamente, em comparação com 15,6 horas em receptores adultos de transplante renal. As taxas de depuração aumentadas contribuem para a meia-vida mais curta observada em receptores de transplantes.
Metabolismo e Biotransformação
O tacrolimo é extensivamente metabolizado no fígado, principalmente pelo citocromo P450-3A4. O tacrolimo é também consideravelmente metabolizado na parede intestinal. Existem vários metabólitos identificados. Apenas um deles demonstrou ter atividade imunossupressora in vitro semelhante ao tacrolimo. Os outros metabólitos têm apenas fraca ou nenhuma atividade imunossupressora. Na circulação sistêmica, apenas um dos metabólitos inativos está presente em baixas concentrações. Portanto, os metabólitos não contribuem para a atividade farmacológica do tacrolimo.
Excreção
Após a administração intravenosa e oral de tacrolimo marcado com 14C, a maior parte da radioatividade foi eliminada nas fezes.
Aproximadamente 2% da radioatividade foi eliminada na urina. Menos de 1% de tacrolimo inalterado foi detectado na urina e nas fezes, indicando que o tacrolimo é quase que completamente metabolizado antes da eliminação: a bile foi a principal via de eliminação.
Dados Pré-clínicos de Segurança
Os rins e o pâncreas foram os principais órgãos afetados nos estudos de toxicidade realizados em ratos e babuínos. Em ratos, o tacrolimo causou efeitos tóxicos para o sistema nervoso e olhos. Efeitos cardiotóxicos reversíveis foram observados em coelhos após a administração intravenosa de tacrolimo.
Toxicidade embriofetal foi observada em ratos e coelhos e esteve limitada à doses que causaram toxicidade significativa nas progenitoras. Em ratos, a função reprodutora feminina, incluindo o nascimento, foi debilitada em doses tóxicas e a prole apresentou peso, viabilidade e crescimento reduzidos ao nascimento.
Foi observado um efeito negativo do tacrolimo na fertilidade masculina em ratos, sob a forma de contagem reduzida e da motilidade dos espermatozoides.
Populações especiais
Pacientes Pediátricos
A farmacocinética do tacrolimo, foi estudada em pacientes receptores de transplante hepático, com idades entre 0,7 e 13,2 anos. Após administração via intravenosa de uma dose de 0,037 mg/kg/dia em 12 pacientes pediátricos, a meia-vida terminal média, o volume de distribuição médio e a depuração média foram de 11,5 ± 3,8 horas, 2,6 ± 2,1 L/kg e 0,138 ± 0,071 L/h/kg, respectivamente.
Após administração oral em 9 pacientes, a AUC e a Cmáx médias foram 337 ± 167 ng•h/mL e 43,4 ± 27,9 ng/mL, respectivamente. A biodisponibilidade absoluta foi 31 ± 21%.
Após a administração de tacrolimo, as concentrações mínimas no sangue total de 31 pacientes com menos de 12 anos de idade mostraram que pacientes pediátricos necessitam de doses mais elevadas que os adultos para alcançar uma concentração mínima similar de tacrolimo.
A farmacocinética de tacrolimo também foi estudada em pacientes submetidos ao transplante de rim, com idade de 8,2 ± 2,4 anos.
Após administração via intravenosa de uma dose de 0,06 mg/kg/dia (variação de 0,06 – 0,09) em 12 pacientes pediátricos (8 do sexo masculino e 4 do sexo feminino), a meia-vida terminal média e a depuração média foram de 10,2 ± 5,0 horas (variação de 3,4 – 25) e de 0,12 ± 0,04 L/h/kg (variação de 0,06 – 0,17), respectivamente. Após a administração oral aos mesmos pacientes, a AUC e Cmáx médias foram de 181 ± 65 ng•h/mL (variação de 81 – 300) e 30 ± 11 ng/mL (variação de 14 – 49), respectivamente. A biodisponibilidade absoluta foi de 19 ± 14 % (variação de 5,2 – 56).
Pacientes com Insuficiência Hepática e Renal
As médias dos parâmetros farmacocinéticos do tacrolimo, após administração única em pacientes com insuficiência hepática e renal, são dadas na tabela abaixo.
Farmacocinética em Pacientes com Insuficiência Renal e Hepática
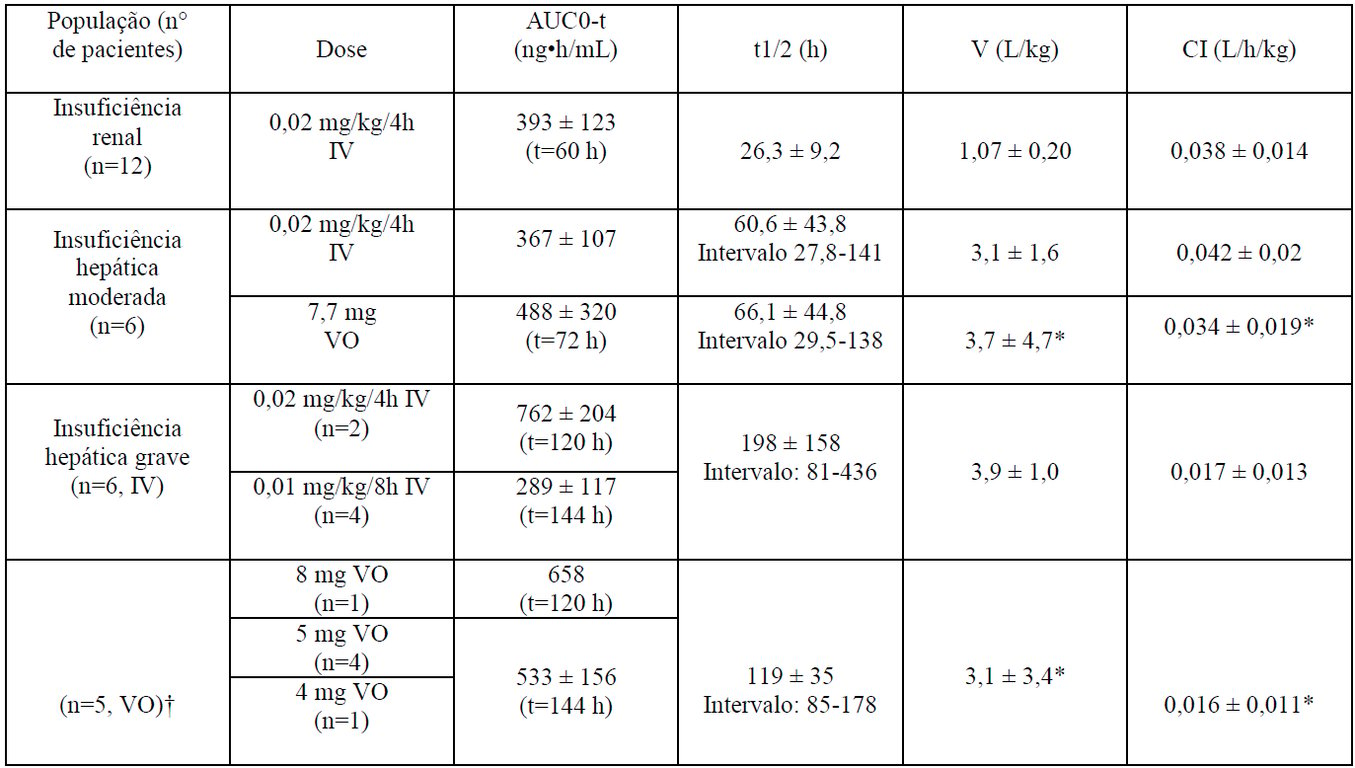
*Corrigida para biodisponibilidade.
†1 paciente não recebeu a dose por via oral.
IV: intravenosa VO: via oral.
Pacientes com Insuficiência Renal
A farmacocinética do tacrolimo após a administração de dose única intravenosa foi determinada em 12 pacientes (7 não estavam em diálise e 5 em diálise, creatinina sérica de 3,9±1,6 e 12,0±2,4 mg/dL, respectivamente) anteriormente ao transplante renal. Os parâmetros farmacocinéticos obtidos foram similares em ambos os grupos.
A depuração média de tacrolimo em pacientes com disfunção renal foi similar a de voluntários normais.
Pacientes com Insuficiência Hepática
A farmacocinética do tacrolimo foi determinada em 6 pacientes com disfunção hepática leve (média do escore de Pugh: 6,2) após administrações de dose única via oral e intravenosa. A depuração média de tacrolimo em pacientes com disfunção hepática leve não foi substancialmente diferente da depuração de voluntários normais.
A farmacocinética do tacrolimo foi estudada em 6 pacientes com disfunção hepática grave (média do escore de Pugh: > 10). A depuração média foi substancialmente menor nos pacientes com disfunção hepática grave, independentemente da via de administração.
Raça
A farmacocinética do tacrolimo foi estudada após uma única administração intravenosa e oral de tacrolimo aos seguintes voluntários sadios: 10 negros, 12 latino-americanos e 10 caucasianos.
Não houve diferenças farmacocinéticas significativas entre os três grupos étnicos após uma infusão IV de 0,015 mg / kg por 4 horas. Entretanto, após uma única administração oral de 5 mg, a Cmáx ± DP de tacrolimo em negros (± 12,1 ng / mL) foi significativamente menor que em caucasianos (40,2 ± 12,6 ng / mL) e em latinoamericanos (36,2 ± 15,8 ng / mL)( p< 0,01).
A AUC0-inf média tendeu a ser menor em negros (203 ± 115 ng •h / mL) que em caucasianos (344 ± 186 ng • h / mL) e latinoamericanos (274 ± 150 ng •h / mL).
A média da biodisponibilidade oral absoluta (F) (± DP) em negros (12 ± 4,5%) e latino-americanos (14 ± 7,4%) foi significativamente menor que em caucasianos (19 ± 5,8%, p = 0,011).
Não houve diferença significativa na média do T½ terminal entre os três grupos étnicos (variação de aproximadamente 25 a 30 horas).
A comparação retrospectiva dos pacientes negros e caucasianos submetidos ao transplante de rim indicou que os pacientes negros necessitavam de doses mais elevadas de tacrolimo para atingirem concentrações mínimas semelhantes.
Sexo
Não foi conduzido estudo formal para avaliar o efeito do sexo na farmacocinética de tacrolimo. No entanto, não se observa diferença na dosagem por sexo nos estudos clínicos envolvendo transplante renal. Uma comparação retrospectiva da farmacocinética em voluntários sadios, pacientes receptores de transplante renal e pacientes receptores de transplante hepático indicam que não há diferenças relacionadas ao sexo.
Cuidados de Armazenamento
Você deve conservar Protopic em temperatura ambiente (15 - 30 °C).
Este medicamento tem validade de 24 meses a partir de sua data de fabricação.
A data de validade refere-se ao ultimo dia do mês.
Certifique-se que a tampa da bisnaga esteja devidamente fechada.
Nunca deixe Protopic no porta-luvas do carro.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use este medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Todo medicamento deve ser mantido fora do alcance das crianças.
Características organolépticas
Protopic é uma pomada branca a levemente amarelada.
Protopic 0,03%
Está disponível em cartucho e bisnaga com uma faixa na cor verde claro.
Protopic 0,1%
Está disponível em cartucho e bisnaga com uma faixa na cor azul claro.
Antes de usar, observe o aspecto do medicamento Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto do medicamento, consulte o médico ou o farmacêutico para saber se poderá utilizá-lo.
Dizeres Legais
Registro MS-1.7717.0004.
Farmacêutico Responsável:
Sandra Winarski
CRF-SP: 18.496.
Fabricado por:
Astellas Pharma Tech Co., Ltd.
2-178, Kojin-machi – Toyama City
Toyama – 930- 0809 – Japão.
Registrado e importado por:
Astellas Farma Brasil Importação e Distribuição de Medicamentos Ltda.
Av. Guido Caloi, 1935, Bloco B, 2o andar
Santo Amaro, CEP: 05802-140
São Paulo – SP.
CNPJ 07.768.134/0001-04.
Venda sob prescrição médica.