SUPRAHYAL DUO 10MG/ML C/1 SER PREE 2,5ML na Farma Visa
Suprahyal Duo 10Mg/Ml Injetável 2,5Ml + Seringa

SUPRAHYAL DUO 10MG/ML C/1 SER PREE 2,5ML na Farma Visa
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Confira os menores preços para Suprahyal Duo 10Mg/Ml Injetável 2,5Ml + Seringa

Suprahyal Duo 10Mg/Ml Injetável 2,5Ml + Seringa
69.51%
R$ 290,91
Life Medicamentos
32.00%
R$ 648,70
Farma Visa
32.00%
R$ 648,70
Imune Farma Medicamentos Especiais
31.99%
R$ 648,80
Farma Ame
31.99%
R$ 648,85
Para que serve
Suprahyal Duo é indicado na osteoartrite de joelho e no ombro doloroso.
Também está indicado na osteoartrose trapeziometacarpiana (rizartrose) de graus I, II, e III e nos quadros de dor e limitação funcional por alterações degenerativas e traumáticas de outras articulações sinoviais.
Como Suprahyal Duo funciona?
O hialuronato de sódio é um polímero natural pertencente à classe dos glicosaminoglicanos (mucopolissacáridos ácidos) largamente distribuídos nos tecidos conjuntivos animais e humanos.
É um polissacárido composto por unidades repetidas do dissacárido formado pela N-acetilglucosamina e pelo glucuronato sódico unidos por pontes glucosídicas alternantes ß-1,3 e ß-1,4.
É um composto majoritário do fluido articular e desempenha um importante papel nas suas funções fisiológicas.
O Suprahyal Duo é uma solução estéril a 1% de hialuronato sódico obtido a partir do Streptococcus zooepidemicus por um processo de fermentação e posterior purificação.
Caracteriza-se pela sua viscoelasticidade, higroscopicidade e propriedades lubrificantes.
A ação intra-articular de Suprahyal Duo permite melhorar a função articular, aliviando a dor produzida pela artrose e artrite; melhora a mobilidade articular e normaliza o líquido sinovial alterado.
O Suprahyal Duo está disponível na forma de seringa descartável previamente preparada, a qual facilita a administração, mantém a esterilidade e previne a contaminação por partículas durante a sua utilização.
Contraindicação
Este produto esta contraindicado em pacientes com hipersensibilidade ao hialuronato sódico. Em pacientes pediátricos, gestantes e durante o período de amamentação.
Como usar
Instruções de utilização da seringa
- Retire a seringa do blister. Caso seja conservado em geladeira (ver condições de armazenamento), retirar a embalagem 20 a 30 minutos antes da utilização.
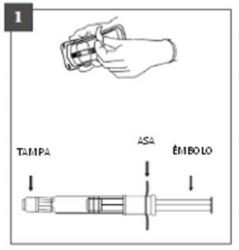
- Retirar a tampa rodando.
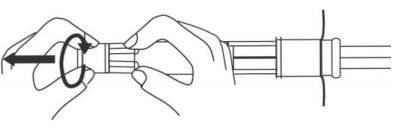
- Colocar uma agulha para injeção (21 a 23G).
?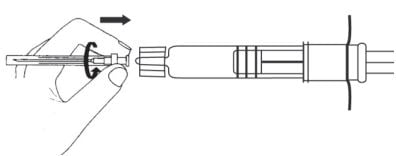
- A seringa esta pronta a ser utilizada.
*Antes da administração, desinfectar cuidadosamente o local de injecção.
*Após a administração, a seringa e a agulha podem ser rejeitadas separadamente.
Descarte
Os produtos inadequados para uso devem ser inutilizados de forma a assegurar a completa descaracterização do mesmo, impedindo qualquer possibilidade de sua reutilização.
A identificação e descarte são de responsabilidade de cada local, que deve levar em consideração seu plano de gerenciamento de resíduos, obedecendo normativas ambientais estabelecidas ANVISA e orientações locais do comitê de controle de infecções.
A agulha deve ser descartada em local adequado para componentes perfuro cortantes.
Rastreabilidade
A rastreabilidade é assegurada por um conjunto de 03 etiquetas adesivas fornecidas na embalagem, junto com o produto, trazendo as informações de nome do produto, modelo, tamanho, número de lote, identificação do fabricante e número de registro na ANVISA. Dessa forma é possível fazer o caminho reverso e atingir a produção, matéria-prima, fornecedor e demais itens de controle de qualidade estabelecidos no plano geral de qualidade do Fabricante.
É responsabilidade da equipe médica e do local (os depositários das informações e prontuários do paciente) a disponibilização e fixação das etiquetas no prontuário clínico, no documento a ser entregue ao paciente e na documentação fiscal que gera a cobrança.
O médico deverá orientar o paciente a guardar o laudo entregue a ele após a cirurgia, explicando que o documento possui uma etiqueta de identificação do produto implantado.
As etiquetas têm como objetivo fornecer rastreabilidade do produto implantado.
Em caso de ocorrência de efeitos adversos, o médico ou o paciente deverá reportar ao distribuidor do produto no Brasil e ao órgão sanitário competente, Agência Nacional de Vigilância Sanitária, através do site www.anvisa.gov.br.
Embalagem
Inspecione cada embalagem antes do uso e não use o componente caso o lacre tenha sido danificado ou violado ou se a data de validade tenha se excedido. Inspecionar a embalagem, bem como o estado do produto, para verificar a integridade estrutural antes de utilizar.
Queda ou qualquer tipo de dano ao produto e/ou a embalagem, mesmo que superficial, inviabilizam o uso do produto.
Transportar e ou manusear com atenção e cuidado.
Posologia
Normalmente, recomenda-se uma infiltração por via intra-articular uma vez por semana durante 5 semanas consecutivas.
A administração deverá realizar-se no espaço intra-articular da articulação do joelho, da articulação do ombro (espaço intra-articular da articulação do ombro, bolsa subacromial ou bainha da poção larga do tendão do bíceps braquial), da articulação trapezio-metacarpiana ou da articulação sinovial afetada.
No caso da articulação trapezio-metacarpiana, recomendam-se duas técnicas de administração dependendo do grau de artrose: via lateral externa (Rizartrose de Grau I) e via interdigital/primeira comissura (Rizartrose de Graus II e III). No entanto, a utilização de uma técnica ou de outra depende de cada caso em particular, recomendando-se, para maior facilidade, que se realize a administração sob visão endoscópica.
Em todos os casos, a dose deverá ser ajustada em função da gravidade dos sintomas.
Dados clínicos recentes (estudo AMELIA) mostraram os efeitos benéficos a longo prazo de Suprahyal Duo decorridos 3,4 anos de tratamento, na melhoria dos sintomas da osteoartrite do joelho, utilizando um ciclo de Suprahyal Duo por ano.
Precauções
Este produto pode agravar a inflamação local nos pacientes com artrose do joelho que apresentem simultaneamente inflamação e derrame da articulação. Assim, recomenda·se a administração deste produto após tratamento da inflamação.
Raramente poderá ocorrer dor local após a administração do produto.
Para evitar a dor após a injeção, aconselha·se manter em repouso a zona onde se efetuou a administração.
O produto deve ser administrado exatamente no espaço intra-articular, pois, caso contrário, pode causar dor.
A administração a pacientes com hipersensibilidade a outros medicamentos e insuficiência hepática deverá ser feita com cuidado.
Injeção
Dado que o produto se injeta na articulação, todo o processo deverá realizar-se em estritas condições de assepsia.
Suspender o tratamento se não se observar melhoria dos sintomas no fim do primeiro ciclo de 5 semanas.
Se observarem pequenas retenções de líquido sinovial, drená-lo por artrocentese.
Outras
Ter o cuidado de não injetar o produto nos vasos.
Não aplicar o produto nos olhos.
Dada a viscosidade da solução, recomenda-se a utilização de agulhas de 21-23 G.
Caso seja conservado em geladeira, deve permitir que o produto atinja a temperatura ambiente antes da sua utilização.
Utilizar o produto imediatamente depois de abrir; caso contrário não se poderá garantir a sua esterilidade.
O produto deve ser utilizado apenas uma vez e sempre num único paciente, descartando o produto restante. Caso contrário, poderiam ocorrer infecções cruzadas.
Reações Adversas
Raramente alguns pacientes desenvolveram erupções cutâneas, como urticária e prurido. Nestes casos deve-se suprimir a administração e dar ao paciente tratamento adequado.
Dor (geralmente transitória após a administração) e inchaço no local da injeção foram descritos com pouca frequência.
Ocasionalmente pode ocorrer hidropisia, enrubescimento, sensação de calor e de peso no local da injeção.
Muito raramente pode ocorrer o aparecimento de choque, situação em que deve-se suspender a administração, vigiar atentamente o paciente e tratá-lo adequadamente.
População Especial
Utilização em idosos
O produto deverá ser administrado com cuidado, uma vez que estes pacientes apresentam funções fisiológicas geralmente diminuídas.
Composição
Cada 1mL Contém:
| Hialuronato de Sódio | 10mg |
| Cloreto de Sódio | 8,52mg |
| Fosfato dissódico | 0,6mg |
Excipientes: Ácido Clorídrico, Hidróxido de Sódio e Água para Injetáveis, q.b.
Produto de uso único, proibido reprocessar.
Interação Medicamentosa
Deve-se evitar o uso concomitante com produtos que contenham sais de amônio quaternário em sua composição (cloreto de benzalcônio ou clorohexidina), pois pode ocorrer precipitação do ácido hialurônico.
Deve-se evitar a utilização concomitante de anestésicos locais e/ou outros medicamentos de uso intra-articular, sob o risco de diluição de Hialuronato De Sódio, o que pode comprometer sua ação.
Até o momento, não foram detectadas interações de Hialuronato De Sódio com outros fármacos.
Interação Alimentícia
Não há relatos até o momento.
Ação da Substância
Resultados de eficácia
Maheu et al. (2002) realizaram revisão sistemática da literatura que avaliou os resultados de 24 estudos clínicos que empregaram a injeção intra-articular de hialuronato de sódio 20 mg no tratamento de osteoartrite de joelho. O início da melhora do quadro clínico normalmente ocorreu após 3-4 semanas e o efeito terapêutico permaneceu por no mínimo 6 meses, sendo possível prolongar-se por até 1 ano após o término do tratamento. Os autores concluíram que ciclos de tratamento com 3 a 5 injeções com periodicidade semanal melhoraram significantemente a dor e os índices funcionais desses pacientes.
Estudo multicêntrico, controlado e randomizado, realizado por Altman e Moskowitz (1998), demonstrou a eficácia de aplicações intra-articulares semanais de hialuronato de sódio 20 mg, durante 5 semanas, no alívio da dor em pacientes com osteoartrite de joelho. Além disso, Kolarz et al. (2003) confirmaram a eficácia e a boa tolerabilidade de 1 ciclo de tratamento dos sintomas da osteoartrite de joelho, com 5 injeções intra-articulares de hialuronato de sódio 20 mg.
Em alguns estudos, a administração semanal intra-articular de 1 injeção de Hialuronato De Sódio, durante 3 semanas, comprovou ser eficiente em proporcionar efeitos benéficos na cartilagem e na viscossuplementação da articulação, com significante redução da dor em pacientes acompanhados durante 60 dias. Em estudo controlado, randomizado e duplo-cego realizado por Carrabba et al. (1995), foi verificado que a administração intra-articular de 3 a 5 injeções de hialuronato de sódio 20 mg foi eficaz no tratamento de pacientes com osteoartrite de joelho, produzindo efeito terapêutico persistente durante 60 dias de acompanhamento.
Nesse sentido, estudo controlado e duplo-cego, realizado por Grecomoro et al. (1987), também confirmou a eficácia terapêutica duradoura do tratamento intra-articular semanal de hialuronato de sódio 20 mg, durante 3 semanas, em pacientes com osteoartrite de joelho. A redução da intensidade de dor espontânea, de dor a palpação e de dor ao caminhar produzida, permaneceu por longos períodos após o término do tratamento com hialuronato de sódio.
Estudo multicêntrico, controlado, randomizado e duplo-cego, realizado por Blaine et al. (2008), avaliou a eficácia e a segurança do uso intra-articular de hialuronato de sódio no tratamento da dor persistente no ombro, resultante da ocorrência de osteoartrite. Foram recrutados 660 pacientes, dos quais 495 completaram o estudo durante 26 semanas de acompanhamento. Os autores confirmaram que o uso intra-articular semanal de 3 ou 5 aplicações de hialuronato de sódio 20 mg foi efetivo e bem tolerado no tratamento da osteoartrite e da dor persistente no ombro, sendo uma boa intervenção terapêutica não cirúrgica.
Estudo duplo-cego, controlado e randomizado, avaliou a eficácia do hialuronato de sódio no tratamento da osteoartrite do tornozelo. Nesta pesquisa, 20 pacientes receberam administração semanal intra-articular de hialuronato de sódio. Os resultados indicaram que Hialuronato De Sódio foi útil e bem tolerado no tratamento sintomático dos pacientes com osteoartrite de tornozelo (Salk et al., 2006). Schumacher et al. (2004) demonstraram que 5 injeções de hialuronato de sódio 20 mg, administradas pela via intra-articular em intervalos de 1 semana, foram capazes de melhorar a sintomatologia álgica de pacientes com osteoartrite na articulação carpometacarpiana.
Bragantini e Molinaroli (1994) avaliaram a eficácia e segurança da aplicação intra-articular de hialuronato de sódio em 44 pacientes com osteoartrite de quadril. Cinquenta articulações foram tratadas com 3 a 5 injeções intra-articulares de Hialuronato De Sódio. As injeções foram administradas uma vez por semana. Os resultados demonstraram que o tratamento foi significantemente efetivo no controle da dor e aumentou a mobilidade articular em 68% dos pacientes. Essa melhora nos parâmetros avaliados persistiu durante os 180 dias de acompanhamento, após o término das aplicações. O tratamento apresentou boa tolerabilidade e somente 1 paciente relatou aumento de dor na articulação tratada após a primeira injeção.
Em 2005, Guarda-Nardini et al. investigaram os efeitos do hialuronato de sódio no tratamento de doenças degenerativas da articulação temporomandibular. Os vinte pacientes com essa patologia que foram tratados semanalmente com 1 injeção intra-articular de Hialuronato De Sódio, durante 5 semanas, apresentaram melhora na abertura da boca, na redução da dor e na eficiência de mastigação. Isso indicou que a infiltração de hialuronato de sódio é um tratamento não cirúrgico útil e bem tolerado de doenças degenerativas da articulação temporomandibular.
Características farmacológicas
Hialuronato De Sódio contém o sal sódico do ácido hialurônico, um polímero natural da família dos glicosaminoglicanos (ácido mucopolissacáride). É importante constituinte da matriz extracelular e está presente, em concentrações particularmente elevadas, nas cartilagens e no líquido sinovial. A substância ativa de Hialuronato De Sódio é uma fração definida do ácido hialurônico, obtida com elevado grau de pureza através de filtração molecular a partir de material biológico.
Este fato contribui com propriedades bioquímicas, físico-químicas e farmacológicas especiais. Hialuronato De Sódio demonstrou propriedades analgésicas e antiinflamatórias. Em articulações artrósicas, induz a normalização da fluidez ou viscoelasticidade do líquido sinovial e a ativação da regeneração tecidual na cartilagem comprometida, restabelecendo o equilíbrio funcional da articulação.
Toxicidade
A DL50 de Hialuronato De Sódio em ratos e camundongos foi superior a 100 mg/kg. Os resultados das provas de toxicidade (crônica e sub-aguda) na fertilidade, toxicidade fetal, peri e pós-natal, mutagênese, imunogenicidade e estudos sobre tolerância intra-articular, demonstraram que o produto é bem tolerado.
Farmacocinética
O ácido hialurônico é eficientemente metabolizado no organismo animal, sendo rapidamente removido da corrente sanguínea e degradado no fígado. Estas propriedades estão de acordo com a natureza do composto. Após a administração de ácido hialurônico marcado em cobaias, níveis máximos sanguíneos de radioatividade foram observados depois de 48 horas. A excreção foi principalmente urinária e cerca de 42% estavam presentes no fígado, 24 horas após a aplicação. No líquido sinovial, a radioatividade foi detectada em 2 horas e, na cartilagem articular, dentro de 6 horas.
Cuidados de Armazenamento
Conservar entre 1 e 30°C. Se não for possível garantir esta temperatura, deve-se conservar em geladeira. Proteger da luz.
Não utilizar o produto após o prazo de validade impresso na embalagem. O prazo de validade é de 3 anos a partir da data de fabricação.
Manter fora do alcance e da vista das crianças.
Não utilizar o produto se estiver danificado.
A graduação na etiqueta da seringa dever ser usada apenas como orientação.
Dizeres Legais
Registro ANVISA nº: 80146290006.
Responsável Técnico:
Marcia da Costa Pereira
CRF/SP 32700.
Importador no Brasil:
Zodiac Produtos Farmacêuticos S/A
Rodovia Vereador Abel Fabrício Dias, Nº 3400 Água Preta
CEP: 12403610 - Pindamonhangaba/SP
Autorização: 8.01.462-9 (XH238L40M7WW)
CNPJ 55.980.684/0001-27.
Fabricante por:
Tedec-Meiji Farma, S.A
Ctra. M-300, Km. 30,500
Alcalá de Henares, 28802
Madri, Espanha.
Venda sob prescrição médica.