Comparamos o preço de Restiva 10Mg Com 2 Sachês, veja o menor preço

R$ 188,80
RReferência
1
ofertasMelhores preços a partir de R$ 188,80 até R$ 188,80
Menor preço
vendido por Promofarma
R$ 188,80
Para que serve
Restiva é indicado para o tratamento de dor moderada à forte intensidade (quando é necessário terapia contínua com opioide para obter um controle adequado da dor).
Como Restiva funciona?
Os adesivos Restiva contêm como princípio ativo a buprenorfina que pertence a um grupo de medicamentos chamados analgésicos opioides.
A buprenorfina é continuamente absorvida através da pele em contato com o adesivo transdérmico, atinge a corrente sanguínea e bloqueia as mensagens de dor que são enviadas para o cérebro.
O efeito analgésico total da dose inicial ocorre em 72 horas (3 dias), momento a partir do qual o médico poderá alterar a dose.
Contraindicação
Restiva é contraindicado a:
- Pacientes com hipersensibilidade (alergia) à buprenorfina ou a qualquer componente da fórmula;
- Pacientes com função respiratória gravemente comprometida ou a pacientes que estejam utilizando antidepressivos inibidores da monoaminoxidase (IMAOs), devendo esperar no mínimo 14 dias para iniciar tratamento com buprenorfina.
Restiva não deve ser utilizado em pacientes com miastenia gravis (uma doença crônica autoimune, caracterizada por déficit motor e fadiga muscular) e delirium tremens (síndrome de abstinência, caracterizada por alucinações e tremedeira).
Como usar
Analgésicos opióides, como Restiva, foram usados para tratar a dor por muitos anos. Na maioria dos casos, não ocorre vício. Entretanto, com o passar do tempo, seu corpo pode se acostumar com o uso de Restiva de modo que, se você parar repentinamente de usá-lo, pode apresentar alguns sintomas de abstinência.
É importante discutir essa questão com seu médico.
Restiva está disponível em três potências diferentes.
Seu médico decidirá que adesivo, ou combinação de adesivos, é adequado para controlar sua dor.
Cada adesivo é aplicado na pele e dura por sete dias.
Após sete dias, retire o adesivo e aplique um novo adesivo na pele em um lugar diferente.
Utilizando pela primeira vez
A dose de partida usual de Restiva é de 5 microgramas/h, aplicada uma vez a cada 7 dias.
Adesivos de 10 e 20 microgramas/h estão disponível para dores mais fortes.
Seu médico pode prescrever uma combinação de adesivos, se necessário, para controlar sua dor.
O primeiro adesivo pode levar até três dias para alcançar o efeito máximo. Isso porque buprenorfina é absorvida lentamente através da pele e através do sangue.
Seu médico pode prescrever medicamentos adicionais para controlar a dor durante esse tempo.
Aplicando o adesivo
- Encontre uma região de pele limpa e intacta na parte externa superior do braço, na região superior do tórax, superior das costas ou do lado do tórax. Não aplique o adesivo na pele quando estiver vermelha, queimada ou lesionada. O local da aplicação deve ser alternado se o adesivo for reaplicado ou quando for ser aplicado um segundo adesivo. O local de aplicação pode ser repetido após intervalo de pelo menos 3 semanas.
- Certifique-se de que o local esteja quase sem pelos e sem cicatrizes grandes. Se a região apresentar pelos, corte-os com tesoura, mas não depile ou raspe a área escolhida, já que isso pode lesionar a pele.
- A área escolhida deve estar limpa. Se necessário, lave a área somente com água limpa, não use sabão, álcool, óleos, loções ou dispositivos abrasivos. A área escolhida para aplicar o adesivo deve estar seca, portanto, seque a área completamente após a lavagem com água.
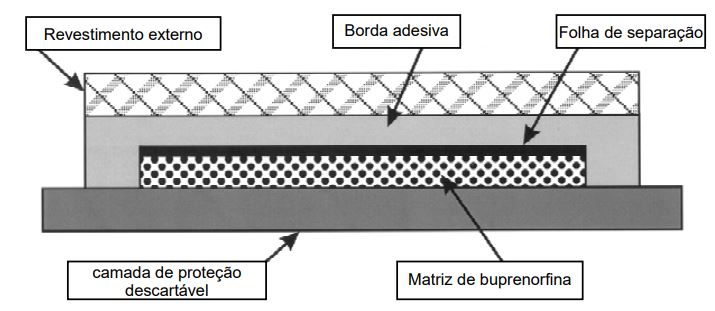
- Retire o adesivo do sachê. Restiva deve ser aplicado imediatamente após a abertura do sachê.
- Para aplicar o adesivo, retire a camada de proteção e pressione firmemente o adesivo com a palma da mão no local escolhido por aproximadamente 30 segundos.
- Certifique-se que todo o adesivo está em contato com a pele especialmente ao redor das bordas. Se as bordas do adesivo começarem a se soltar, elas podem ser grudadas com uma fita adesiva adequada para pele.
- Lave suas mãos com água limpa.
O adesivo deve ser usado continuamente por 7 dias, não é afetado por banho, ducha e natação. Entretanto, é recomendado mantê-lo seco sempre que possível. Se um adesivo cair, um novo deve ser aplicado, seguindo as recomendações acima.
Durante o tratamento com Restiva, deve-se evitar exposição do local de aplicação a fontes de calor externas, tais como almofadas de aquecimento, cobertores elétricos, lâmpadas de aquecimento, etc, já que pode ocorrer aumento na absorção da buprenorfina, o que pode levar a um aumento na incidência de eventos adversos relacionados aos opioides.
Os efeitos de uso de Restiva em banheiras quentes e sauna não foram estudados.
Durante o tratamento com Restiva, também se deve evitar o uso de protetores solares, soluções, cremes e outros produtos na área em que o adesivo será aplicado.
Trocando o adesivo
Troque seu adesivo no mesmo horário do mesmo dia de cada semana. Por exemplo, se você começar a usar seu adesivo às 9h00 da manhã de segunda-feira, troque seu adesivo na próxima segunda-feira às 9h00.
- Após sete dias, retire o adesivo.
- Dobre o adesivo pela metade de modo que o lado adesivo fique para dentro.
- Jogue o adesivo em um lugar seguro, no qual as crianças não tem acesso.
- Aplique um novo adesivo em uma área diferente da pele, seguindo as etapas “Aplicando o adesivo”.
- O local da aplicação deve ser alternado se um adesivo for reaplicado ou adicionado. O local de aplicação pode ser repetido após intervalo de pelo menos 3 semanas.
Posologia
A menor dose de Restiva, 5 mg, deve ser usada como a dose inicial em todos os pacientes.
No tratamento da dor é fundamental a avaliação do paciente. Além disso, a terapia deverá ser revisada regularmente, sendo ajustada baseando-se nas informações do próprio paciente referentes à dor e reações adversas, bem como na avaliação clínica do médico.
Como ocorre com todos os opioides, a concentração plasmática efetiva mínima para analgesia varia entre os pacientes, especialmente em pacientes tratados anteriormente com opioides agonistas potentes.
Consequentemente, os pacientes devem ser tratados com variação individualizada da dose para se obter o efeito desejado.
A dose efetiva mínima de buprenorfina poderá aumentar em função do uso de doses repetidas, em qualquer paciente, devido ao aumento da dor e/ou desenvolvimento de tolerância farmacológica.
Idosos
Não é necessário ajuste de dosagem no idoso.
Crianças
Não foi estabelecida a segurança e eficácia de Restiva em pacientes com menos de 18 anos de idade.
Insuficiência renal
Não é necessário ajuste de dose em pacientes com insuficiência renal.
Insuficiência hepática
Em pacientes com insuficiência hepática leve a moderada, não é necessário ajuste de dose de Restiva.
Pacientes com insuficiência hepática grave podem acumular buprenorfina durante o tratamento. Deve-se considerar terapia alternativa e Restiva deve ser usado com cautela neste caso.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
Descontinuação
Após a remoção de um adesivo de Restiva, as concentrações da substância no sangue diminuem gradativamente. Isto deve ser considerado quando a terapia com Restiva for seguida por tratamento com outros opioides.
Como uma regra geral, um opioide subsequente não deve ser administrado dentro de 24 horas após a remoção de um adesivo Restiva.
Este medicamento não deve ser cortado.
O que devo fazer quando eu me esquecer de usar Restiva?
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
- Trocar o adesivo (aplicar um novo) e seguir os intervalos conforme descrito acima, baseando-se no dia e horário que aplicou o novo adesivo.
- Não aplique dois adesivos ao mesmo tempo para compensar dose omitida. Isto aumentará a chance de ter reações adversas indesejáveis.
Precauções
Febre
Doença febril grave pode aumentar a taxa de absorção de buprenorfina.
Lesões cranianas
Restiva deve ser usado com particular precaução em pacientes com lesão cerebral, lesões intracranianas ou aumento na pressão intracraniana, ou nível reduzido de consciência de origem indeterminada.
Convulsões
A buprenorfina pode diminuir o limiar para convulsão em pacientes com histórico de distúrbios convulsivos.
Depressão respiratória
Deve-se ter especial cautela quando Restiva for prescrito para pacientes que sabidamente têm, ou suspeita-se que tenham, problemas com abuso de drogas ou álcool ou doença mental séria, uma vez que há relatos de ocorrência de depressão respiratória devido ao uso concomitante de buprenorfina via intravenosa com álcool e benzodiazepínicos.
Intervalo QT
Deve-se ter cautela ao prescrever Restiva para pacientes com prolongamento congênito de intervalo QT e para pacientes tomando medicações antiarrítmicas de Classe 1A (por exemplo, quinidina, procainamida) ou de Classe III (por exemplo, amiodarona, sotalol) ou qualquer outra medicação que prolongue o intervalo QT.
Dependência de drogas
A buprenorfina produz efeitos semelhantes aos da morfina, incluindo euforia e dependência física, porém a magnitude destes efeitos é menor quando comparado aos efeitos observados com doses semelhantes de agonistas puros.
A administração de buprenorfina a pessoas que são fisicamente dependentes de opioides enquadrados como agonistas puros pode levar à síndrome de abstinência, dependendo do nível de dependência física, do tempo e da dose de buprenorfina.
O uso crônico de buprenorfina pode resultar no desenvolvimento de dependência física. A síndrome de abstinência (síndrome de retirada), quando ocorre, geralmente é leve, começa após 2 dias e pode durar até 2 semanas.
Os sintomas da síndrome de abstinência incluem agitação, ansiedade, nervosismo, insônia, hipercinesia (excesso de movimentação de um órgão ou região do corpo), tremor e distúrbios gastrointestinais.
Atenção: pode causar dependência física ou psíquica.
Carcinogenicidade, mutagenicidade e comprometimento da fertilidade
Testes indicam que a buprenorfina não é genotóxica, ou seja, não causa danos ao material genético do organismo.
Em estudos realizados em ratos e camundongos não houve evidência de qualquer potencial carcinogênico relevante para os seres humanos.
Estudos para avaliar toxicidade reprodutiva da buprenorfina em ratos não demonstraram comprometimento na fertilidade.
Testes laboratoriais
Foram observados níveis aumentados de aminotransferase (enzimas do fígado) e diminuição de peso com a utilização de buprenorfina.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Este medicamento pode causar “doping”.
Reações Adversas
Em geral, as reações adversas incluídas neste item são aquelas com uma relação plausível com o uso do medicamento.
As frequências das reações adversas são dadas como se segue:
- Muito comum - ocorre em mais de 10% dos pacientes que utilizam este medicamento;
- Comum - ocorre entre 1% e 10% dos pacientes que utilizam este medicamento;
- Incomum - ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento;
- Rara - ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento;
- Muito rara - ocorre em menos de 0,01% dos pacientes que utilizam este medicamento.
Distúrbios do sistema imunológico
Incomum
- Reações alérgicas (incluindo inchaço da garganta e da língua).
Rara
- Respostas anafiláticas (reação alérgica grave e imediata que pode levar à morte).
Distúrbios metabólico e nutricional
Comum
- Anorexia (redução ou perda do apetite).
Rara
-
Desidratação.
Distúrbios psiquiátricos
Comum
- Confusão;
- Depressão;
- Insônia;
- Nervosismo;
- Ansiedade.
Incomum
- Labilidade de afeto;
- Agitação;
- Humor eufórico;
- Alucinação;
- Diminuição da libido;
- Pesadelos;
- Agressão.
Rara
- Distúrbio psicótico.
Não conhecida
- Despersonalização (experiências de sentimentos de irrealidade, de ruptura com a personalidade).
Distúrbios do sistema nervoso
Muito comum
- Tontura;
- Dor de cabeça;
- Sonolência.
Comum
- Tremor.
Incomum
- Comprometimento da concentração;
- Coordenação anormal;
- Disartria (dificuldade de articular as palavras);
- Disgeusia (alteração ou diminuição do paladar);
- Hipoestesia (perda ou diminuição de sensibilidade em determinada parte do organismo);
- Comprometimento da memória;
- Enxaqueca;
- Síncope (desmaio);
- Parestesia (sensação anormal como ardor, formigamento e coceira na pele).
Não conhecida
- Convulsões.
Distúrbios oculares
Incomum
- Olho seco;
- Visão embaçada.
Rara
- Miose (diminuição do diâmetro da pupila).
Distúrbios do ouvido e labirinto
Incomum
- Tinido (zumbido no ouvido);
- Vertigem (tontura).
Distúrbios cardíacos
Incomum
- Palpitações;
- Taquicardia (aceleração do ritmo cardíaco).
Rara
- Angina de peito (dor no peito, relacionada à doença das artérias coronárias.
Distúrbios vasculares
Incomum
- Vermelhidão;
- Hipertensão (pressão alta);
- Hipotensão (pressão baixa).
Rara
- Vasodilatação;
- Hipotensão ortostática (queda súbita de pressão arterial na posição ereta).
Distúrbios respiratório, torácico e mediastinal
Comum
- Dispneia (dificuldade respiratória, falta de ar).
Incomum
- Tosse;
- Soluços;
- Chiado no peito.
Rara
- Insuficiência respiratória
- Depressão respiratória;
- Asma agravada;
- Hiperventilação;
- Rinite.
Distúrbios gastrintestinais
Muito comum
- Constipação;
- Náusea;
- Vômito.
Comum
- Dor abdominal;
- Diarreia;
- Dispepsia (má digestão);
- Boca seca.
Incomum
- Flatulência.
Rara
- Disfagia (dificuldade de engolir);
- Íleo paralítico (obstrução funcional dos intestinos).
Não conhecida
- Viverticulite (inflamação no intestino grosso).
Distúrbios hepatobiliares
Não conhecida
- Cólica biliar.
Distúrbios da pele e tecido subcutâneo
Muito comum
- Prurido (coceira e/ou ardência).
Comum
- Eritema (vermelhidão);
- Sudorese.
Incomum
- Pele seca;
- Urticária;
- Dermatite de contato (inflamação na pele)**.
Rara
- Edema (inchaço) facial.
Distúrbios musculoesqueléticos e do tecido conjuntivo
Incomum
- Espasmos musculares;
- Mialgia (dor muscular).
Distúrbios renal e urinário
Incomum
- Incontinência urinária (perda de urina);
- Retenção urinária (dificuldade para urinar);
- Hesitação urinária (dificuldade de iniciar a micção).
Distúrbios do sistema reprodutivo e mamário
Rara
- Disfunção sexual.
Distúrbios gerais e condições no local da administração
Muito comum
- Reação no local da aplicação*.
Comum
- Condições de astenia (incluindo fraqueza muscular);
- Edema periférico (inchaço nas extremidades do corpo).
Incomum
- Edema (inchaço);
- Pirexia (febre);
- Tremores;
- Síndrome de retirada;
- Dermatite no local da aplicação**;
- Dor no peito.
Rara
-
Sintomas tipo gripe.
Não conhecido
-
Síndrome de retirada neonatal (sintomas de abstinência no recém-nascido por uso materno da medicação).
Laboratoriais
Incomum
- Aumento da alanina aminotransferase (uma enzima do fígado);
- Diminuição de peso.
Lesões, envenenamento e complicações do processo
Incomum
- Lesão acidental (incluindo queda).
* Inclui: eritema (vermelhidão) no local da aplicação, edema (inchaço) no local da aplicação, prurido (coceira) no local da aplicação, erupção no local da aplicação.
** Em alguns casos, reações alérgicas locais tardias ocorreram com sinais evidentes de inflamação. Nesses casos, o tratamento com Restiva deve ser interrompido.
Atenção: este produto é um medicamento que possui nova forma farmacêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
População Especial
Uso na gravidez
Restiva deve ser usado durante a gravidez apenas se os benefícios justificarem o potencial risco para o feto.
Demonstrou-se que a buprenorfina atravessa a placenta em humanos, sendo detectada no sangue, urina e mecônio de recém-nascidos e também no leite materno em baixas concentrações.
A administração de analgésicos opioides às mães, incluindo buprenorfina, podem causar depressão respiratória no bebê recém-nascido.
O uso prolongado de buprenorfina durante a gravidez pode resultar em síndrome de retirada nos bebês recém-nascidos.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Uso durante a lactação
Uma vez que a buprenorfina passa para o leite da mãe, Restiva não deve ser usado por mulheres que estejam amamentando.
Trabalho de parto
Restiva não é recomendado para uso em mulheres imediatamente antes ou durante o trabalho de parto e parto, uma vez que opioides, em geral, podem causar depressão respiratória em recém-nascidos.
Efeitos na habilidade de dirigir veículos e operar máquinas
A buprenorfina pode prejudicar a habilidade de dirigir veículos e operar máquinas.
Durante o tratamento, e 24 horas após a retirada do adesivo, o paciente não deve dirigir veículos ou operar máquinas, pois sua habilidade e atenção podem estar prejudicadas.
Outras condições
Restiva deve ser usado com precaução em pacientes com hipotensão (pressão arterial baixa), hipovolemia e choque (volume sanguíneo reduzido), doença do trato biliar, pancreatite, distúrbios inflamatórios intestinais, hipertrofia prostática, insuficiência adrenocortical.
Restiva deve ser usado com precaução em pacientes com comprometimento hepático grave.
Restiva deve ser usado com precaução após cirurgia abdominal, já que os opioides são conhecidos por comprometer a motilidade intestinal.
Assim como recomendado para todos os opioides, uma redução na dosagem pode ser aconselhável para pacientes com hipotireoidismo.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Composição
Restiva 5mg
Cada adesivo transdérmico contém:
5 mg de buprenorfina (libera 5 microgramas/h).
Excipientes: ácido levulínico, oleiloleato, povidona, Duro-Tak 387-2051(poliacrilato sem ligação cruzada), Duro-Tak 387- 2054 (poliacrilato com ligação cruzada), tereftalato de polietileno.
A área contendo a substância ativa é de 6,25 cm2.
Restiva 10mg
Cada adesivo transdérmico contém:
10 mg de buprenorfina (libera 10 microgramas/h).
Excipientes: ácido levulínico, oleiloleato, povidona, Duro-Tak 387-2051(poliacrilato sem ligação cruzada), Duro-Tak 387- 2054 (poliacrilato com ligação cruzada), tereftalato de polietileno.
A área contendo a substância ativa é de 12,5 cm2.
Restiva 20mg
Cada adesivo transdérmico contém:
20 mg de buprenorfina (libera 20 microgramas/h).
Excipientes: ácido levulínico, oleiloleato, povidona, Duro-Tak 387-2051(poliacrilato sem ligação cruzada), Duro-Tak 387- 2054 (poliacrilato com ligação cruzada), tereftalato de polietileno.
A área contendo a substância ativa é de 25 cm2.
Superdosagem
Os sintomas de uma superdosagem incluem depressão respiratória, apneia (parada respiratória), sedação, sonolência, náusea, vômito, colapso cardiovascular (insuficiência cardiovascular) e miose (diminuição das pupilas) marcante.
No caso de superdosagem, retire qualquer adesivo em contato com o paciente e descarte adequadamente e procure socorro médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
IMAOs não-seletivos intensificam os efeitos de medicamentos opióides, o que pode causar ansiedade, confusão e depressão respiratória. Este medicamento não deve ser usado concomitantemente com IMAOs não-seletivos ou em pacientes que receberam IMAOs não-seletivos nos últimos 14 dias. Como não se sabe se existe uma interação entre IMAOs seletivos (por exemplo, selegilina) e buprenorfina, aconselha-se tomar cuidado com essa combinação medicamentosa.
Este medicamento, assim como todos os analgésicos opióides, deve ser administrado com precaução em pacientes que estão atualmente tomando outros depressores de SNC ou outros medicamentos que podem causar depressão respiratória, hipotensão, sedação profunda ou potencialmente resultam em coma. Tais agentes incluem sedativos ou hipnóticos, anestésicos gerais, outros analgésicos opióides, fenotiazinas, antieméticos de ação central, benzodiazepinas e álcool.
Reduções no fluxo de sangue hepático induzidas por alguns anestésicos gerais (por exemplo, halotano) e outros medicamentos podem levar a uma queda na taxa de eliminação hepática.
Buprenorfina é metabolizada a norbuprenorfina por CYP450 3A4. Aconselha-se cuidado quando este medicamento é administrado concomitantemente com inibidores de CYP3A4 (por exemplo, inibidores de protease, algumas classes de medicamento de antimicóticos azóis, antagonistas de canal de cálcio e antibióticos macrólidos) já que isso pode levar a níveis aumentados de buprenorfina. A co-administração deste medicamento e indutores de enzima (por exemplo, fenobarbitona, carbamazepina, fenitoína, rifampicina) poderia levar à depuração aumentada resultante em eficácia reduzida.
Em pacientes de ensaios clínicos, não houve nenhum efeito aparente sobre a exposição deste medicamento quando usado concomitantemente com vários antagonistas H2 ou inibidores de bomba de próton. Existe o potencial para elevação de INR em pacientes que estiverem concomitantemente tomando varfarina.
Ação da Substância
Resultados de eficácia
A eficácia de Buprenorfina (substância ativa) foi comparada com placebo em um estudo duplo-cego randomizado com grupo paralelo em pacientes com osteoartrite do joelho ou quadril (n=315) cuja dor não era controlada apenas com não opioides (400 mg de ibuprofeno 4 vezes ao dia). As chances de tratamento bem sucedido foram 1,66 vezes maiores nos pacientes tratados com o Buprenorfina (substância ativa) do que nos pacientes que receberam placebo.
Em outro estudo multicêntrico, randomizado, duplo-cego, controlado com placebo e com controle ativo e grupo paralelo de longo prazo (84 dias) foi conduzido em 134 pacientes com dor lombar crônica não controlada com não-opioides. Os pacientes foram mantidos em suas doses de AINE pré-estudo e randomizados para receber um dos seguintes: adesivo transdérmico Buprenorfina (substância ativa) a cada 7 dias, comprimidos de oxicodona 5 mg/paracetamol 325 mg a cada 6 horas ou placebo equivalente.
O controle da dor obtido com Buprenorfina (substância ativa) em pacientes com dor lombar crônica foi superior estatisticamente ao placebo e não inferior aos comprimidos de oxicodona/paracetamol. Um estudo multicêntrico, duplo-cego com grupo paralelo comparou a eficácia e o perfil de segurança de Buprenorfina (substância ativa) e do placebo em pacientes com dor persistente (?2 meses) não relacionada ao câncer que precisaram de analgésicos opioides. Os resultados mostraram que as chances de tratamento ineficaz foram 1,79 (95% IC, 1,09–2,95) vezes maior para placebo em relação ao adesivo transdérmico Buprenorfina (substância ativa) (p=0,022). Demonstrando que em pacientes com dor crônica não relacionada ao câncer que precisavam de terapia com opioides, o uso do adesivo transdérmico Buprenorfina (substância ativa) proporcionou analgesia eficaz.
A eficácia e a tolerabilidade de longo prazo do Buprenorfina (substância ativa) foram investigadas em um estudo aberto de acompanhamento de pacientes de dor crônica. Dos 385 pacientes inscritos, 98% foram recrutados de estudos anteriores do Buprenorfina (substância ativa) e a maioria tinha dor devido a doenças articulares ou ósseas degenerativas. Os pacientes no estudo receberam o Buprenorfina (substância ativa) por entre 1 e 609 dias; a exposição média foi de 234 dias. A maioria dos pacientes começou com o adesivo de 5 mg e as doses foram tituladas até o controle eficaz da dor com o adesivo de 10 ou 20 mg. No 3º mês, 14% dos pacientes estavam com Buprenorfina (substância ativa) inicial de 5 mg, 35% com o adesivo de 10 mg e 48% com o adesivo de 20 mg. A maioria das doses permaneceu inalterada após mais 3 meses. Os escores médios de dor permaneceram constantes durante todo o estudo, indicando que o Buprenorfina (substância ativa) proporcionou controle consistente por longo prazo da dor dos pacientes. Também há evidências de alguma melhora na funcionalidade, qualidade de vida e resultados de saúde. No longo prazo, o adesivo transdérmico Buprenorfina (substância ativa) proporcionou controle consistente da dor em pacientes com dor crônica devido a doenças articulares ou ósseas degenerativas.
Características farmacológicas
Propriedades farmacodinâmicas
A buprenorfina é um agonista opioide parcial, que age no receptor opioide mµ. Ela também possui atividade antagonista no receptor opioide kappa. É classificada como uma substância psicotrópica por convenção internacional.
Sistema endócrino
Os opioides podem influenciar os eixos hipotalâmico-pituitário-adrenal ou –gonadal. Algumas alterações que podem ser observadas durante o uso de opioides são aumento na prolactina sérica e diminuição no cortisol e na testosterona plasmáticos. Sintomas clínicos podem se manifestar devido a essas alterações hormonais.
Outros efeitos farmacológicos
Estudos in vitro e em animais indicam vários efeitos dos opioides naturais, como por exemplo a morfina, nos componentes do sistema imune; a significância clínica desses efeitos é desconhecida. Não se sabe se a buprenorfina, um opioide semissintético, tem efeitos imunológicos semelhantes aos da morfina. Assim como outros analgésicos opioides, a buprenorfina apresenta um risco potencial de depressão respiratória. No entanto, as evidências sugerem que a buprenorfina é um agonista parcial no que diz respeito à sua atividade depressora respiratória, sendo observado um efeito teto após a administração de doses intravenosas maiores que 2 ?g/kg. A depressão respiratória parece ser um evento raro em doses terapêuticas da apresentação transdérmica (até 40 ?g/h). Em alguns pacientes, a buprenorfina pode causar retenção urinária e miose relacionadas com a dose. Em comparação com outros analgésicos, a buprenorfina tem uma longa duração de ação. Isso está relacionado à alta afinidade que possui pelos receptores opioides e sua lenta dissociação deles.
Propriedades farmacocinéticas
Cada adesivo transdérmico de Buprenorfina (substância ativa) fornece uma quantidade constante de buprenorfina por até 7 dias. O estado de equilíbrio (steady state) é atingido em 72 horas (3 dias), momento a partir do qual se pode iniciar a titulação da dose, conforme a necessidade de cada paciente.
Após a remoção de Buprenorfina (substância ativa), as concentrações de buprenorfina declinam, diminuindo aproximadamente 50% em 12 horas (variação 10-24 h).
A taxa de liberação de buprenorfina de cada adesivo é proporcional à área superficial. Cada adesivo transdérmico de Buprenorfina (substância ativa) 5 mg libera 5 microgramas de buprenorfina por hora. Cada adesivo transdérmico de Buprenorfina (substância ativa) 10 mg libera 10 microgramas de buprenorfina por hora. Cada adesivo transdérmico de Buprenorfina (substância ativa) 20 mg libera 20 microgramas de buprenorfina por hora.
Absorção:
Após a aplicação de Buprenorfina (substância ativa), a buprenorfina se difunde do adesivo para a corrente sanguínea através da pele.
A absorção não varia significativamente entre os locais de aplicação especificados. A exposição média (ASC) em cada local de aplicação está dentro de aproximadamente ± 11% da exposição média para os quatro locais. Em estudos de farmacologia clínica, o tempo mediano para que Buprenorfina (substância ativa) 10 mg depositasse concentrações detectáveis de buprenorfina (25 picogramas/mL) foi de aproximadamente 17 horas. A biodisponibilidade de buprenorfina de um adesivo de Buprenorfina (substância ativa) em relação à buprenorfina IV é de 15% (para todas as três concentrações).
Distribuição:
Aproximadamente 96% da buprenorfina se liga a proteínas plasmáticas.
Em um estudo no qual foi administrada buprenorfina IV a indivíduos saudáveis, o volume de distribuição no estado de equilíbrio (steady state) foi de 430 L, refletindo o grande volume de distribuição e alta lipofilicidade da substância. As concentrações de buprenorfina no líquor parecem ser de aproximadamente 15% a 25% das concentrações plasmáticas.
Metabolismo e Eliminação:
O metabolismo de buprenorfina na pele após a aplicação do adesivo de Buprenorfina (substância ativa) é desprezível.
A buprenorfina absorvida pelo organismo sofre metabolismo hepático, e subsequente excreção biliar e renal dos metabólitos solúveis. O metabolismo hepático através das enzimas CYP3A4 e UGT1A1/1A3 resulta em 2 metabólitos primários, norbuprenorfina e buprenorfina 3-O-glicuronídeo, respectivamente. A norbuprenorfina é o único metabólito ativo conhecido da buprenorfina. Esta é glicuronizada antes de sua eliminação.
A buprenorfina livre é eliminada nas fezes em 7 dias.
Em um estudo em pacientes pós-operatórios, a depuração total de buprenorfina foi de 55 L/h.
Local de Aplicação:
Um estudo realizado em indivíduos saudáveis demonstrou que o perfil farmacocinético de buprenorfina depositada por Buprenorfina (substância ativa) é semelhante quando aplicado na parte externa superior do braço, no tórax superior, nas costas ou no lado do tórax (linha axilar média, 5o espaço intercostal).
Dados de Segurança Pré-clínicos
Toxicidade sistêmica e dérmica: Em estudos de toxicidade de dose única e de doses repetidas em ratos, coelhos, porquinhos da índia, cães e mini porcos, Buprenorfina (substância ativa) causou nenhuma ou poucas reações adversas sistêmicas, enquanto irritação da pele foi observada em todas as espécies analisadas.
Dados toxicológicos disponíveis não indicam um potencial de sensibilização dos aditivos dos sistemas transdérmicos.
Genotoxicidade e carcinogenicidade:
Uma bateria padrão de testes de genotoxicidade indicou que a buprenorfina não é genotóxica. Em estudos a longo prazo em ratos e camundongos, não houve evidência de qualquer potencial carcinogênico relevante para seres humanos.
Toxicidade reprodutiva e no desenvolvimento: Não foram observados efeitos na fertilidade ou na capacidade reprodutiva em ratos tratados com buprenorfina. Não foram observados efeitos tóxicos embriofetais em ratos ou coelhos. Em um estudo de toxicidade no desenvolvimento pré e pós natal realizado com buprenorfina, houve morte da prole e redução do peso dos filhotes quando foram administradas doses maternas que produziam redução no consumo de alimentos e sintomas clínicos.
Cuidados de Armazenamento
Restiva deve ser conservado em temperatura ambiente (15o a 30oC), protegido da luz e da umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Todo medicamento deve ser mantido fora do alcance das crianças.
Características organolépticas
Os adesivos Restiva são retangulares ou quadrados com cantos arredondados e de coloração bege.
Cada adesivo de Restiva é impresso com o nome comercial e a potência em tinta azul.
Cada potência tem um tamanho diferente.
Quanto maior a potência, maior o tamanho do adesivo.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Dizeres Legais
MS - 1.9198.0002
Farm. Resp:
Kátia Esteves dos Santos
CRF-SP nº 36.165.
Fabricado por:
LTS – Lohmann Therapie Systeme A.G.
Andernach - Alemanha.
Importado por:
Mundipharma brasil prod. médicos e farmacêuticos LTDA.
Rua Verbo Divino, 2001 – 16º andar – Sala A
Chácara Santo Antônio
São Paulo - SP
CNPJ: 15.127.898/0001-30.
Venda sob prescrição médica.
Atenção: pode causar dependência fisica ou psiquica.