Comparamos o preço de Androcur - 50Mg 20 Comprimidos, veja o menor preço

R$ 191,98
RReferência
1
ofertasMelhores preços a partir de R$ 191,98 até R$ 191,98
Menor preço
vendido por Pague Menos
R$ 191,98
Para que serve
Androcur contém acetato de ciproterona que apresenta propriedades antiandrogênicas, ou seja, atua no tratamento de doenças associadas aos hormônios sexuais masculinos, os quais também estão presentes no organismo feminino em pequena quantidade. Converse com o seu médico para obter maiores esclarecimentos sobre a ação do produto e sua utilização.
Como o Androcur funciona?
Androcur é uma preparação hormonal que bloqueia o efeito dos andrógenos que são hormônios sexuais produzido principalmente em homens, mas também, em menor quantidade, em mulheres.
Em pacientes do sexo feminino, Androcur influencia favoravelmente condições andrógeno-dependentes como problemas de crescimento excessivo de pelo no hirsutismo, perda de cabelo no couro cabeludo (alopecia androgênica) e aumento da atividade da glândula sebácea em acne e seborreia.
Em pacientes do sexo masculino, Androcur reduz a concentração de testosterona (andrógenos) no sangue, o que resulta na redução do impulso em desvios sexuais.
Sabe-se também que andrógenos estimulam o crescimento do câncer de próstata, e nestes pacientes, Androcur inibe este efeito.
Contraindicação
Não tome Androcur se você apresenta qualquer uma das condições apresentadas abaixo. Se alguma destas condições se aplica a você, fale com seu médico antes de iniciar o tratamento com Androcur.
Contraindicações em mulheres
- Se você está grávida ou amamentando;
- Se você tem doença no fígado;
- Se você tem antecedente de icterícia ou prurido (coceira) persistente durante gravidez anterior;
- Se você tem antecedente de herpes durante a gravidez;
- Se você sofre de uma doença do fígado onde há excreção alterada de bilirrubina (pigmento resultante das células vermelhas do sangue) (Síndromes de Dubin-Johnson e de Rotor);
- Se você tem ou já teve tumores benignos ou malignos de fígado;
- Se você tem ou teve tumor benigno no cérebro (meningioma);
- Se você tem doenças debilitantes (que cause desânimo ou fraqueza);
- Se você sofre de depressão crônica grave;
- Se você tem ou já teve distúrbios que afetem a circulação sanguínea: em particular, aqueles problemas relacionados à trombose (formação de coágulo de sangue) nos vasos sanguíneos (processos tromboembólicos);
- Se você tem diabetes mellitus grave com alterações nos vasos sanguíneos;
- Se você tem anemia falciforme;
- Se você é alérgico (hipersensibilidade) ao acetato de ciproterona ou qualquer outro componente da formulação.
Se seu médico prescreveu a terapia cíclica combinada, você deve prestar cuidadosa atenção também às informações contidas na bula do produto escolhido, que será usado em associação ao Androcur.
Contraindicações em homens
- Quando prescrito para redução do impulso em casos de desvios sexuais em homens
- Se você tem alguma doença no fígado;
- Se você sofre de uma doença do fígado onde há excreção alterada de bilirrubina (pigmento resultante das células vermelhas do sangue) (Síndromes de Dubin-Johnson e de Rotor);
- Se você tem ou teve tumores benignos ou malignos de fígado;
- Se você tem ou teve tumor benigno no cérebro (meningioma);
- Se você tem doenças debilitantes (que cause desânimo ou fraqueza);
- Se você sofre de depressão crônica grave;
- Se você tem ou teve distúrbios que afetem a circulação sanguínea: em particular, aqueles problemas relacionados à trombose (formação de coágulo de sangue) nos vasos sanguíneos (processos tromboembólicos);
- Se você tem diabetes mellitus grave com alterações nos vasos sanguíneos;
- Se você tem anemia falciforme;
- Se você é alérgico (hipersensibilidade) ao acetato de ciproterona ou qualquer outro componente da formulação;
- Quando prescrito para tratamento antiandrogênico em câncer de próstata inoperável;
- Se você tem alguma doença no fígado;
- Se você sofre de uma doença do fígado onde há excreção alterada de bilirrubina (pigmento resultante das células vermelhas do sangue) (Síndromes de Dubin-Johnson e de Rotor);
- Se você tem ou teve tumores benignos ou malignos de fígado (apenas se estes não forem devidos a metástases do carcinoma de próstata);
- Se você tem ou teve tumor benigno no cérebro (meningioma);
- Se você tem doenças debilitantes (que cause desânimo ou fraqueza, com exceção de carcinoma da próstata inoperável);
- Se você sofre de depressão crônica grave;
- Se você tem distúrbios atuais ou anteriores que afetem a circulação sanguínea: em particular, aqueles problemas relacionados à trombose (formação de coágulo de sangue) nos vasos sanguíneos (processos tromboembólicos);
- Se você é alérgico (maior sensibilidade) ao acetato de ciproterona ou qualquer outro componente da formulação.
Como usar
Os comprimidos devem ser ingeridos com pequena quantidade de líquido, após as refeições.
Se você acha que o efeito de Androcur é muito forte ou muito fraco, informe ao seu médico ou farmacêutico.
Uso em homens
Não ingerir mais que a dose máxima diária que é de 300mg.
Redução do impulso em desvios sexuais
As doses individuais serão determinadas pelo médico. O tratamento geralmente é iniciado com 50mg, 2 vezes ao dia. Seu médico pode aumentar a dose para 100mg, 2 vezes ao dia ou mesmo 3 vezes ao dia por curto período de tempo. Uma vez obtida melhora clínica satisfatória, seu médico deverá manter o efeito terapêutico com a menor dose possível. Com bastante frequência, é suficiente a dose de 25mg (½ comprimido de 50mg), 2 vezes ao dia. Ao estabelecer a dose de manutenção ou quando for necessário interromper o tratamento, seu médico não deverá reduzir a dose abruptamente, mas de maneira gradual, reduzindo a dose diária de 50mg de cada vez, ou melhor, de 25mg, com intervalos de várias semanas entre cada redução.
Para estabilizar o efeito terapêutico, é necessário utilizar Androcur por um período de tempo prolongado, se possível com uso simultâneo de medidas psicoterapêuticas.
Tratamento antiandrogênico em carcinoma de próstata inoperável
100mg, 2 a 3 vezes ao dia (total: 200 a 300mg).
O tratamento e a dose prescritos pelo médico, não devem ser alterados ou interrompidos após melhora ou remissões terem ocorrido.
Para reduzir o aumento inicial de hormônios sexuais masculinos em tratamento com agonistas de GnRH (hormônio liberador de gonadotrofina, estimula liberação de hormônio nas gônadas)
Inicialmente, 100mg, 2 vezes ao dia (total: 200mg) isoladamente por 5 a 7 dias seguidos por 100mg, 2 vezes ao dia (total: 200mg), durante 3 a 4 semanas juntamente com o agonista de GnRH na dose recomendada em sua bula.
Para tratar fogachos em pacientes em tratamento com análogos de GnRH ou que foram submetidos à orquiectomia (remoção cirúrgica dos testículos)
50 a 150mg por dia, podendo chegar até 100mg, 3 vezes ao dia, se necessário. (total: 300mg).
Uso em mulheres
Mulheres em idade reprodutiva
Se você está grávida, você não deve usar Androcur. Portanto, a possibilidade de existência de gravidez deve ser excluída antes do início do tratamento.
Em mulheres em idade reprodutiva, o tratamento deve ser iniciado no 1º dia do ciclo (1º dia do ciclo = 1º dia de sangramento). Apenas as pacientes que apresentarem amenorreia (falta de menstruação) podem iniciar o tratamento prescrito imediatamente. Neste caso, o 1º dia de tratamento deve ser considerado como se fosse o 1º dia do ciclo e as recomendações descritas a seguir devem ser observadas.
Terapia cíclica combinada
A dose recomendada é de 100mg diariamente, do 1º ao 10º dia do ciclo (por 10 dias).
Adicionalmente, deve-se usar um medicamento anticoncepcional contendo associação progestógeno-estrogênio, por exemplo, do 1º ao 21º dia do ciclo – uma drágea de Diane 35 diariamente, para promover a necessária proteção contraceptiva e estabilizar o ciclo.
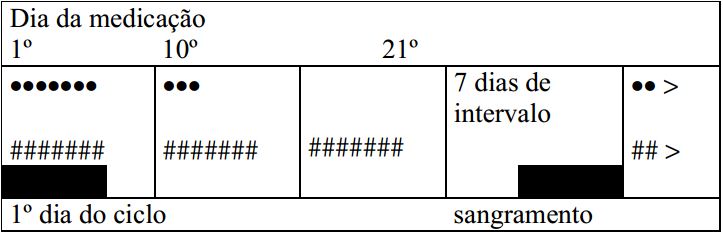 • Androcur
• Androcur
# Diane 35
Se você recebe a terapia cíclica combinada, você deve manter constante um determinado horário do dia para a ingestão do medicamento.
Após 21 dias de tratamento, deve-se intercalar uma pausa de 7 dias, durante a qual deve ocorrer sangramento semelhante à menstruação.
Exatamente quatro semanas após o início de cada curso de tratamento, reinicia-se o mesmo esquema de tratamento combinado, isto é, no mesmo dia da semana e mantendo as mesmas orientações, tenha ou não cessado o sangramento.
Quando seu médico notar melhora clínica, ele pode reduzir a dose diária de Androcur para 50mg ou 25mg (½ comprimido de 50mg), durante os 10 dias iniciais do tratamento combinado com Diane 35. Em alguns casos, o uso isolado de Diane 35 pode ser suficiente.
Ausência de sangramento no intervalo de pausa
Se, excepcionalmente, não ocorrer sangramento durante o intervalo de pausa, o tratamento deve ser provisoriamente interrompido e o médico deve ser consultado para exclusão da possibilidade de gravidez antes de reiniciar o tratamento.
Pacientes pós-menopausadas ou histerectomizadas
Terapia isolada
Androcur pode também ser administrado isoladamente. De acordo com a gravidade do caso, a dose média deve ser de 50mg a 25mg (½ comprimido de 50mg), 1 vez ao dia, seguindo o esquema “21 dias de tratamento, 7 dias de pausa”.
Informações adicionais para populações especiais
Crianças e Adolescentes
Androcur não deve ser administrado antes do término da puberdade, uma vez que durante este período não se pode excluir uma influência desfavorável do medicamento sobre o crescimento longitudinal e o eixo da função endócrina ainda não estabilizado (totalmente amadurecido).
Para pacientes do sexo masculino, Androcur não é recomendado para o uso em crianças e adolescentes abaixo de 18 anos de idade devido a falta de dados de segurança e eficácia.
Para pacientes do sexo feminino, Androcur é somente indicado em meninas que já concluíram a puberdade. Não há dados que sugerem a necessidade de ajuste de dose. Além disso, a segurança e eficácia de Androcur não foram estabelecidas em estudos clínicos com crianças e adolescentes menores de 18 anos de idade.
Pacientes idosos (65 anos ou mais)
Não há dados que sugiram necessidade de ajuste de doses em pacientes idosos.
Pacientes com insuficiência hepática
Não tome Androcur se você sofre de problemas no fígado.
Pacientes com insuficiência renal
Não há dados que sugiram necessidade de ajuste de doses em pacientes com problemas no rim.
Interrupção do tratamento
Não pare de tomar Androcur a menos que seu médico diga para você parar de tomar Androcur. Se você deseja interromper o tratamento, você, primeiramente, deve conversar com seu médico.
Se você tiver qualquer dúvida em como usar este medicamento, pergunte a seu médico
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar o Androcur?
Em pacientes do sexo masculino, caso você se esqueça de tomar um comprimido de Androcur, não tome o comprimido esquecido (não tome duas doses para compensar o comprimido esquecido). Continue tomando os comprimidos de Androcur normalmente.
Em pacientes do sexo feminino, o esquecimento da ingestão do(s) comprimido(s) de Androcur pode diminuir o efeito terapêutico e ocasionar sangramento entre uma menstruação e outra. Os comprimidos esquecidos de Androcur devem ser descartados (não se deve administrar dose dupla de Androcur para repor o comprimido esquecido) e o próximo comprimido de Androcur deve ser ingerido em seu horário habitual, juntamente com a drágea correspondente de Diane 35, quando sob terapia cíclica combinada.
Se você recebe terapia cíclica combinada com Diane 35, você deve manter um determinado horário do dia para a ingestão da drágea [junto com Androcur]. Se houver esquecimento de tomada de uma drágea de Diane 35 você deve tomá-la o quanto antes, se o período de esquecimento for de até 12 horas em relação ao horário que você normalmente toma a drágea de Diane 35. Se o período de esquecimento da drágea for de mais de 12 horas em relação ao horário que você normalmente toma a pílula, a proteção contraceptiva pode ficar reduzida nesse ciclo. Deve-se dar atenção às recomendações para esquecimento de tomada de drágea e segurança contraceptiva contidas na bula de Diane 35. Se não ocorrer sangramento no ciclo em que houve o esquecimento de ingestão da drágea, deve-se investigar a existência de gravidez antes de iniciar a próxima cartela.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Informe ao seu médico se você sofre de diabetes, pois ele poderá necessitar adequar seu medicamento antidiabético. Isto requer supervisão restrita durante o tratamento com Androcur.
Pode ocorrer sensação de falta de ar no tratamento com altas doses de Androcur.
Dados de estudos conduzidos em animais sugerem que altas doses de Androcur podem diminuir a função da glândula produtora de hormônio anexa aos rins (glândula adrenal). Desta forma, seu médico pode realizar alguns testes para monitorar este efeito durante o tratamento com Androcur.
A ocorrência de tumores benignos no cérebro (meningiomas simples ou múltiplos) tem sido relatada em associação ao uso prolongado (anos) de acetato de ciproterona na dose de 25 mg por dia ou mais. Se você for diagnosticado com meningioma, seu médico interromperá o tratamento com Androcur.
Informe seu médico se você alguma vez já teve coágulos de sangue nas artérias ou veias, como trombose venosa profunda, coágulo de sangue nos pulmões (embolia pulmonar), ataque cardíaco (infarto do miocárdio) ou derrame (acidente vascular cerebral).
A ocorrência de coágulos de sangue (eventos tromboembólicos) foi reportada em pacientes sob tratamento com Androcur, embora a relação causal não tenha sido estabelecida. Pacientes que já apresentaram coágulos de sangue ou então tumores avançados têm risco aumentado de coágulos de sangue.
Para ser observado, especificamente, nas pacientes do sexo feminino
Antes de iniciar o tratamento, pacientes do sexo feminino devem ser submetidas a exames clínicos gerais e ginecológicos completos (incluindo mamas e citologia cervical) e a ocorrência de gravidez deve ser excluída.
Se, durante o tratamento combinado com contraceptivo contendo associação progestógeno-estrogênio, como, por exemplo, Diane® 35, ocorrerem gotejamentos (spotting) durante as três semanas em que os comprimidos de contraceptivo estão sendo tomados, não se deve interromper o tratamento. Todavia, se a intensidade do sangramento aumentar, consulte seu médico.
No caso de uso adicional da terapia cíclica combinada com contraceptivo como, por exemplo, Diane 35, deve-se também observar os dados contidos na bula do produto escolhido.
Para ser observado, especificamente, nos pacientes do sexo masculino
Se você está sob tratamento de redução do impulso em casos de desvios sexuais, deve saber que o efeito redutor de impulso produzido por Androcur pode ser diminuído sob a influência do álcool.
Anemia tem sido relatada durante o tratamento de Androcur. Assim, seu médico deverá monitorar a contagem de células vermelhas do sangue durante o tratamento.
Se você possui câncer de próstata inoperável, informe seu médico se você tem antecedentes de qualquer problema listado abaixo, pois ele precisará realizar uma avaliação cuidadosa antes de prescrever Androcur:
- Problemas na circulação do sangue (especialmente formação de coágulo de sangue);
- Anemia falciforme;
- Diabetes grave, com alterações vasculares.
Este medicamento requer uso cuidadoso, sob vigilância médica estrita e acompanhado por controles periódicos da função hepática (bilirrubinas e transaminases) por causar hepatotoxicidade (tóxico para o fígado) aos 8, 15, 30 e 90 dias de tratamento. Este medicamento não é aprovado para uso como anticoncepcional.
Reações Adversas
Como qualquer medicamento, Androcur pode causar reações adversas, embora, nem todos os pacientes apresentam tais reações.
Se alguma reação adversa se tornar séria, ou se você notar qualquer reação adversa não relacionada nesta bula, por favor, informe ao seu médico.
Informe imediatamente ao seu médico se você notar qualquer um dos seguintes sintomas:
- Sensações geralmente desconhecidas, febre, náusea, vômito, perda de apetite, coceira no corpo todo, amarelamento de sua pele e olhos, fezes escurecidas, urina escura. Estes sintomas podem ser sinais de toxicidade do fígado, incluindo inflamação do fígado (hepatite) ou falência do fígado;
- Distúrbios na função do fígado, alguns deles graves (icterícia, hepatite e falência hepática) têm sido observados em pacientes tratados com Androcur. Na dose de 100mg ou mais também têm sido relatados casos fatais. A maioria dos casos fatais foi relatada em homens com câncer de próstata avançado. Os distúrbios da função do fígado são dose-dependentes e normalmente se desenvolvem muitos meses após o início do tratamento. Então, seu médico deverá monitorar sua função hepática antes e durante o tratamento especialmente se há sintomas e sinais que sugerem toxicidade do fígado. Se esta toxicidade do fígado for confirmada, seu médico irá parar o tratamento com Androcur em pacientes do sexo feminino. Já em pacientes do sexo masculino, o tratamento com Androcur será interrompido, a menos que a toxicidade do fígado possa ser explicada por outra causa (por exemplo, tumores secundários). Neste caso, seu médico pode continuar o tratamento com Androcur se os benefícios percebidos superarem o risco;
- Dores não usuais na porção superior do abdômen que não desapareçam espontaneamente em curto período de tempo. Estes sintomas podem ser sinais de tumores benignos ou malignos no fígado que podem levar a um sangramento interno com risco para a vida do paciente (hemorragia intra-abdominal);
- Inchaço da panturrilha ou pernas, dor no peito, falta de ar ou cansaço repentino.
Estes sintomas podem ser sinais de formação de coágulos de sangue (eventos tromboembólicos).
Em homens
As reações adversas podem ocorrer com as frequências definidas abaixo:
- Muito comum: ocorre em pelo menos em 1 em 10 pacientes;
- Comum: ocorre em pelo menos em 1 em 100 pacientes, mas menos que 1 em 10 pacientes;
- Incomum: ocorre em pelo menos em 1 em 1.000 paciente, mas menos que 1 em 100 pacientes;
- Rara: ocorre em pelo menos em 1 em 10.000 pacientes, mas menos que 1 em 1.000 pacientes;
- Muito rara: ocorre em menos que 1 em 10.000 pacientes;
- Desconhecida: frequência que não pode ser estimada a partir dos dados disponíveis.
Reações adversas muito comuns:
- Inibição reversível da produção de esperma (espermatogênese);
- Redução do desejo sexual (diminuição da libido);
- Inabilidade para atingir ou manter a ereção (disfunção erétil).
Reações adversas comuns:
- Toxicidade do fígado, incluindo icterícia, inflamação do fígado (hepatite), falência do fígado;
- Ganho de peso corporal;
- Perda de peso corporal;
- Estados depressivos;
- Inquietação temporária;
- Crescimento das mamas (ginecomastia);
- Cansaço (fadiga);
- Ondas de calor;
- Sudorese;
- Dispneia (falta de ar, desconforto para respirar).
Reação adversa incomuns:
- Erupção de pele.
Reação adversa rara:
- Reação alérgica (hipersensibilidade).
Reação adversa muito rara:
- Tumores malignos e benignos de fígado.
Reações adversas com frequência desconhecida:
- Sangramento interno (hemorragia intra-abdominal);
- Formação de coágulos de sangue (eventos tromboembólicos);
- Tumores benignos de cérebro (meningiomas);
- Osteoporose;
- Anemia.
Em pacientes do sexo masculino que estão em tratamento com Androcur, a potência e o impulso sexual são reduzidos, assim como a função dos testículos é inibida. Estas alterações são reversíveis após a descontinuação do tratamento com Androcur.
No decorrer de várias semanas de utilização, Androcur inibe a formação de espermatozoides (espermatogênese) em consequência de sua ação antiandrogênica e antigonadotrópica. A espermatogênese retorna gradualmente em poucos meses após a descontinuação do tratamento com Androcur.
Em pacientes do sexo masculino, Androcur pode provocar crescimento anormal das glândulas mamárias (também conhecida como ginecomastia, algumas vezes combinada à sensibilidade dolorosa do mamilo ao toque), que normalmente regride após interrupção do tratamento com Androcur.
Do mesmo modo como em outros tratamentos antiandrogênicos, o uso prolongado de Androcur pode levar a osteoporose.
Foram reportados tumores cerebrais benignos (meningiomas) associados ao uso prolongado (vários anos) de Androcur na dose de 25mg ou mais.
Em mulheres
Reações adversas que podem ocorrer com frequência desconhecida:
- Tumores malignos e benignos de fígado;
- Tumores benignos de cérebro (meningiomas);
- Reação alérgica (hipersensibilidade);
- Ganho de peso corporal;
- Perda de peso corporal;
- Estados depressivos;
- Inquietação temporária;
- Redução do desejo sexual (diminuição da libido);
- Aumento do desejo sexual (aumento da libido);
- Formação de coágulos de sangue (eventos tromboembólicos);
- Dispneia (falta de ar, desconforto para respirar);
- Sangramento interno (hemorragia intra-abdominal);
- Toxicidade do fígado, incluindo icterícia, inflamação do fígado (hepatite), falência do fígado;
- Erupção de pele;
- Inibição da ovulação;
- Sensibilidade dolorosa nas mamas;
- Gotejamento (spotting);
- Cansaço (fadiga).
A ovulação é inibida durante o tratamento combinado com contraceptivo como, por exemplo, Diane 35, portanto há um estado de infertilidade temporária.
Se seu médico prescrever um contraceptivo como, por exemplo, Diane 35 em combinação com Androcur, você também deve prestar atenção nas reações adversas descritas na bula deste medicamento.
Foram reportados tumores cerebrais benignos (meningiomas) associados ao uso prolongado (vários anos) de Androcur na dose de 25mg ou mais.
Se você notar qualquer reação adversa não mencionada nesta bula, informe seu médico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
População Especial
Gravidez e Amamentação
O produto é contraindicado para mulheres grávidas ou que estejam amamentando.
Este medicamento não deve ser utilizado por mulheres grávidas ou que possam ficar grávidas durante o tratamento.
Habilidade para dirigir veículos ou operar máquinas
Androcur pode produzir cansaço e redução da energia e prejudicar sua concentração.
Composição
Cada comprimido de Androcur contém 50 ou 100mg de acetato de ciproterona.
Excipientes Androcur 50 mg: lactose, amido, povidona, estearato de magnésio, dióxido de silício.
Excipientes Androcur 100 mg: lactose, amido, povidona, estearato de magnésio.
Superdosagem
Não há relatos de efeito danoso com a ingestão de muitos comprimidos de Androcur.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Embora estudos clínicos sobre interação não tenham sido realizados, uma vez que o Acetato de ciproterona (substância ativa) é metabolizado pelo CYP3A4, espera-se que o cetoconazol, itraconazol, clotrimazol, ritonavir e outros potentes inibidores de CYP3A4 inibam o metabolismo do Acetato de ciproterona (substância ativa). Por outro lado, indutores de CYP3A4 como, por exemplo, rifampicina, fenitoína e produtos que contenham erva-de-São João podem reduzir os níveis de Acetato de ciproterona (substância ativa).
Com base em estudos de inibição in vitro, é possível que ocorra inibição do citocromo P450 e enzimas CYP2C8, 2C9, 2C19, 3A4 e 2D6 com elevadas doses terapêuticas de Acetato de ciproterona (substância ativa) de 100 mg, 3 vezes ao dia.
O risco de ocorrência de miopatia ou rabdomiólise associada ao uso de estatinas pode ser elevado quando inibidores de HMGCoA (estatinas), que são primariamente metabolizadas por CYP3A4, são administrados concomitantemente com altas doses terapêuticas de Acetato de ciproterona (substância ativa), uma vez que as duas substâncias utilizam o mesmo processo metabólico.
Ação da Substância
Resultados de eficácia
Em pacientes do sexo masculino, foi conduzido um total de 24 estudos com Acetato de ciproterona (substância ativa) em pacientes que necessitam de tratamento paliativo para carcinoma de próstata avançado. Mundialmente, mais de 1000 pacientes participaram desses estudos, os quais incluíram muitos estudos multicêntricos grandes em adição ao importante estudo multicêntrico comparativo conduzido pelo Grupo de Câncer e Oncologia Europeu.
Pacientes e o estágio da doença
Mais de 90% dos pacientes tratados com Acetato de ciproterona (substância ativa) tinham carcinoma avançado de próstata estágio C, ou carcinoma de próstata D1 ou D2 com metástase.
A maioria dos pacientes (75%) não recebeu terapia prévia ao tratamento com Acetato de ciproterona (substância ativa). Um grande grupo de pacientes recebeu vários tipos de terapia estrogênica, mas provou ser refratário ou não tolerante a droga. Poucos pacientes foram submetidos à orquiectomia ou receberam tratamento com radioterapia.
Dosagem e administração
A administração via oral de Acetato de ciproterona (substância ativa) foi utilizada em 910 pacientes (84%), enquanto 172 pacientes receberam, em solução oleosa contendo 100 mg de Acetato de ciproterona (substância ativa)/mL. A dose padrão de solução oleosa foi uma injeção intramuscular de 300 mg semanalmente. A dose oral diária variou consideravelmente de um estudo para o outro e de paciente para paciente. Entretanto, a maioria dos pacientes foi tratada com doses que variavam de 200 a 300 mg/dia. Em pacientes orquiectomizados, a dose diária em geral foi reduzida em torno de 50% para a faixa de 100 a 200 mg/dia, via oral ou a frequência de administração de solução oleosa injetável foi reduzida a uma injeção a cada duas semanas.
Apenas 32 pacientes (3%) receberam terapia concomitante com Acetato de ciproterona (substância ativa). Nenhum outro paciente recebeu terapia concomitante, mas 521 pacientes (48%) foram submetidos à orquiectomia.
Resultados dos Estudos Clínicos
Efeitos na testosterona sérica e fosfatase ácida prostática (FAP)
Os efeitos do Acetato de ciproterona (substância ativa) na testosterona sérica foram monitorados em sete estudos. A testosterona sérica foi rapidamente reduzida após dose oral diária de 200 a 300 mg, com nível estéril atingido em 1 a 4 semanas. A redução é usualmente em torno de 70 a 90%; a melhor porcentagem de redução ocorreu quando o Acetato de ciproterona (substância ativa) foi combinado com estrogênio.
Os resultados da avaliação de FAP consistentemente mostraram uma normalização dos valores em curto espaço de tempo nos pacientes responsivos. Similarmente, quando há sinais de metástase progressiva, os valores de FAP novamente se desviam dos níveis normais.
Efeitos no tumor primário
O efeito do Acetato de ciproterona (substância ativa) em tumor primário foi avaliado em um total de 678 pacientes. Destes, 489 não foram previamente tratados; o tumor primário foi reduzido em 318 desses pacientes (65%) e foi estabilizado em outros 69 (14%). Assim, a taxa de resposta positiva completa neste grupo foi 79%.
Um significativo, embora menor, percentual (59%) dos pacientes estrógeno refratários também exibiu resultados positivos.
Efeito na metástase
A metástase foi reduzida em 31% dos 216 pacientes avaliados que não foram previamente tratados, mas em apenas 13% dos pacientes estrógeno refratários avaliados. A progressão da metástase aparentou ser tempo-dependente. Apesar da redução a níveis séricos de testosterona, a metástase irá progredir por períodos de muitos meses a anos, mesmo em pacientes que foram inicialmente estabilizados. A principal causa de morte durante a terapia com Acetato de ciproterona (substância ativa) foi a progressão da metástase e não o tumor primário.
Efeito na dor
O alívio da dor foi notado em aproximadamente 50 a 80% dos pacientes que receberam tratamento com Acetato de ciproterona (substância ativa). O efeito de Acetato de ciproterona (substância ativa) na dor geralmente é comparável com seu efeito na metástase. Desde que a metástase fosse reduzida ou mantida estável, a necessidade de analgésicos também foi reduzida. Novas necessidades de analgésico foram frequentemente indicativo de progressão da metástase.
Respostas subjetivas e objetivas
Uma melhora geral na avaliação subjetiva de qualidade de vida foi alcançada em 70% dos 367 pacientes avaliados.
As avaliações objetivas de remissão foram baseadas no critério ECOG. Os melhores resultados foram obtidos quando Acetato de ciproterona (substância ativa) foi usado em combinação com a orquiectomia. Um estudo revelou que mais de 1/3 dos pacientes tratados com Acetato de ciproterona (substância ativa) alcançou remissão completa ou parcial por 3 a 5 anos. Os estudos canadenses encontraram que a remissão completa ou parcial ainda foi evidente em 75% dos pacientes após um ano de tratamento.
A taxa de sobrevida com tratamento de cinco anos ficou entre 41 a 64%. A taxa para três anos de tratamento de pacientes em estágio D foi 27% e a taxa para tratamento de 1 a 2 anos variou de menor que 15% a maior que 80%. Estas taxas de sobrevida geralmente representaram uma melhora dos resultados além daqueles previamente obtidos com a terapia estrogênica.
Em pacientes do sexo feminino, condições androgênio-dependentes como crescimento de cabelo patológica no hirsutismo, alopecia androgênica e aumento da função da glândula sebácea na acne e seborreia, são influenciadas favoravelmente por deslocamento competitivo do androgênio nos órgãos-alvo. A redução da concentração de andrógeno que resultou da propriedade antigonadotrópica do Acetato de ciproterona (substância ativa) tem um efeito terapêutico adicional. Essas alterações são reversíveis após a descontinuação da terapia.
Características Farmacológicas
Propriedades farmacodinâmicas
O Acetato de ciproterona (substância ativa) é um produto hormonal com efeito antiandrogênico.
Pacientes do sexo feminino com condições patológicas androgênio-dependentes, tais como, crescimento de pelo em hirsutismo, alopecia androgenética e ocorrência de acne e seborreia devido ao aumento das funções das glândulas sebáceas, são favoravelmente influenciadas pelo deslocamento competitivo de androgênios nos órgãos-alvo. A redução da concentração androgênica que resulta da atividade antigonadotrópica do Acetato de ciproterona (substância ativa) constitui um efeito terapêutico adicional. Estas alterações são reversíveis após a descontinuação da terapia. Durante o tratamento combinado com Acetato de ciproterona (substância ativa) + etinilestradiol, a função ovariana é inibida.
Em pacientes do sexo masculino, a potência e o impulso sexuais são reduzidos com o tratamento com Acetato de ciproterona (substância ativa) e a função das gônadas é inibida. Estas alterações são reversíveis após a descontinuação da terapia.
O Acetato de ciproterona (substância ativa) inibe competitivamente os efeitos dos androgênios nos órgãos-alvo androgênio-dependentes, por exemplo, protege a próstata dos efeitos de androgênios provenientes das gônadas e/ou do córtex adrenal.
O Acetato de ciproterona (substância ativa) tem efeito inibitório central. O efeito antigonadotrópico conduz a redução da síntese de testosterona nos testículos e, consequentemente, a redução da concentração sérica de testosterona.
O efeito antigonadotrópico do Acetato de ciproterona (substância ativa) é também exercido quando o mesmo está associado com agonistas GnRH (hormônio liberador de gonadotrofina). O aumento inicial de testosterona, provocado por este grupo de substâncias, é reduzido pelo Acetato de ciproterona (substância ativa).
Foi observada uma tendência ocasional para aumento discreto nos níveis de prolactina, quando altas doses de Acetato de ciproterona (substância ativa) são administradas.
Propriedades farmacocinéticas
Absorção
Após administração oral, o Acetato de ciproterona (substância ativa) é completamente absorvido, considerando uma extensa faixa de doses.
A biodisponibilidade absoluta do Acetato de ciproterona (substância ativa) é quase completa (88% da dose).
Distribuição
A ingestão de 50 e 100 mg de Acetato de ciproterona (substância ativa) resulta, respectivamente, em níveis séricos máximos de cerca de 140 ng/mL em aproximadamente 3 horas (50 mg) e 239,2 ± 114,2 ng/mL em 2,8 ± 1,1 horas (100 mg). Posteriormente, os níveis séricos diminuem durante um período de 24 a 120 horas, com meia-vida final de 43,9 ± 12,8 horas (50 mg) e 42,8 ± 9,7 horas (100 mg). A depuração sérica total do Acetato de ciproterona (substância ativa) foi determinada como sendo de aproximadamente 3,5 ± 1,5 mL/min/kg (50 mg) e 3,8 ± 2,2 mL/min/Kg (100 mg).
O Acetato de ciproterona (substância ativa) liga-se quase que exclusivamente à albumina plasmática. Cerca de 3,5 a 4% dos níveis totais do fármaco apresentam-se na forma livre. Uma vez que a ligação a proteínas é inespecífica, as alterações nos níveis de SHBG (globulinas ligadora de hormônios sexuais) não afetam a farmacocinética do Acetato de ciproterona (substância ativa).
Condições no estado de equilíbrio
Considerando a prolongada meia-vida da fase de disposição final do plasma (soro) e a ingestão diária do produto, pode-se esperar um acúmulo sérico de Acetato de ciproterona (substância ativa) por um fator de aproximadamente 3, durante a administração diária repetida.
Metabolismo / Biotransformação
O Acetato de ciproterona (substância ativa) é metabolizado em várias etapas que incluem hidroxilações e conjugações. O principal metabólito no plasma humano é o derivado 15 beta-hidroxilado. A fase 1 do metabolismo do Acetato de ciproterona (substância ativa) é catalisado, principalmente, pelo citocromo P450, a enzima CYP3A4.
Eliminação
Uma parte da dose é excretada inalterada pela bile. A maior parte é excretada na forma de metabólitos pelas vias urinárias e biliares, na proporção de 3:7. A meia-vida de excreção renal e biliar é de 1,9 dias. Os metabólitos do plasma são eliminados com uma taxa similar (meia-vida de 1,7 dias).
Dados pré-clínicos de segurança
Toxicidade sistêmica
Dados pré-clínicos não revelam risco específico para humanos baseados em estudos convencionais de toxicidade de dose repetida.
Embriotoxicidade / Teratogenicidade
Investigações sobre embriotoxicidade não indicaram efeito teratogênico após tratamento durante a organogênese, antes do desenvolvimento dos órgãos sexuais externos.
A administração de altas doses de Acetato de ciproterona (substância ativa) durante a fase de diferenciação hormônio-sensível dos órgãos genitais levou a sinais de feminização em fetos masculinos. A observação de recém-nascidos do sexo masculino que foram expostos ao Acetato de ciproterona (substância ativa) no útero não apresentou qualquer sinal de feminização. Entretanto, o uso de Acetato de ciproterona (substância ativa) é contraindicado durante a gravidez.
Toxicidade reprodutiva
A inibição temporária da fertilidade em ratos ocasionada pela terapia oral diária com Acetato de ciproterona (substância ativa) não indicou que o tratamento causa dano aos espermatozoides que poderia provocar malformação ou alteração da fertilidade da prole.
Genotoxicidade e carcinogenicidade
Testes de genotoxicidade, reconhecidos como de primeira linha, apresentaram resultados negativos quando conduzidos com Acetato de ciproterona (substância ativa). Entretanto, testes adicionais mostraram que o Acetato de ciproterona (substância ativa) foi capaz de produzir aductos de DNA (e aumentar a atividade de reparação do DNA) em células hepáticas de ratos e macacos e também em hepatócitos humanos isolados. O nível de aducto de DNA em células hepáticas de cães foi extremamente baixo.
Esta formação de aducto de DNA ocorreu sob exposições sistêmicas e pode ser esperada nos tratamentos com a dose recomendada de Acetato de ciproterona (substância ativa). As consequências in vivo do tratamento com Acetato de ciproterona (substância ativa) foram: aumento da incidência de lesões hepáticas focais, possivelmente pré-neoplásicas, onde enzimas celulares foram alteradas em ratas e um aumento na frequência de mutação em ratos transgênicos carregando um gene de bactéria como alvo para mutações.
A experiência clínica e estudos epidemiológicos bem conduzidos até o momento não embasam um aumento na incidência de tumores hepáticos no homem. Investigações de tumorigenicidade do Acetato de ciproterona (substância ativa) em roedores também não revelaram qualquer indicação de um potencial tumorigênico específico.
Entretanto, deve-se levar em consideração que esteroides sexuais podem promover o crescimento de determinados tumores e tecidos hormônio-dependentes.No geral, os dados disponíveis não mostram qualquer objeção ao uso de Acetato de ciproterona (substância ativa) em humanos se usado de acordo com as orientações das indicações e nas doses recomendadas.
Investigações experimentais produziram efeitos semelhantes aos corticoides nas glândulas adrenais em ratos e cães após doses mais elevadas, o que pode indicar efeitos similares em humanos na maior dose utilizada (300 mg/dia).
Cuidados de Armazenamento
O medicamento deve ser mantido em temperatura ambiente (entre 15ºC e 30°C). Proteger da umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Características organolépticas
Androcur 50mg
Comprimido branco a levemente amarelado, com marca de fracionamento em um lado e gravação “BV” em um hexágono regular do outro lado. O comprimido pode ser dividido em duas metades iguais.
Androcur 100mg
Comprimido branco a levemente amarelado, com marca de fracionamento em um lado e gravado “LA” em ambos os lados da marca de fracionamento, e um hexágono regular no lado oposto. O comprimido pode ser dividido em duas metades iguais.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
MS-1.7056.0066
Farm. Resp.:
Dra. Dirce Eiko Mimura
CRF-SP nº 16532
Fabricado por:
Delpharm Lille S.A.S.
Lys Lez Lannoy – França
Embalado por:
Schering do Brasil, Química e Farmacêutica Ltda.
São Paulo – SP
Importado por:
Bayer S.A.
Rua Domingos Jorge, 1.100 - Socorro
04779-900 - São Paulo – SP
C.N.P.J. nº 18.459.628/0001-15
Industria Brasileira
SAC 0800 7021241
[email protected]
Venda sob prescrição médica.