Comparamos o preço de Fostair Dpi Com 120 Doses Pó, veja o menor preço

R$ 211,03
RReferência
15
ofertasMelhores preços a partir de R$ 107,52 até R$ 221,85
Oferta patrocinada
vendido por Drogaria São Paulo
economize
4.88%
R$ 211,03
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogarias Pacheco
R$ 221,85
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Drogão Net
economize
51.53%
R$ 107,52
vendido por Farmácia Super Droga 10
economize
38.83%
R$ 135,70
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Farmácia Preço Popular
economize
38.81%
R$ 135,74
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Farmácia Indiana
economize
18.31%
R$ 181,22
vendido por Drogaria Primus
economize
17.51%
R$ 183,00
vendido por Agille Medicamentos
economize
15.90%
R$ 186,58
Preço Válido para compra em Boleto
vendido por Promofarma
economize
10.58%
R$ 198,37
vendido por Pague Menos
economize
10.30%
R$ 198,99
vendido por Farmácia Online Farmagora
economize
8.41%
R$ 203,20
Pagamento em até 6X sem juros. Frete Grátis! Regras no Site.
vendido por Drogaria Catarinense
economize
8.41%
R$ 203,20
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Drogaria Vera Cruz
economize
7.29%
R$ 205,68
Entregas para todo o Brasil. Clique e confira!
vendido por Drogaria Araújo
economize
7.29%
R$ 205,68
vendido por Panvel Farmácias
economize
4.88%
R$ 211,03
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Para que serve
Fostair DPI, pó para inalação contido em dispositivo Next DPI, é indicado para o tratamento do estreitamento das vias aéreas e da dificuldade de respirar associada à doenças das vias aéreas, como asma.
Fostair DPI deve ser usado por pessoas
- Cuja condição clínica da asma não está suficientemente controlada pelo uso de corticosteroides inalados e broncodilatadores de ação curta;
- Que respondam bem ao tratamento envolvendo dispositivos com corticosteroides e broncodilatadores de ação prolongada.
Fostair DPI não é indicado para o tratamento inicial da asma.
Não há dados clínicos relevantes para o uso Fostair DPI no tratamento de ataques agudos de asma.
Como o Fostair DPI funciona?
Fostair DPI é um medicamento em pó para a inalação oral (pela boca) que contém duas substâncias ativas: o dipropionato de beclometasona e o fumarato de formoterol.
O dipropionato de beclometasona pertence a um grupo de medicamentos chamado corticosteroides e age diminuindo a inflamação, inchaço e irritação das vias aéreas inferiores.
O fumarato de formoterol pertencente ao grupo de medicamentos chamado broncodilatadores de ação prolongada, ajuda a aumentar o calibre das vias aéreas.
A ação do fumarato de formoterol (broncodilatação) ocorre rapidamente, de 1 a 3 minutos após a inalação. Porém, o efeito sinérgico dos dois princípios ativos (diminuição das exacerbações da asma) só será percebido após alguns dias de tratamento.
Os dois princípios ativos facilitam a respiração ao aliviar a broncoconstrição nas vias aéreas.
Contraindicação
Você não deve utilizar o medicamento se for alérgico aos princípios ativos ou quaisquer componentes da formulação ou se você for alérgico a outros medicamentos usados para tratamento da asma.
Você não deve utilizar o medicamento se estiver apresentando sintomas agudos da asma como falta de ar, chiado e tosse, se sua asma estiver piorando ou se você estiver apresentando crise aguda de asma. Nesse caso, você deve usar o medicamento de resgate de ação rápida, o qual deve ser carregado por você a todo o momento.
Como usar
Leia atentamente as instruções para o uso correto. Se necessário, consulte o seu médico para obter explicações mais detalhadas.
Instruções de Uso do Dispositivo Next DPI
Não remova o dispositivo do cartucho e do envelope de alumínio se você não pretende usá-lo imediatamente.
Use o medicamento conforme indicado.
Se você não tiver certeza se sua dose está correta, entre em contato com seu médico ou farmacêutico.
Se você não tiver certeza que o contador de doses esteja funcionando adequadamente após a inalação, espere até a sua próxima dose e considere esta dose como normal. Não use uma dose extra.
Mantenha a tampa do dispositivo inalatório fechada nos intervalos entre as doses. Quando não estiver usando seu dispositivo, mantenha-o limpo e em local seco.
Não tente abrir ou desmontar seu dispositivo em hipótese alguma.
Não use seu dispositivo (Next DPI): após a data de validade, se estiver aberto por mais de 2 meses, se estiver quebrado, se o contador de doses mostrar “0”, se você não conseguir ler o contador de doses.
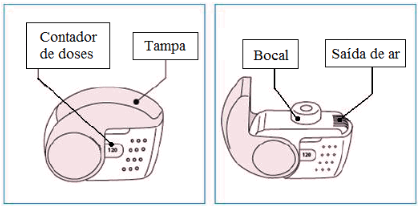
Para administrar uma dose do seu dispositivo Next DPI são necessários apenas três simples passos: abrir, inalar e fechar.
Antes de usar seu dispositivo
- Abra o cartucho e o envelope de alumínio e retire o seu dispositivo. Não use seu dispositivo se o cartucho não estiver lacrado ou se o cartucho estiver danificado.
- Verifique seu dispositivo. Se seu dispositivo estiver quebrado ou danificado não o use.
- Cheque o contador de doses. Se seu dispositivo for novo deverá aparecer “120” no mostrador.
Como usar seu dispositivo
- Verifique o número de doses restantes (qualquer número entre “1” e “120” significa que ainda existem doses restantes. Se o contador mostrar “0” não há nenhuma dose restante, descarte seu dispositivo e adquira um novo).
- Certifique-se de que a tampa esteja completamente fechada antes de usá-lo.
Abrir
-
Abra-o.
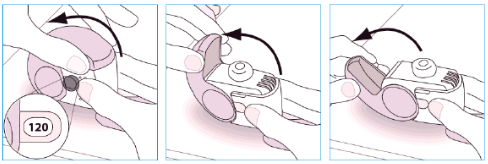
- Segure seu dispositivo firmemente na posição indicada na figura.
- Abra a tampa completamente.
Inalar
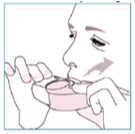
- Leve o dispositivo à boca e coloque o bocal entre os lábios.
Não tampe a saída de ar ao segurar o dispositivo.
Não inale através da saída de ar.
- Fazer uma inspiração rápida e profunda pela boca.
Você pode notar um discreto sabor doce ao utilizar a sua dose.
Você pode escutar ou sentir um clique ao utilizar sua dose.
Não inale pelo nariz.
Não remova o dispositivo dos lábios durante a inalação.
- Após a inalação, remova o dispositivo da sua boca.
- Segure o ar por 5 a 10 segundos ou o quanto for confortável.
- Expire normalmente.
Não expire através do seu dispositivo.
Fechar
- Coloque seu dispositivo na posição vertical e feche-o completamente.
- Verifique se o contador mostra uma dose inferior à dose mostrada imediatamente antes desta inalação.
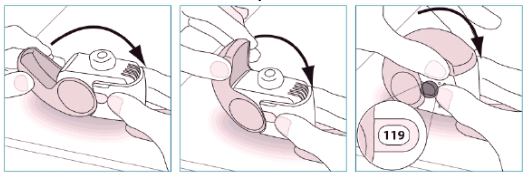
Caso necessite de outra dose, mantenha o dispositivo na posição vertical e repita as etapas 4 a 13.
Para diminuir o risco de uma infecção fúngica na boca e garganta, enxágue sua boca com água após cada inalação.
Se achar que o efeito de Fostair DPI é muito forte ou muito fraco, diga isso ao seu médico ou farmacêutico.
Se você tem dificuldade de respirar e ela piorou ou o tornou ofegante (você respira com um som de assobio), logo após a inalação, pare o tratamento imediatamente e procure seu médico.
Isso é causado pelo estreitamento das vias aéreas (broncoespasmo) em seus pulmões e pode ocorrer ao usar um dispositivo.
Limpeza
Normalmente não é necessário limpar seu dispositivo. Se necessário você pode limpar seu dispositivo após o uso com um pano seco.
Não use água ou outros líquidos para limpar essa peça. Mantenha-a seco.
Posologia
Fostair DPI deve somente ser utilizado por via inalatória (oral).
Em relação à duração do tratamento, seguir as orientações do seu médico.
As doses serão ajustadas pelo médico em cada caso.
Fostair DPI libera uma formulação extrafina que resulta em uma maior quantidade do medicamento nos pulmões, quando comparado com formulações não extrafinas. Portanto, se você fazia uso de outra medicação contendo dipropionato de beclometasona, em formulação não extrafina, e agora irá fazer uso de Fostair DPI, seu médico poderá prescrever uma dose menor de dipropionato de beclometasona, se comparado ao medicamento anteriormente utilizado. Entretanto, se você fazia uso da formulação em aerossol (Fostair aerossol) e agora irá fazer uso de
Fostair DPI não é necessário ajuste de dose. Você deve utilizar o medicamento de acordo com a orientação do seu médico.
Seu médico lhe fará regularmente um check-up a fim de certificar-se de que você esteja usando a dose correta. Uma vez que sua asma esteja bem controlada, seu médico pode considerar apropriado reduzir a dose de Fostair DPI. Você não deve, sob nenhuma circunstância, alterar sua dose sem antes falar com seu médico.
Doses Recomendadas
Uso adulto
Recomenda-se utilizar de 1 ou 2 inalações, a cada 12 horas (duas vezes ao dia).
A dose máxima diária é de 4 inalações.
Não aumente a dose.
Se você sentir que este medicamento não é eficaz, sempre converse com seu médico antes de aumentar a dose.
Lembre-se de sempre andar com o seu medicamento de resgate para tratar os sintomas de piora da asma ou uma crise súbita de asma.
Pacientes sob riscos
Pessoas idosas não precisam de ajuste de dose. Fostair DPI não é recomendado para uso em crianças.
Mesmo que esteja se sentindo melhor, não interrompa o tratamento com Fostair DPI ou diminua a dose. Caso queira fazer isso, converse com seu médico antes. É muito importante para você usar Fostair DPI todos os dias como prescrito pelo seu médico, mesmo que você não apresente mais sintomas.
Se os seus sintomas não melhorarem após o uso de Fostair DPI, você pode estar usando-o incorretamente. Portanto, verifique as instruções de uso corretamente ou entre em contato com seu médico para ele lhe ensinar como usar o dispositivo outra vez.
Se os seus sintomas piorarem ou estiverem difíceis de controlar (por exemplo, se estiver usando sua medicação de resgate com mais frequência) ou se sua medicação de resgate não estiver melhorando seus sintomas, você deve continuar usando Fostair DPI, mas deve procurar seu médico o quanto antes. Seu médico pode precisar mudar sua dose de Fostair DPI ou prescrever medicamentos adicionais.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.Não interrompa o tratamento sem o conhecimento do seu médico.
Informe ao seu médico ou cirurgião-dentista o aparecimento de sintomas novos, agravação de sintomas atuais ou retorno de sintomas antigos.
O uso inadequado do medicamento pode mascarar ou agravar sintomas.
Consulte um médico regularmente. Ele avaliará corretamente a evolução do tratamento. Siga corretamente suas orientações.
O que devo fazer quando eu me esquecer de usar o Fostair DPI?
Se esquecer de usar Fostair DPI utilize o medicamento logo que lembrar. Se for quase hora da dose seguinte, não utilize a dose faltante, apenas utilize a próxima dose no próximo horário. Não dobre a dose.
Em caso de dúvidas, procure a orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Com o propósito de se obter um efeito terapêutico total e eficaz do tratamento, torna-se indispensável que você siga rigorosamente as instruções relativas à forma de inalação de Fostair DPI.
Sempre utilize Fostair DPI exatamente como indicado pelo seu médico. Procure seu médico ou o farmacêutico caso você tenha dúvidas.
É importante você consultar seu médico regularmente. Ele fará exames para garantir que você está utilizando a dose ideal de Fostair DPI e ajustará seu tratamento à dose mais baixa que melhor controle seus sintomas.
Sob nenhuma circunstância você deve mudar a dose sem primeiro conversar com seu médico.
Se achar que o medicamento não está sendo eficaz, sempre converse com seu médico antes de aumentar a dose.
Não reduza a dose ou suspenda a medicação sem orientação do seu médico. Mesmo ao se sentir melhor, não pare de utilizar Fostair DPI nem reduza a dose. Se quiser fazê-lo, converse com seu médico. É muito importante que você use Fostair DPI regularmente mesmo se não apresentar mais sintomas.
Se achar mais difícil respirar após usar o dispositivo, pare de usá-lo imediatamente e procure assistência médica.
Se seus sintomas piorarem ou se tornarem mais difíceis de controlar (p.ex. caso você use seu dispositivo de "resgate" com mais frequência), você deve ser examinado por seu médico. Se seu dispositivo de "resgate" não melhorar seus sintomas, procure seu médico imediatamente. Sua doença pode ter piorado e seu médico pode precisar alterar sua dose ou prescrever outro medicamento.
Sempre informar o médico, nos casos de
- Doença cardíaca grave, especialmente se sofreu um ataque cardíaco recente (infarto do miocárdio), doença dos vasos coronários ou fraqueza severa dos músculos cardíacos (insuficiência cardíaca congestiva);
- Se tiver distúrbios do ritmo cardíaco como frequência cardíaca elevada ou irregular, defeito na válvula do coração ou certas anormalidades no eletrocardiograma ou qualquer outra doença cardíaca;
- Se tiver um estreitamento das artérias (doença oclusiva arterial, especialmente aterosclerose) ou abaulamento anormal da parede do vaso sanguíneo (aneurisma);
- Se tiver pressão arterial alta;
- Se tiver hiperatividade da glândula da tireoide;
- Baixos níveis de potássio no sangue (hipocalemia);
- Qualquer doença no fígado ou nos rins;
- Apresentar diabetes. A inalação de doses altas de formoterol pode elevar o nível de glicose no sangue;
- Se tiver um tumor na glândula adrenal (feocromocitoma);
- Se você estiver para realizar alguma anestesia, diga a seu médico que está usando Fostair DPI. Dependendo do tipo de anestesia planejada, pode ser necessário interromper o uso de Fostair DPI por no mínimo 12 horas antes da anestesia;
- Se tiver tuberculose pulmonar ativa ou não ativa, infecções fúngicas ou virais das vias aéreas.
Como os corticosteroides podem apresentar propriedades imunossupressoras, caso você tenha recebido vacina recentemente, informe o seu médico.
O tratamento com beta2-agonista, como formoterol contido no Fostair DPI, pode causar uma queda acentuada no nível de potássio sérico (hipocalemia), cujos sintomas são: tonturas, fadiga, paralisias, falta de ar, dor muscular, obstipação intestinal e cãibras.
Se você tem asma severa, deve ter atenção redobrada. Isso se deve ao fato de que a falta de oxigênio no sangue e outros tratamentos os quais o paciente pode estar utilizando tornam esse efeito mais forte.
Caso você esteja utilizando altas doses de corticosteroides inalados por períodos longos, pode ser necessário o aumento de dose de corticosteroides habitualmente utilizados em situações de emergência (hospitalização após um acidente, ferimento grave ou antes de uma operação, por exemplo). Nesse caso, seu médico deve ser informado para decidir a necessidade de aumentar sua dose e pode prescrever esteroide em comprimidos ou injetável.
Alguns estudos científicos têm indicado que o formoterol, um dos componentes presentes no Fostair DPI, pode aumentar o risco de morte relacionado à asma. Em caso de dúvida, procure seu médico.
Caso você precise ir ao hospital, lembre-se de levar todos os seus medicamentos e dispositivos com você, incluindo Fostair DPI e qualquer outro medicamento comprado sem prescrição, em sua embalagem original, se possível.
Antes de iniciar outro tratamento, converse com o seu médico ou farmacêutico se você estiver usando ou se usou recentemente outros medicamentos, incluindo qualquer outro dispositivo e medicamentos obtidos sem prescrição médica. Isto porque Fostair DPI pode interferir no modo de ação de alguns outros medicamentos e, além disso, alguns medicamentos podem interferir no modo de ação do Fostair DPI.
Não utilizar betabloqueadores, usados para tratar diversos problemas no coração, hipertensão e glaucoma (pressão aumentada nos olhos), com este medicamento. Se você precisar usar betabloqueadores (inclusive colírio), o efeito do formoterol pode se tornar reduzido ou o formoterol pode, inclusive, não fazer nenhum efeito.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Uma vez que Fostair DPI contém dipropionato de beclometasona e fumarato de formoterol, o tipo e severidade das reações adversas associadas a cada composto podem ser previstos. Não há incidência de eventos adversos adicionais após a administração concomitante dos dois compostos.
Reações adversas reportadas durante os estudos clínicos e experiência clínica com Fostair DPI
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento)
- Não foram relatadas reações muito comuns até o momento.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento)
- Tremores.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento)
- Nasofaringite (inflamação da mucosa nasal);
- Candidíase na boca;
- Hipertrigliceridemia (aumento de triglicérides no sangue);
- Dor de cabeça;
- Aumento ou diminuição dos batimentos do coração;
- Angina pectoris (dor no coração);
- Isquemia do miocárdio (falta de oxigênio no coração);
- Irritação na garganta;
- Crise asmática;
- Dispneia (falta de ar);
- Dor orofaríngea;
- Disfonia (alteração da voz);
- Tosse;
- Náusea;
- Fadiga;
- Irritabilidade;
- Alterações em eletrocardiograma (prolongamento do intervalo QT e/ou progressão lenta da onda R);
- Diminuição de cortisol livre na urina;
- Diminuição da concentração de cortisol no sangue;
- Aumento do potássio no sangue;
- Aumento da glicose sanguínea.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento)
- Não foram relatadas reações raras até o momento.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento)
- Não foram relatadas reações muito raras até o momento.
Reações adversas típicas associadas ao uso de formoterol
- Tremores;
- Dores de cabeça;
- Aumento ou diminuição dos batimentos do coração;
- Dor no coração (angina pectoris);
- Falta de oxigênio no coração (isquemia do miocárdio);
- Prolongamento do intervalo QT.
Reações adversas não observadas na experiência clínica com doses terapêuticas de Fostair DPI, mas tipicamente associadas com a administração de medicamentos da mesma classe do formoterol são
- Palpitações;
- Alterações no batimento do coração (fibrilação atrial, extra-sístole ventricular, taquiarritmia);
- Níveis baixos de potássio;
- Aumento ou diminuição da pressão sanguínea.
Reações ocasionalmente reportadas durante terapia inalatória com formoterol
- Insônia;
- Tontura;
- Inquietação;
- Ansiedade.
Formoterol pode também induzir cãibras e dores musculares.
Reações adversas típicas associadas ao uso de beclometasona
- Nasofaringite;
- Candidíase oral;
- Disfonia;
- Irritação da garganta;
- Irritabilidade;
- Diminuição de cortisol livre na urina;
- Diminuição da concentração sanguínea de cortisol;
- Aumento da glicemia.
Reação adversa não observada na experiência clínica com doses terapêuticas de Fostair DPI, mas tipicamente associada com a administração de dipropionato de beclometasona é
- Infecção fúngica oral;
- Pneumonia.
Distúrbio de paladar tem sido ocasionalmente reportado durante a terapia com corticoide inalatório.
Usar altas doses de corticosteroides inalatórios por um longo período pode ocasionar
- Alteração da função da sua glândula adrenal (adrenossupressão);
- Alteração da densidade da massa óssea;
- Alteração do crescimento de crianças e adolescentes;
- Aumento da pressão ocular (glaucoma), catarata;
- Rápido ganho de peso (particularmente na face e no tronco);
- Insônia, depressão, preocupação, irritação, nervosismo, inquietação, excitação (esses sintomas são mais prováveis de ocorrerem em crianças);
- Comportamento anormal.
Assim como ocorre com outras terapêuticas inalatórias, podem surgir espasmos da musculatura bronquial (broncoespasmos paradoxais). Eles são caracterizados pela presença de sons em sibilos (chiados no peito), que aparecem quando você respira imediatamente após o processo da inalação da medicação, e por piora da tosse.
Caso isso ocorra, interrompa o tratamento e procure imediatamente seu médico.
Informe seu médico imediatamente se você apresentar reações alérgicas, que incluem
- Alergias na pele;
- Coceira;
- Erupções na pele;
- Vermelhidão;
- Inchaço da pele e de mucosas, especialmente dos olhos, da face, lábios e garganta.
Reações adversas reportadas para medicamento semelhante contendo a associação de dipropionato de beclometasona e formoterol
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento):
Não foram relatadas reações muito comuns até o momento.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento)
- Faringite;
- Candidíase oral;
- Cefaleia;
- Disfonia.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento)
- Gripe;
- Infecção fúngica ora;
- Candidíase orofaríngea, esofágica e vulvovaginal;
- Gastroenterite;
- Sinusite;
- Rinite;
- Pneumonia;
- Granulocitopenia;
- Dermatite alérgica;
- Hipocalemia;
- Hiperglicemia;
- Inquietação;
- Tontura;
- Tremor;
- Otite (infecção no ouvido);
- Palpitações;
- Eletrocardiograma com prolongamento do intervalo QT corrigido;
- Alteração em eletrocardiograma;
- Taquicardia;
- Taquiarritmia;
- Fibrilação atrial (um tipo de arritmia do coração);
- Hiperemia;
- Rubor;
- Tosse;
- Tosse produtiva;
- Irritação na garganta;
- Crise asmática;
- Diarreia;
- Boca seca;
- Dispepsia;
- Disfagia;
- Sensação de queimação nos lábios;
- Náusea;
- Disgeusia (alteração no paladar);
- Prurido;
- Erupção cutânea;
- Hiperidrose (sudorese excessiva);
- Urticária;
- Câimbra muscular;
- Mialgia (dores musculares);
- Proteína C-reativa elevada;
- Contagem de plaquetas elevada;
- Aumento nos ácidos graxos livres;
- Aumento na insulina sanguínea;
- Aumento de corpos cetônicos sanguíneos;
- Diminuição do cortisol sanguíneo.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento)
- Extrassístole ventricular (contração prematura do ventrículo do coração);
- Angina pectoris (dor no coração);
- Broncoespasmo paradoxal;
- Angioedema;
- Nefrite (inflamação nos rins);
- Aumento na pressão sanguínea;
- Diminuição da pressão sanguínea.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento)
- Trombocitopenia;
- Reações de hipersensibilidade, incluindo eritema;
- Edema nos lábios, face, olhos e faringe;
- Supressão adrenal;
- Catarata;
- Glaucoma;
- Dispneia (falta de ar);
- Exacerbação da asma;
- Retardo no crescimento em crianças e adolescentes;
- Edema periférico;
- Diminuição da densidade óssea.
Reação cuja frequência é desconhecida
- Hiperatividade psicomotora;
- Distúrbios do sono;
- Ansiedade;
- Depressão;
- Agressividade;
- Mudanças comportamentais (predominantemente em crianças).
Todas as reações adversas descritas acima podem ocorrer durante o uso de Fostair DPI. Caso você apresente algumas destas reações ou apresente qualquer outra reação não descrita, informe seu médico, cirurgião-dentista ou farmacêutico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe a empresa sobre o aparecimento de reações indesejáveis e problemas com este medicamento, entrando em contato através do serviço de atendimento ao consumidor (SAC).
Atenção: este produto é um medicamento que possui nova forma farmacêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer reações adversas imprevisíveis ou desconhecidas. Nesse caso, informe seu médico ou cirurgião- dentista.
População Especial
Gravidez e lactação
Não há dados clínicos sobre mulheres usando o Fostair DPI durante a gravidez.
Se estiver grávida, converse com seu médico antes de usar este medicamento. Você deve usar Fostair DPI somente se seu médico achar que os benefícios do medicamento para você são superiores a qualquer risco potencial à sua criança. Isso se aplica especialmente aos primeiros três meses de gravidez. Não se deve utilizar este medicamento enquanto estiver em período de amamentação, salvo se seu médico achar que os benefícios são superiores a qualquer risco potencial à sua criança.
Converse com seu médico ou farmacêutico antes de utilizar/usar qualquer medicamento.
Uso em idosos
Não é necessário ajuste de dose para pacientes idosos.
Uso em crianças
Não está indicado para uso em crianças.
Uso em pacientes com insuficiência hepática e renal
Não há dados disponíveis sobre o uso de Fostair DPI em pacientes com comprometimento hepático ou renal.
Efeitos sobre a capacidade de conduzir e utilizar máquinas
É improvável que Fostair DPI cause qualquer efeito sobre a capacidade de dirigir e operar máquinas. Porém, se você apresentar eventos adversos como tontura e tremor, sua capacidade em conduzir ou operar máquinas pode ficar prejudicada.
Composição
Cada dose de Fostair DPI contém:
|
Dipropionato de beclometasona | 100 mcg |
| Fumarato de formoterol | 6 mcg |
| Excipiente q.s.p. | 1 dose |
Excipientes: lactose monoidratada e estearato de magnésio.
Superdosagem
Se você usar uma quantidade maior do que deveria de Fostair DPI entre em contato com seu médico ou vá a um hospital mais próximo para receber instruções. Leve seu medicamento com você. Reações adversas podem ocorrer.
Informe seu médico caso sinta qualquer sintoma não usual. Seu médico pode querer alguns exames ou decidir as melhores medidas a serem adotadas.
Se você utilizar mais formoterol do que deveria pode ter os seguintes efeitos
- Sensação de enjoo;
- Aceleração dos batimentos do coração,;
- Palpitações;
- Distúrbios do ritmo cardíaco;
- Certas alterações no eletrocardiograma,;
- Cefaleia;
- Tremor;
- Sensação de sono;
- Baixos níveis de potássio no sangue;
- Altos níveis de glicose no sangue.
Já o uso excessivo de dipropionato de beclometasona pode resultar em uma diminuição temporária do funcionamento de suas glândulas adrenais. Não é necessária ação emergencial uma vez que a função adrenal se recupera em poucos dias.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações sobre como proceder.
Interação Medicamentosa
Interações farmacocinéticas
O dipropionato de beclometasona é submetido a um metabolismo muito rápido via enzimas esterase sem envolvimento do sistema do citocromo P450.
Interações farmacodinâmicas
?-bloqueadores (incluindo colírios) devem ser evitados por pacientes asmáticos. Caso sejam administrados por motivos maiores, o efeito do formoterol será reduzido ou extinto. Por outro lado, o uso concomitante de outros medicamentos ?-adrenérgicos pode ter efeitos potencialmente aditivos, portanto é necessário ter cuidado quando teofilina ou outro ?-adrenérgico for prescrito concomitantemente com formoterol.
O tratamento concomitante com quinidina, disopiramida, procainamida, fenotiazinas, alguns anti-histamínicos (como a terfenadina), inibidores da monoaminooxidase e antidepressivos tricíclicos pode prolongar o intervalo de QTc e elevar o risco de arritmias ventriculares. Além disso, L-Dopa, L-tiroxina, oxitocina e álcool podem comprometer a tolerância cardíaca à ?2 simpatomiméticos. O tratamento concomitante com inibidores da monoaminooxidase, incluindo agentes com propriedades semelhantes, como furazolidona e procarbazina, podem precipitar reações hipertensivas.
Há um risco elevado de arritmia em pacientes recebendo anestesia concomitante com hidrocarbonos halogenados. Tratamento concomitante com derivados da xantina, esteroides ou diuréticos podem potencializar um possível efeito de hipocalemia do ?-2-agonista. A hipocalemia pode elevar a disposição à arritmia em pacientes tratados com glicosídeos digitálicos.
Há um potencial teórico de interação particularmente em pacientes sensíveis utilizando dissulfiram ou metronidazol, pois Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) (aerossol) contém álcool e sua interação com dissulfiram pode causar vermelhidão e com metronidazol pode ocorrer vermelhidão, vômitos e taquicardia.
Os pacientes devem ser avisados que o Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) (aerossol) contém pequena porcentagem de álcool. Em doses normais, não há risco para os pacientes.
Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) Pó para Inalação para inalação contém lactose. Pacientes com raros problemas hereditários de intolerância a galactose, deficiência de Lapp lactase ou a má absorção de glicose-galactose, não devem usar Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) Pó para Inalação.
Ação da Substância
Resultados de eficácia
Dados de Segurança Pré Clínica
A toxicidade observada em estudos com animais com dipropionato de beclometasona e formoterol, administrados em combinação ou separadamente, foram decorrentes de efeitos associados à atividade farmacológica aumentada. Eles estão relacionados à atividade imunossupressora de dipropionato de beclometasona e aos efeitos cardiovasculares conhecidos do formoterol, evidentes principalmente em cães. Não foram observadas elevações da toxicidade ou ocorrência de achados inesperados.
Estudos da reprodução de ratos (0,2; 2,0 e 20 mg/kg/dia) apresentaram efeitos dependentes da dose. Não foram observados efeitos na fertilidade de machos, ao passo que o NOAEL (maior nível em que não se observou efeito adverso) em fêmeas e no desenvolvimento fetal foi de 2 mg/kg/dia. Em doses mais altas (20 mg/kg/dia), Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) induziu dificuldades no parto e sinais de toxicidade materna (taxa de implantação reduzida, peso reduzido da placenta) e fetal (distúrbios da ossificação, peso reduzido). Sabe-se que a administração de corticosteroides em doses altas a animais prenhes pode causar anormalidades no desenvolvimento fetal incluindo fissura palatal e retardo do crescimento intra-uterino. A ação tocolítica de agentes simpatomiméticos ?-2 pode influenciar o parto.
Dados não clínicos dos componentes individuais de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) não mostraram perigo para humanos, baseado nos estudos convencionais de segurança farmacológica e de toxicidade de dose repetida. O perfil de toxicidade da combinação refletiu os de toxicidade dos componentes separados sem aumento na toxicidade ou de achados inesperados.
Estudos sobre a reprodução de ratos mostrou efeitos dependentes de dose. A presença de altas doses de dipropionato de beclometasona foi associada com a redução na fertilidade das fêmeas, diminuição no número de implantações e toxicidade embriofetal.
Sabe-se que altas doses de corticosteroides em animais prenhos causam anormalidades no desenvolvimento fetal incluindo fenda palatal e crescimento intrauterino diminuído, e é provável que os efeitos observados com o uso da combinação dipropionato de beclometasona/formoterol sejam em função do dipropionato de beclometasona. Estes efeitos foram observados apenas com exposição sistêmica elevada ao metabólito ativo B-17-MP (beclometasona 17-monopropionato), mais de 200 vezes dos níveis séricos esperados em pacientes. Além disso, aumento na duração da gestação e do parto, atribuído ao efeito tocolítico do ?-2-simpatomimético foi visto em estudos com animais. Estes efeitos foram observados quando o nível sérico materno de formoterol era menor que o nível esperado em pacientes tratados com Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa).
Não foram realizados estudos de oncogenicidade com Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa). Contudo, não foi evidenciado potencial de mutagenicidade com a combinação, e os dados relatados por indivíduos não sugerem qualquer risco potencial de oncogenicidade em homens.
Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) (aerossol)
Eficácia clínica pata a terapia de manutenção
A eficácia da combinação fixa de beclometasona e formoterol (BDP/F - Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa)) foi avaliada em um estudo randomizado, controlado, durante 3 meses, em pacientes com asma moderada que permaneciam sintomáticos apesar de receberem baixa dose de corticoide inalatório, até 500 mcg/dia de beclometasona (BDP) ou equivalente.
Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) foi aplicado, por inalação, duas vezes ao dia, provando ser mais eficaz na melhora da função pulmonar que uma dose dupla equipotente de BDP não extrafina.
Uma segunda investigação foi realizada em pacientes com asma mais severa, caracterizada por sintomas recorrentes e insuficiência respiratória, apesar do tratamento com até 1000 mcg/dia de BDP ou equivalente. Nesse contexto, BDP/formoterol, administrado 2 vezes ao dia durante seis meses, mostrou uma melhoria no pico do fluxo expiratório (PFE) e volume expiratório forçado (FEV1), comparável com a de um regime equipotente, não extrafino, de aplicação de beclometasona e formoterol administrado através de dispositivoes separados, e provou ser mais eficaz do que 1000 mcg/dia de beclometasona não extrafina.
Além disso, a combinação fixa de beclometasona/formoterol foi superior a monoterapia com beclometasona e formoterol inalados separadamente ou com a monoterapia utilizando-se beclometasona apenas, em termos percentuais de medidas necessárias para o controle clínico da asma, sugerindo que os pacientes que recebem a combinação extrafina de beclometasona e formoterol podem apresentar benefícios adicionais que são estendidos a melhora da função pulmonar.
O percentual de pacientes com exacerbações de asma que requerem esteroides por via oral (percentagem referida como pacientes com exacerbações graves) foi menor no grupo tratado com a combinação fixa de beclometasona e formoterol (6,0%) do que aqueles que recebem beclometasona e formoterol separadamente (12,1%) ou beclometasona isoladamente (14,1%).
A medida dos níveis de cortisol sérico na semana 24 foi significativamente maior no grupo que recebeu a combinação fixa de beclometasona e formoterol em relação aos valores basais, enquanto que nenhuma alteração foi observada nos outros dois grupos, sugerindo que a combinação do Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) produziu uma menor inibição do eixo hipotálamo-pituitária-adrenal comparado com os outros tratamentos.
Estes resultados estão de acordo com a baixa ingestão de esteroides, que caracteriza a formulação do Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa). Finalmente, nenhuma anormalidade clinicamente significativa foi observada em relação ao potássio sérico e glicose.
Em dois estudos clínicos “head-to-head” (comparação direta), foram avaliadas a eficácia e tolerabilidade da beclometasona e formoterol (BDP/F (Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa))) vs budesonida/ formoterol (BUD/F) e propionato de fluticasona/salmeterol (FP/S). Os dois estudos partilharam um desenho de estudo semelhante. O critério de inclusão dos pacientes no estudo foram sintomas da asma e função pulmonar (VEF1) < 80% do previsto, apesar de receberem até 1000 mcg / dia BDP ou equivalente.
No primeiro estudo, os pacientes que receberam 2 inalações duas vezes ao dia de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) apresentaram melhora na função pulmonar, medida pela avaliação do (PEF), antes da administração do medicamento pela manhã, que era comparável com a de um regime equipotentes de 2 aplicações duas vezes ao dia de BUD/F 200/6 mcg.
Notadamente, quando a velocidade de broncodilatação que foi avaliada como a mudança no VEF1 nos primeiros 60 min após a dose de manhã, no primeiro e no último dia do tratamento, Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) (BDP / F) demonstrou um início de ação equivalente à dos BUD/F. Ambos os tratamentos foram igualmente eficazes na melhora dos sintomas da asma e aumento da percentagem de dias sem o uso de medicação de resgate. No segundo ensaio (Papi et al 2007b), BDP/F foi comparada com propionato de fluticosana / salmeterol (FP/S) 125/25 mcg, os dois administrados em 2 doses 2 vezes ao dia.
BDP/F mostraram melhora no PFE e VEF1 comparável aos efeitos da PF/S quando a função pulmonar foi medida na pré-dose. O início da broncodilatação, avaliada como uma mudança no VEF1 nos primeiros 60 minutos após a dose de manhã, no primeiro e no último dia de tratamento, foi significantemente mais rápida com o Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) (BDP / F) do que com FP / S, devido principalmente às propriedades farmacodinâmicas do formoterol.
Eficácia Clínica para a terapia de manutenção e alívio
Em um estudo paralelo de 48 semanas envolvendo 1701 pacientes com asma, a eficácia de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) administrado como terapia de manutenção (1 dose, duas vezes ao dia) e alívio (até um total de 8 puffs ao dia) foi comparada ao Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) administrado como terapia de manutenção (1 dose, duas vezes ao dia) mais salbutamol quando necessário em pacientes adultos com asma moderada ou severa não controlada e >80% dos pacientes utilizando beta2-agonistas de longa ação ao início do estudo. O objetivo primário do estudo foi demonstrar a superioridade de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) utilizado como manutenção e alívio em termos de tempo para a primeira exacerbação severa da asma.
O resultado confirmou que Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) utilizado como terapia de manutenção e alívio prolongou significativamente o tempo para a primeira exacerbação severa quando comparado com Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) administrado como manutenção mais salbutamol quando necessário (p< 0,001 para ambos população ITT e PP) e reduziu o risco de ocorrer uma exacerbação severa da asma em 36% (IC: 18% - 51%) versus salbutamol quando necessário. Exacerbações que requerem corticoesteróides orais e hospitalizações ou visitas ao serviço de emergência foram significativamente menores no grupo utilizando Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) como terapia de manutenção e alívio.
Pacientes utilizando Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) como terapia de manutenção e alívio alcançaram uma melhora significativa no controle da asma.
CT07 Resultados Secundários
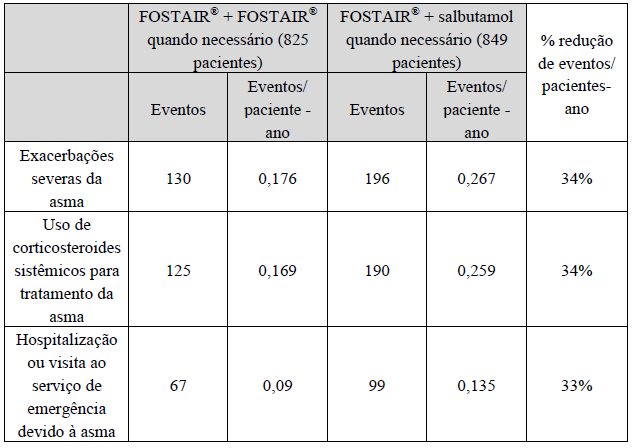
P<0,001 Dipropionato de beclometasona/fumarato de Formoterol + Dipropionato de Beclometasona/fumarato de Formoterolquando necessário versus Dipropionato de Beclometasona/fumarato de Formoterol + salbutamol quando necessário.
Em outro estudo clínico, uma dose simples de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) 100/6 mcg provocou um efeito broncodilatador acelerado e um alívio rápido dos sintomas de dispneia similar ao do salbutamol 200 mcg/dose em pacientes asmáticos quando desafio com metacolina é utilizado para induzir a broncoconstrição.
Avaliar o efeito da beclometasona + formoterol versus budesonida + formoterol (não inferioridade) e em comparação com o formoterol (superioridade), em pacientes com doença pulmonar obstrutiva crônica grave estável (DPOC)
Um estudo duplo-cego, double-dummy, randomizado, controlado com ativo, de grupos paralelos foi realizado em pacientes com DPOC de severa intensidade, durante 48 semanas.
Após 4 semanas de run-in com o ipratrópio + salbutamol (40/200 mcg, três vezes ao dia), os pacientes foram randomizados para receber beclometasona + formoterol (200/12 mcg em inalador pressurizados dosimetrados), budesonida + formoterol (400/12 mg com inalador de pó seco) ou formoterol (12 mg inalador de pó seco), administrados duas vezes ao dia, durante 48 semanas. Co-variáveis de eficácia primária foi a mudança dos valores basais do FEV1 após 48 semanas de tratamento e a taxa média das exacerbações da DPOC.
Resultados
Dos 718 pacientes randomizados, 703 (232 beclometasona + formoterol, 238 com budesonida + formoterol e 233 com formoterol) foram avaliados na análise ITT. Melhora na pré-dose do VEF1 matinal foi de 0,077 L, 0,080 L e 0,026 L com beclometasona / formoterol, budesonida / formoterol e formoterol, respectivamente (LS médio do modelo ANCOVA). Beclometasona / formoterol não foi inferior ao de budesonida / formoterol (95% IC da diferença 0,052, 0,048) e superior com o formoterol (p = 0,046). A taxa geral de exacerbações de COPD / paciente / ano foi semelhantes e não significativamente estatisticamente diferente entre os tratamentos (beclometasona / formoterol 0,414, budesonida / formoterol 0,423 e formoterol 0,431). Qualidade de vida e sintomas da DPOC melhoraram em todos os grupos e uso de medicação de emergência diminuiu.
Perfis de segurança foram como esperado e os tratamentos, bem tolerado.
Conclusões
Beclometasona / formoterol (400/24 mcg) durante 48 semanas, melhorou a função pulmonar, reduziu os sintomas em comparação com o formoterol, foi seguro e bem tolerado em pacientes com DPOC estável grave.
Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) Pó para Inalação
A eficácia dos dois componentes de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) pó para inalação foi avaliada em dois estudos separados em comparação com 100 microgramas/6 microgramas solução inalatória pressurizada em pacientes sintomáticos com asma moderada a grave.
No primeiro estudo, o objetivo inicial era avaliar a eficácia do componente corticoide inalatório sobre a broncodilatação (FEV1 pré-dose). Uma melhora clínica significativa na pré-dose FEV1 foi observada em 696 pacientes sintomáticos com asma moderada a grave ao final do terceiro mês de tratamento, em comparação com os valores basais, com uma inalação duas vezes ao dia ou com duas inalações, duas vezes ao dia para ambas as formulações. Foi observado um aumento médio de pelo menos 250 mL. Não há diferenças clínicas relevantes na FEV1 pré-dose entre Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) pó para inalação e a solução inalatória pressurizada em ambas as dosagens.
Medidas de controle da asma como sintomas da asma matinais e noturnos e porcentagem de dias sem sintomas melhoraram significativamente do basal para o final do tratamento, particularmente para as duas maiores doses de ambas as formulações. Nenhuma diferença foi encontrada entre as duas formulações em ambas as dosagens.
Em um segundo estudo, o objetivo primário era avaliar a eficácia do agonista ?-2 adrenérgico de longa ação, componente do Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) Pó para Inalação. Neste estudo, o início de ação broncodilatadora e até 12 horas após a administração de doses únicas foi mensurada através de avaliações espirométricas de FEV1 (FEV1 AUC de pelo menos 80% da duração de ação do formoterol). Em comparação ao placebo, Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) Pó para Inalação uma inalação e quatro inalações de ambos os ativos melhora significativamente o FEV1 AUC0-12.
Ambas as doses de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) pó para inalação foram não inferiores a dose correspondente da formulação solução inalatória pressurizada. Uma dose resposta estatisticamente significativa foi encontrada com ambas as formulações entre a menor e a maior dose.
Outro estudo aberto, realizado com placebo, foi conduzido a fim de verificar se o fluxo inspiratório que pode ser gerado através do dispositivo Next Pó para inalação não é influenciado pela idade do paciente, doença e severidade da doença e, portanto, a ativação e a biodisponibilidade do fármaco a partir do aparelho podem ser atingidas por todos os pacientes.
O desfecho primário foi a porcentagem de pacientes capazes de ativar o dispositivo de acordo com a faixa etária e com o estágio da doença. Oitenta e nove pacientes, na faixa etária de 5-84 anos, incluindo asmáticos moderados a graves (FEV1 > 60% e ? 60% previsível, respectivamente), e pacientes com DPOC moderada e grave (FEV1 ? 50% e < 50% previsível, respectivamente) participaram do estudo clínico.
Todos os pacientes independentemente da idade, doença, ou severidade da doença, foram capazes de gerar um fluxo inspiratório suficiente para ativar o dispositivo Next Pó para inalação.
Características farmacológicas
Mecanismos de Ação e Efeitos Farmacodinâmicos
Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) na forma de aerossol (solução pressurizada contendo o gás HFA) ou na forma de pó para inalação, liberando partículas extrafinas com uma média de diâmetro aerodinâmico de massa de 1.4-1.5 micrômetros e uma deposição pulmonar alta e homogênea. As partículas extrafinas são em média muito menores que as partículas de formulações não extrafinas.
Um estudo de deposição do fármaco marcado com radioisótopos, em adultos asmáticos, mostrou que a maioria do fármaco (55% da dose emitida) se depositou nos pulmões e uma quantidade limitada (43% da dose emitida) teve deposição extratorácica. Estas características de liberação permitem uma baixa dose de corticosteroide com melhores efeitos farmacodinâmicos, os quais mostraram ser equivalentes a uma dose correspondente de solução pressurizada para inalação.
Os mecanismos de ação das duas substâncias são discutidos a seguir.
O dipropionato de beclometasona, administrado por inalação e em doses recomendadas, apresenta ação anti-inflamatória, resultando em redução dos sintomas e exacerbações da asma, com menos efeitos adversos do que quando corticosteroides são administrados por via sistêmica.
Formoterol é um agonista ?-2-adrenérgico seletivo que produz relaxamento do músculo liso brônquico em pacientes com obstrução reversível das vias aéreas. O efeito broncodilatador surge rapidamente, em 1-3 minutos após a inalação, e dura 12 horas após uma única administração.
Propriedades Farmacocinéticas
A exposição sistêmica aos princípios ativos dipropionato de beclometasona e formoterol na combinação fixa do medicamento foi comparada à exposição sistêmica dos componentes isolados, em estudo clínico.
Para o dipropionato de beclometasona, a AUC do seu principal metabólito ativo Beclometasona 17-monopropionato (B-17-MP) e sua concentração plasmática máxima foram inferiores após a administração da combinação fixa, porém, a taxa de absorção foi mais rápida em comparação à administração de beclometasona isolada.
Para o formoterol, a concentração plasmática máxima foi semelhante após a administração da combinação fixa ou dos componentes isolados e a exposição sistêmica foi ligeiramente superior após administração de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa).
Não houve evidência de interações farmacocinética ou farmacodinâmica entre dipropionato de beclometasona e formoterol.
Em um estudo realizado em voluntários sadios, o uso de Dipropionato de Beclometasona + Fumarato de Formoterol (substância ativa) aerossol com o espaçador Aerochamber Plus aumentou a deposição de dipropionato de beclometasona e formoterol no pulmão sem aumentar a exposição sistêmica total em comparação ao uso do dispositivo de aplicação padrão (bocal em L).
Dipropionato de beclometasona
O dipropionato de beclometasona é uma pró-droga com fraca afinidade de ligação com o receptor de glicocorticoide que é hidrolisado via enzimas esterase para um metabólito ativo que é a beclometasona-17-monopropionato (B-17-MP), o qual tem uma atividade anti-inflamatória tópica mais potente se comparado à pró-droga (dipropionato de beclometasona).
Absorção e distribuição
O dipropionato de beclometasona inalado é rapidamente absorvido pelos pulmões; antes da absorção há uma vasta conversão de dipropionato de beclometasona em seu metabólito ativo B-17-MP.
A biodisponibilidade do dipropionato de beclometasona deglutido é insignificante, mas a conversão pré-sistêmica para B-17-MP resulta em 41% de absorção como B-17-MP. Há um aumento aproximadamente linear na exposição sistêmica com o aumento da dose inalada.
A biodisponibilidade absoluta após a inalação é de aproximadamente 2% e 62% da dose nominal para o dipropionato de beclometasona inalterado e B-17-MP, respectivamente.
Após a administração intravenosa, a disposição de dipropionato de beclometasona e B-17-MP se caracteriza por alta depuração plasmática (150 e 120L/h respectivamente), com pequeno volume de distribuição em estado de equilíbrio para dipropionato de beclometasona (20L) e ampla distribuição tecidual para B-17-MP (424L). A disposição metabólica do dipropionato de beclometasona resulta principalmente em seu metabólito ativo (B-17-MP). A ligação proteica plasmática é moderadamente elevada (87%).
Metabolismo
O dipropionato de beclometasona é depurado muito rapidamente da circulação sistêmica, pelo metabolismo mediado via enzimas esterases que são encontradas na maioria dos tecidos. O principal produto do metabolismo é o metabólito ativo (B-17-MP). Metabólitos secundários inativos, 21-monopropionato de beclometasona (B-21-MP) e beclometasona (BOH) também são formados, mas eles contribuem pouco com a exposição sistêmica.
Excreção
A excreção fecal é a principal via de eliminação de dipropionato de beclometasona, principalmente como metabólitos polares. A excreção renal de dipropionato de beclometasona e seus metabólitos são desprezíveis. As meias-vidas de eliminação terminal são 0,5h e 2,7 h para dipropionato de beclometasona e B17MP, respectivamente.
Populações especiais
Uma vez que o dipropionato de beclometasona é submetido a um metabolismo muito rápido via enzimas esterases (presentes no líquido intestinal, soro, pulmões e fígado,) para originar produtos mais polares (B-21-MP, B-17-MP e BOH), é pouco provável que o comprometimento hepático modifique o perfil de segurança e a farmacocinética do dipropionato de beclometasona. A farmacocinética do dipropionato de beclometasona em pacientes com comprometimento renal não foi estudada.
Não é esperado que a insuficiência hepática modifique a farmacocinética e o perfil de segurança do dipropionato de beclometasona. Uma vez que o dipropionato de beclometasona ou seus metabólitos não foram observados na urina, uma elevação na exposição sistêmica não foi verificada em pacientes com comprometimento renal.
Formoterol
Absorção e distribuição
Após a inalação, o formoterol é absorvido a partir dos pulmões e do trato gastrointestinal. A fração de dose inalada que é engolida depende do tipo de dispositivo usado e da técnica de inalação: com um MDI (aerossol) pode chegar a 90%, portanto, os dados relacionados à administração oral são relevantes para a via inalatória. No mínimo 65% de uma dose oral de formoterol foi absorvido a partir do trato gastrointestinal, embora 70% tenha sido submetido ao metabolismo pré-sistêmico.
As concentrações plasmáticas de pico do medicamento inalterado ocorreu em 0,5 a 1 hora da administração oral. A ligação proteica plasmática de formoterol foi 61-64% com 34% de ligação com albumina. Não houve saturação de ligação na faixa de concentração atingida com doses terapêuticas.
A meia-vida de eliminação determinada após a administração oral foi de 2-3 horas. A absorção de formoterol foi linear após a inalação de 12 a 96 ?g de fumarato de formoterol.
Metabolismo
O formoterol é amplamente metabolizado e a via proeminente envolve conjugação direta no grupo hidroxila fenólico. O conjugado ácido glicuronídeo é inativo. A segunda principal via envolve a O-desmetilação seguida por conjugação no grupo 2’-hidroxila fenólico. Isoenzimas do Citocromo P450 CYP2D6, CYP2C19 e CYP2C9 estão envolvidas na O-desmetilação de formoterol. O fígado parece ser o local primário de metabolismo. O formoterol não inibe as enzimas CYP450 em concentrações terapeuticamente relevantes.
Excreção
A excreção urinária cumulativa de formoterol após inalação única de um Pó para inalação (pó inalatório) aumentou linearmente na faixa de dose 12 – 96 ?g. Em média, 8% e 25% da dose foi excretada como formoterol inalterado e total, respectivamente. Com base nas concentrações plasmáticas medidas após a inalação de uma dose única de 120 ?g em 12 voluntários saudáveis, a meia-vida de eliminação terminal média foi determinada como sendo 10 horas.
Os enantiômeros (R,R) e (S,S) representaram cerca de 40% e 60% do medicamento inalterado excretado na urina, respectivamente.
A proporção relativa dos dois enantiômeros permaneceu constante na faixa de dose estudada e não houve evidência de acúmulo relativo de um enantiômero sobre o outro após a administração repetida.
Após a administração oral (40 a 80 ?g), 6% a 10% da dose foi recuperado na urina como medicamento inalterado em sujeitos de pesquisa saudáveis; até 8% da dose foi recuperada como glicuronídeo. Um total de 67% de uma dose oral de formoterol é excretado na urina (principalmente como metabólitos) e o restante nas fezes. A depuração renal de formoterol é de 150 mL/min.
Populações especiais
A farmacocinética de formoterol, até o momento, não foi estuda em pacientes com insuficiência renal e hepática.
Cuidados de Armazenamento
Não remova o dispositivo do cartucho e do envelope de alumínio até o momento do uso. Mantenha a tampa do dispositivo inalatório fechada nos intervalos entre as doses. Conservar o medicamento Fostair DPI em temperatura ambiente (15 a 30ºC) e proteger da umidade.
Fostair DPI é um dispositivo multidose de plástico (dispositivo Next DPI) com pó branco e inodoro (sem cheiro).
Depois de aberto, este medicamento pode ser utilizado em 2 meses.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido.
Para a sua segurança, mantenha o medicamento na embalagem original.
Antes de usar, observe o aspecto do medicamento. Caso você observe alguma mudança no aspecto do medicamento que ainda esteja no prazo de validade, consulte o médico ou o farmacêutico para saber se poderá utilizá-lo.
Mensagens de Alerta
Este medicamento é contraindicado para menores de 18 anos.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Este medicamento pode causar doping.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Reg. M.S.: 1.0058.0114
Farmacêutica Responsável:
C.M.H. Nakazaki
CRF-SP nº 12.448
Fabricado por:
Chiesi Farmaceutici S.p.A
Parma - Itália
Importado por:
Chiesi Farmacêutica Ltda.
Uma empresa do Grupo Chiesi Farmaceutici S.p.A
Rua Dr. Giacomo Chiesi nº 151 - Estrada dos Romeiros km 39,2
Santana do Parnaíba - S.P.
CNPJ n° 61.363.032/0001-46
Venda sob prescrição médica.