Comparamos o preço de Insulina - Novomix 30 5 Pen, veja o menor preço

R$ 413,60
BBiológicos
2
ofertasMelhores preços a partir de R$ 413,60 até R$ 446,60
Oferta patrocinada
vendido por Drogaria São Paulo
economize
7.39%
R$ 413,60
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogarias Pacheco
R$ 446,60
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Para que serve
Este medicamento é usado no tratamento de diabetes mellitus.
Como NovoMix funciona?
Diabetes Mellitus é uma doença na qual seu organismo não produz insulina suficiente para controlar o nível de açúcar no sangue. NovoMix 30 diminui a concentração de açúcar no sangue. NovoMix 30 é uma insulina moderna (análogo de insulina) que apresenta tanto ação rápida como ação prolongada,na proporção 30/70. Insulinas modernas são versões aperfeiçoadas da insulina humana.
Este medicamento começará a reduzir o nível de açúcar do seu sangue de 10 a 20 minutos após a aplicação, atingindo seu efeito máximo entre 1 e 4 horas após a aplicação e com duração do efeito por até 24 horas.
NovoMix 30 pode ser usado em combinação com medicamentos antidiabéticos orais.
Contraindicação
Não use NovoMix 30:
- Se for alérgico (hipersensível) à insulina asparte ou a qualquer um dos componentes do produto;
- Se você tiver sintomas de hipoglicemia (sintomas de baixo nível de açúcar no sangue);
- Em bombas de infusão de insulina;
- Se o carpule ou o sistema de aplicação contendo o carpule tiver sofrido uma queda, estiver danificado ou amassado;
- Se não foi armazenado corretamente ou se foi congelado;
- Se a insulina não estiver uniformemente branca e leitosa após ser ressuspendida;
- Se após a ressuspensão grânulos de material estiverem presentes ou se partículas brancas sólidas estiverem aderidas ao fundo ou na parede do carpule.
Este medicamento é contraindicado para menores de 10 anos.
Como usar
Converse com seu médico e enfermeiro sobre sua necessidade de insulina.
Sempre use NovoMix 30 Penfill conforme prescrito pelo seu médico e siga suas orientações cuidadosamente.
Quando NovoMix 30 é usado em combinação com medicamentos antidiabéticos orais, a dose deve ser ajustada.
Se o seu médico trocar o seu tipo ou marca de insulina por outra, ele poderá ter que ajustar a sua dose. Não mude sua dose de insulina sem orientação de seu médico.
Faça uma refeição ou um lanche contendo carboidrato dentro de 10 minutos após a injeção para evitar hipoglicemia.
Geralmente, NovoMix 30 é administrado antes da refeição. Quando necessário, pode ser aplicado logo após a refeição.
População especial
Se você apresenta função renal ou hepática reduzida, ou se você tem mais de 65 anos, você deve medir seu nível de açúcar no sangue mais regularmente e discutir as alterações na sua dose de insulina com seu médico.
- Antes de utilizar NovoMix 30:
- Verifique o rótulo para ter certeza de que é o tipo correto de insulina;
- Verifique sempre o carpule, incluindo o êmbolo de borracha. Não utilize o carpule se tiver algum dano visível ou se existir um espaço entre o êmbolo de borracha e a faixa branca do rótulo Isso pode ser resultado de vazamento de insulina. Se você suspeitar que o carpule esteja danificado, devolva ao seu fornecedor. Consulte o manual de instruções do sistema de aplicação para obter mais informações;
- Use sempre uma agulha nova a cada injeção para evitar a contaminação.
- As agulhas e NovoMix 30 Penfill não devem ser compartilhados.
Como e onde usar esta insulina:
NovoMix 30 deve ser aplicado sob a pele (via subcutânea). Nunca injete sua insulina diretamente na veia ou músculo.
Sempre alterne o local da injeção dentro da mesma região a cada injeção, isso reduz o risco de desenvolvimento de caroços ou lesões na pele.
Os melhores locais para você se aplicar a injeção são:
A parte da frente da sua cintura (abdome), as nádegas, a parte da frente de suas coxas ou a parte superior dos braços. Sua insulina agirá mais rapidamente se você injetá-la na parte da frente de sua cintura.
Você deve medir seu nível de açúcar no sangue regularmente.
Instruções de Uso
Ressuspensão da insulina:
Confira se há no mínimo 12 unidades de insulina restantes no carpule para permitir a ressupensão. Se houver menos de 12 unidades, use um carpule novo.
Toda vez que usar um carpule novo (antes de colocar o carpule dentro do sistema de aplicação):
Deixa a insulina atingir a temperatura ambiente antes do uso. Isso facilita a ressuspensão.
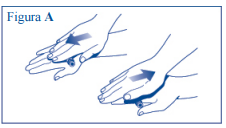
- Role o carpule entre as palmas das mãos 10 vezes. É importante que o carpule seja mantido na horizontal (veja a figura A).
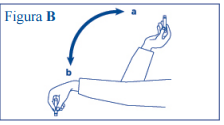
- Mova o carpule para cima e para baixo entre as posições “a” e “b” (veja a figura B) 10 vezes de forma que a esfera de vidro se desloque de uma extremidade do carpule para a outra.
- Repita a rolagem e o procedimento de movimentação (veja as figuras A e B) até que o líquido apresente um aspecto uniformemente branco e leitoso. Não use a insulina se após a ressuspensão o líquido não apresentar aspecto uniformemente branco e leitoso.
- Complete as outras etapas de aplicação imediatamente.
Para cada injeção:
Mova o sistema de aplicação, com o carpule dentro, para cima e para baixo entre as posições “a” e “b” (veja a figura B), pelo menos 10 vezes até que o líquido apresente um aspecto uniformemente branco e leitoso.
Complete as outras etapas de aplicação imediatamente.
Como injetar esta insulina:
- Injete a insulina sob a pele. Use a técnica de injeção aconselhada pelo seu médico ou enfermeiro, e descrita no manual do seu sistema de aplicação.
- Mantenha a agulha sob a pele durante pelo menos 6 segundos. Mantenha o botão injetor totalmente pressionado até que a agulha tenha sido retirada da pele. Isto garantirá a aplicação correta e evitará a entrada de sangue na agulha e no carpule de insulina.
- Após cada injeção, não se esqueça de retirar e descartar a agulha e guarde NovoMix 30, sem a agulha acoplada.
- Caso contrário, o líquido poderá vazar e gerar doses imprecisas.
Não preencha os carpules novamente.
NovoMix 30 Penfill foi desenvolvido para ser usado com os sistemas de aplicação de insulina e agulhas da Novo Nordisk. Se você for tratado com NovoMix 30 Penfill e outra insulina em carpule, você deve usar um sistema de aplicação para cada tipo de insulina.
Como medida de precaução, sempre leve um carpule Penfill de reserva, para o caso de perda ou dano do carpule.
Posologia
A dosagem de NovoMix 30 é individual e determinada de acordo com as necessidades do paciente.
Em pacientes com diabetes Tipo 2, NovoMix 30 pode ser administrado em monoterapia ou em combinação com medicamentos antidiabéticos orais, quando a glicose sanguínea é controlada de modo inadequado somente com estes antidiabéticos orais. Para pacientes com diabetes tipo 2, a recomendação para iniciar a dose de NovoMix 30 é 6 U no café da manhã e 6 U no jantar (refeição da noite). NovoMix 30 também pode ser iniciado uma vez ao dia com 12 U no jantar (refeição da noite). Quando NovoMix 30 é usado uma vez ao dia, geralmente, recomenda-se mudar para duas vezes ao dia quando atingir 30 unidades, dividindo a dose em partes iguais no café da manhã e no jantar.
O regime de três vezes ao dia com NovoMix 30 pode ser iniciado com segurança a partir do regime de dose de duas vezes ao dia com a divisão da dose da manhã, nas doses da manhã e do almoço.
O seguinte guia de titulação é recomendado para o ajuste da dose:
|
Nível de glicose antes da refeição |
Ajuste de dose de | |
|
< 4,4 mmol/L | < 80 mg/dL |
- 2U |
|
4,4 – 6,1 mmol/L | 80 – 110 mg/dL |
0 |
|
6,2 – 7,8 mmol/L | 111 – 140 mg/dL |
+ 2 U |
|
7,9 – 10 mmol/L | 141 – 180 mg/dL |
+ 4 U |
|
> 10 mmol/L | > 180 mg/dL |
+ 6 U |
O menor nível antes da refeição dos três dias anteriores deve ser usado. A dose não deve ser aumentada se ocorrer hipoglicemia nestes três dias. O ajuste de dose pode ser feito uma vez por semana até que o alvo de HbA1C seja atingido. O nível de glicose antes da refeição deve ser utilizado para avaliar a adequação da dose anterior.
Em pacientes com diabetes tipo 1, a necessidade individual de insulina está usualmente entre 0,5 e 1,0 Unidade/kg/dia, e esta necessidade pode ser parcial ou totalmente suprida por NovoMix 30.
A necessidade diária pode ser maior em pacientes com resistência à insulina (por exemplo, devido à obesidade), e menor em pacientes produção de insulina endógena residual.
Transferência de outra insulina:
Ao transferir o tratamento de pré-mistura de insulina humana para NovoMix 30, comece com o mesmo regime de dose. Então, ajuste a dose de acordo com as necessidades individuais (vide orientações de titulação na tabela acima).
Idosos:
NovoMix 30 pode ser usado por pacientes idosos; entretanto existe experiência limitada com o uso de NovoMix 30 em combinação com ADOs em pacientes com mais de 75 anos.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar NovoMix 30?
Caso você se esqueça de aplicar NovoMix 30, o seu nível de açúcar no sangue pode ficar muito alto (isto é chamado de hiperglicemia).
Os sinais de aviso da hiperglicemia aparecem gradualmente.
Estes incluem:
Aumento da micção, sensação de sede, perda de apetite, sensação de enjôo (náuseas ou vômitos), sensação de sonolência ou cansaço, pele seca e corada, boca seca e hálito com cheiro de fruta (cetona).
Estes podem ser sinais de uma condição muito grave chamada cetoacidose diabética (acúmulo de ácido no sangue, pois o organismo está utilizando gordura ao invés de açúcar). Se esta condição não for tratada poderá resultar em coma diabético e morte. Se você apresentar qualquer um dos sinais mencionados acima, meça seu nível de açúcar no sangue, teste sua urina para detectar cetonas, se possível, e procure auxílio médico imediatamente.
A hiperglicemia também pode acontecer se você:
- Não injetar insulina suficiente;
- Injetar repetidamente menos insulina que o necessário;
- Tiver uma infecção ou febre;
- Comer mais do que o habitual;
- Fizer menos exercício do que o habitual.
Se você parar de usar sua insulina:
Isto pode levar a hiperglicemia grave e cetoacidose. Não pare de usar sua insulina sem consultar seu médico, ele lhe dirá o que é necessário ser feito.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Leia toda a bula com atenção antes de começar a usar sua insulina.
Mantenha esta bula com você. Você pode precisar lê-la novamente.Se você tiver dúvidas adicionais, pergunte ao seu médico, enfermeiro ou farmacêutico.
Este medicamento foi prescrito exclusivamente para você. Não o dê para outras pessoas, pois poderá causar danos até mesmo se os sintomas forem os mesmos que os seus.
Se você apresentar qualquer efeito colateral mesmo aqueles não mencionados nesta bula, consulte seu médico, enfermeiro ou farmacêutico.
Tenha cuidado especial com NovoMix 30 se você:
- Tiver problemas nos rins ou no fígado, ou nas glândulas adrenal, pituitária ou tireoide;
- Se exercitar mais do que o usual ou se pretende alterar a sua dieta habitual, já que isso pode afetar seu nível de açúcar no sangue;
- Estiver doente continue usando sua insulina e consulte seu médico;
- For viajar para o exterior viagens para locais com fuso horário diferente podem afetar as necessidades de insulina e os horários das injeções. Consulte seu médico se você está planejando viajar.
Gravidez e amamentação
Se você estiver grávida ou planejando engravidar, consulte o seu médico. A experiência clínica com NovoMix 30 na gravidez é limitada. Sua dose de insulina pode necessitar de ajustes durante a gravidez e após o parto. O controle cuidadoso do diabetes, particularmente prevenção de hipoglicemia, é importante para a saúde do bebê.
Não há restrições no tratamento com NovoMix 30 durante a amamentação.
Se você está grávida não pare de usar sua insulina e procure orientação médica ou do cirurgião-dentista.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Dirigindo e usando máquinas
Se seu nível de açúcar no sangue está alto ou baixo, sua habilidade para concentrar-se ou reagir pode ser prejudicada, portanto, sua habilidade de dirigir e operar máquinas também. Tenha isto em mente em todas as situações que possam representar um risco para você ou para outros. Consulte seu médico se você pode dirigir ou operar máquinas:
- Se você tem hipoglicemias frequentemente.
- Se você acha difícil reconhecer uma hipoglicemia.
População Pediátrica
NovoMix 30 pode ser usado em crianças e adolescentes com idade de 10 anos ou mais quando a pré-mistura de insulina for necessária. Para crianças entre 6 e 9 anos existem dados limitados de estudos clínicos.
Este medicamento pode causar doping.
Principais interações medicamentosas
Muitos medicamentos afetam seu nível de açúcar no sangue e isso pode significar que sua dose de insulina talvez precise ser alterada. Consulte seu médico ou farmacêutico se você estiver tomando ou tomou recentemente qualquer outro medicamento além de NovoMix 30, mesmo aqueles não prescritos. Estão listados abaixo os medicamentos mais comuns que podem afetar seu tratamento com insulina.
Se você usar algum dos medicamentos abaixo, seu nível de açúcar no sangue pode diminuir (hipoglicemia):
- Outros medicamentos para o tratamento do diabetes.
- Inibidores da monoaminaoxidase (IMAO) (usados para tratar depressão).
- Beta-bloqueadores (usados para tratar pressão alta).
- Inibidores da enzima conversora de angiotensina (ECA) (usados para tratar certas doenças cardíacas ou pressão alta).
- Salicilatos (usados para aliviar a dor e baixar a febre).
- Esteroides anabólicos (como testosterona).
- Sulfonamidas (usadas para tratar infecções).
Se você usar algum dos medicamentos abaixo, seu nível de açúcar no sangue pode aumentar (hiperglicemia):
- Anticoncepcionais orais (para o controle de natalidade).
- Tiazidas (usadas para tratar pressão alta e retenção de líquido).
- Glicocorticoides (como “cortisona”, usados no tratamento da inflamação).
- Hormônios da tireoide (usados para tratar distúrbios da glândula tireoide).
- Simpatomiméticos (como epinefrina [adrenalina], ou salbutamol, terbutalina usados para tratar asma).
- Hormônio do crescimento (medicamento para estimulação do crescimento e que exerce grande influência nos processos metabólicos do corpo).
- Danazol (medicamento que atua na ovulação).
- Octreotida e lanreotida (usados no tratamento de acromegalia, um distúrbio hormonal raro que, geralmente, ocorre em adultos de meia idade, causada pelo excesso de produção de hormônio de crescimento pela hipófise) podem aumentar ou diminuir seu nível de açúcar no sangue.
- Beta-bloqueadores (usados para tratar pressão alta) podem diminuir ou eliminar inteiramente os primeiros sintomas de alerta que ajudam a reconhecer uma hipoglicemia.
- Tiazolidinedionas (classe de medicamentos antidiabéticos orais usados para o tratamento de diabetes tipo 2). Alguns pacientes portadores de diabetes tipo 2 de longa data, doença cardíaca ou derrame prévio que são tratados com tiazolidinedionas em combinação com insulina podem desenvolver insuficiência cardíaca. Informe seu médico assim que possível se você apresentar sinais de insuficiência cardíaca, assim como falta de ar ou aumento rápido no peso ou inchaço localizado (edema).
Usando NovoMix 30 com álcool:
Se você ingerir álcool sua necessidade de insulina pode mudar, pois seu nível de açúcar no sangue pode aumentar ou diminuir. É recomendado um monitoramento cuidadoso.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Reações Adversas
Como os demais medicamentos, NovoMix 30 pode causar efeitos colaterais, embora nem todos pacientes apresentem estes efeitos.
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento):
Baixo nível de açúcar no sangue (hipoglicemia).
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
Sinais de alergia:
Podem ocorrer reações (dor, vermelhidão, urticária,inchaço, coceira, inflamação) no local de aplicação (reações alérgicas locais). Essas reações geralmente desaparecem após algumas semanas de uso da sua insulina. Se não desaparecerem, procure seu médico.
Procure o médico imediatamente:
- Se os sinais de alergia se espalharem a outras partes do corpo; ou
- Se você se sentir mal repentinamente e começar a transpirar, começar a ficar enjoado (vômitos), tiver dificuldade em respirar, tiver batimentos cardíacos rápidos, sentir tonturas.
- Problemas de visão: quando você iniciar o seu tratamento com insulina pela primeira vez, você poderá sofrer distúrbios da visão, mas a reação geralmente desaparece.
Alterações no local da injeção (lipodistrofia):
O tecido gorduroso (adiposo) sob a pele no local de aplicação reduz (lipoatrofia) ou aumentar (lipohipertrofia).
Alternar o local da injeção a cada aplicação pode diminuir o risco de desenvolvimento destas alterações na pele. Se você observar marcas ou espessamento da pele no local da injeção, informe o seu médico ou enfermeiro, porque estas reações podem agravar-se ou podem alterar a absorção da insulina se você injetar nesse local;
Inchaço nas articulações:
Quando você começa a usar insulina, a retenção de líquidos pode provocar edema (inchaço) ao redor dos tornozelos e de outras articulações. Normalmente, esta situação desaparece rapidamente.
Retinopatia diabética (uma doença nos olhos relacionada ao diabetes que pode levar à perda de visão):
Se você tem retinopatia diabética e o seu nível de glicose no sangue melhorar muito rapidamente, a retinopatia pode piorar.
Pergunte ao seu médico sobre este assunto.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
Neuropatia dolorosa (dor devido à lesão no nervo associada ao diabetes):
Se o seu nível de glicose no sangue melhorar muito rapidamente, você pode ter dor – isso é chamado de neuropatia dolorosa aguda e geralmente é passageira.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento):
Reação alérgica grave a NovoMix 30 ou a um dos seus componentes (chamada de reação alérgica sistêmica).
Se qualquer efeito colateral piorar, ou se você notar qualquer efeito colateral não mencionado nesta bula, consulte seu médico, enfermeiro ou farmacêutico.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe também à empresa através do seu serviço de atendimento.
Composição
Cada mL da suspensão injetável contém
100 U de insulina asparte (30% de insulina asparte solúvel e 70% de insulina asparte protaminada) produzida por tecnologia de DNA recombinante.
Excipientes: glicerol, fenol, metacresol, cloreto de zinco, cloreto de sódio, fosfato de sódio dibásico di-hidratado, sulfato de protamina, hidróxido de sódio, ácido clorídrico e água para injetáveis. Um carpule contém 3 mL equivalente a 300 U.
Superdosagem
Se você aplicar uma grande quantidade de insulina, o nível de açúcar em seu sangue pode ficar muito baixo (isto é chamado de hipoglicemia). Isto também pode acontecer:
- Se você comer muito pouco ou perder uma refeição.
- Se você se exercitar mais do que o habitual.
- Se você beber bebida alcoólica.
Os sinais de aviso de uma hipoglicemia podem surgir repentinamente e podem incluir:
Suor frio, pele fria e pálida, cefaleia (dor de cabeça), batimento cardíaco rápido, mal-estar, fome excessiva, alterações temporárias na visão, sonolência, sensação incomum de cansaço e fraqueza, nervosismo ou tremores, sensação de ansiedade, sensação de desorientação, dificuldade de concentração.
Se você sentir sintomas de hipoglicemia, coma um alimento rico em açúcar e, em seguida, meça seu açúcar no sangue.
Se seu nível de açúcar no sangue estiver muito baixo, coma tabletes de glicose ou outro alimento rico em açúcar (doces, bolachas, suco de frutas) e, então, descanse.
Sempre carregue tabletes de glicose, doces, bolachas ou suco de frutas com você, no caso de você necessitar.
Quando os sintomas de hipoglicemia tiverem desaparecido ou quando os níveis de glicose no sangue estiverem estáveis, continue seu tratamento com insulina.
Informe aos seus parentes e amigos que você é portador de diabetes e quais podem ser as consequências, incluindo o risco de desmaio (ficar inconsciente) durante a hipoglicemia. Informe-os que se você desmaiar, eles devem virar você de lado e procurar auxílio médico imediatamente. Eles não devem lhe dar qualquer alimento ou bebida, pois isto pode engasgá-lo.
Você pode recuperar-se mais rapidamente da inconsciência com a aplicação de uma injeção do hormônio glucagon, dada por uma pessoa treinada. Se você receber uma injeção de glucagon, terá necessidade de glicose ou de um alimento açucarado logo que recuperar a consciência. Se você não responder ao tratamento com glucagon, terá que receber tratamento num hospital.
- Se a hipoglicemia grave não for tratada poderá causar uma lesão cerebral (temporária ou permanente) e até mesmo a morte.
- Se você tiver um episódio de hipoglicemia que o faça desmaiar, ou se você teve a necessidade de receber uma injeção de glucagon, ou se você tem passado por vários episódios de hipoglicemia, converse com seu médico. A quantidade ou os horários de aplicações de sua insulina, sua alimentação ou exercícios podem necessitar de ajustes.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Sabe-se que vários medicamentos interagem com o metabolismo da glicose.
As seguintes substâncias podem reduzir as necessidades de insulina do paciente
- Antidiabéticos orais;
- Inibidores da monoaminooxidase (IMAOs);
- Beta-bloqueadores;
- Inibidores da enzima conversora da angiotensina (ECA);
- Salicilatos;
- Esteroides anabólicos;
- Sulfonamidas.
As seguintes substâncias podem aumentar as necessidades de insulina do paciente
- Contraceptivos orais;
- Tiazidas;
- Glicocorticoides;
- Hormônios da tireoide;
- Simpatomiméticos;
- Hormônio do crescimento;
- Danazol.
Os agentes beta-bloqueadores podem mascarar os sintomas da hipoglicemia.
Octreotida/lanreotida podem aumentar ou diminuir as necessidades de insulina.
Interação Alimentícia
O álcool pode intensificar ou reduzir o efeito hipoglicêmico da insulina.
Ação da Substância
Resultados de eficácia
Adultos
Dois estudos de segurança e eficácia, abertos, controlados com comparador ativo, com seis meses de duração foram realizados para comparar a segurança e eficácia de Insulina Asparte (substância ativa) e Novolin R® em pacientes adultos com diabetes tipo 1.
Visto que os desenhos e os resultados dos estudos foram muito similares, os dados mostrados são apenas de um estudo (vide Tabela 1).
Insulina Asparte (substância ativa) foi administrado subcutaneamente imediatamente antes das refeições e insulina humana regular foi administrada subcutaneamente 30 minutos antes das refeições.
A insulina humana NPH foi administrada como insulina basal em dose única diária ou em doses divididas.
Alterações ma HbA1c e as taxas de incidência de hipoglicemia grave (determinada pelo número de eventos que requer intervenção por terceiros) foram comparáveis entre os dois tratamentos neste estudo (Tabela 1) assim como no outro estudo clínico mencionado.
Cetoacidose diabética não foi relatada em nenhum dos estudos com adultos e nenhum dos grupos de tratamento.
Tabela 1: Administração subcutânea de Insulina Asparte (substância ativa) em pacientes com diabetes tipo 1 (24 semanas; n=882)2
| Insulina Asparte (substância ativa) + insulina NPH | Novolin R + insulina NPH | |
| N | 596 | 286 |
| HbA1c inicial (%)* | 7,9 ± 1,1 | 8,0 ± 1,2 |
| Alteração da HbA1c inicial (%) | -0,1 ± 0,8 | 0,0 ± 0,8 |
| Diferença entre os tratamentos na média da HbA1c (95% intervalo de confiança) | -0,2 (-0,3, -0,1) | |
| Dose de insulina inicial (UI/Kg/24 horas)* | 0,7 ± 0,2 | 0,7 ± 0,2 |
| Dose de insulina no final do estudo (UI/Kg/ 24 horas)* | 0,7 ± 0,2 | 0,7 ± 0,2 |
| Pacientes com hipoglicemia grave (n, %)** | 104 (17%) | 54 (19%) |
| Peso corporal inicial (Kg)* | 75,3 ± 14,5 | 75,9 ± 13,1 |
| Variação de peso inicial (Kg)* | 0,5 ± 3,3 | 0,9 ± 2,9 |
* Valores são a média ± DP.
** Hipoglicemia grave se refere à hipoglicemia associada com sintomas do sistema nervosa central e que requerem a intervenção de outra pessoa ou hospitalização.
Um estudo de segurança e eficácia, aberto, controlado com comparador ativo, com seis meses de duração foi realizado para comparar a segurança e eficácia de Insulina Asparte (substância ativa) e insulina humana regular em pacientes com diabetes tipo 2 (Tabela 2).
Insulina Asparte (substância ativa) foi administrado subcutaneamente imediatamente antes das refeições e insulina humana regular foi administrada subcutaneamente 30 minutos antes das refeições.
Insulina humana NPH foi administrada como insulina basal em dose única diária ou em doses divididas.
Alterações na HbA1c e as taxas de hipoglicemia grave (determinada pelo número de eventos que requer intervenção por terceiros) foram comparáveis em ambos os tratamentos.
Tabela 2: Administração subcutânea de Insulina Asparte (substância ativa) em pacientes com diabetes tipo 2 (6 meses; n=176)3
| Insulina Asparte (substância ativa) + insulina NPH | Novolin R + insulina NPH | |
| N | 90 | 86 |
| HbA1c inicial (%)* | 8,1 ± 1,2 | 7,8 ± 1,1 |
| Alteração da HbA1c inicial (%) | -0,3 ± 1,0 | -0,1 ± 0,8 |
| Diferença entre os tratamentos na média da HbA1c (95% intervalo de confiança) | -0,1 (-0,4, -0,1) | |
| Dose de insulina inicial (UI/Kg/24 horas)* | 0,6 ± 0,3 | 0,6 ± 0,3 |
| Dose de insulina no final do estudo (UI/Kg/ 24 horas)* | 0,7 ± 0,3 | 0,7 ± 0,3 |
| Pacientes com hipoglicemia grave (n, %)** | 9 (10%) | 5 (8%) |
| Peso corporal inicial (Kg)* | 88,4 ± 13,3 | 85,8 ± 14,8 |
| Variação de peso inicial (Kg)* | 1,2 ± 3,0 | 0,4 ± 3,1 |
* Valores são a média ± DP.
** Hipoglicemia grave se refere a hipoglicemia associada com sintomas do sistema nervosa central e que requerem a intervenção de outra pessoa ou hospitalização.
População pediátrica
Um estudo de segurança e eficácia, com grupos paralelos e 24 semanas de duração com crianças e adolescentes com diabetes tipo 1 (n = 283) com idade entre 6 e 18 anos, comparou dois regimes de tratamento com múltiplas doses subcutâneas diárias: Insulina Asparte (substância ativa) (n = 187) ou insulina humana regular (n = 96).
Insulina NPH foi administrada como insulina basal.
Insulina Asparte (substância ativa) demonstrou controle glicemico comparável ao da insulina humana regular, como medido pela alteração na HbA1c (Tabela 3) e ambos os grupos de tratamentos tiveram incidência de hipoglicemia comparáveis.
A administração subcutânea de Insulina Asparte (substância ativa) e insulina humana regular também foi comparada em um estudo de segurança e eficácia com crianças com diabetes tipo 1 ( n = 26) com idade entre 2 e 6 anos com efeito similar na HbA1c e na hipoglicemia.
Tabela 3: Administração subcutânea de Insulina Asparte (substância ativa) em crianças com diabetes tipo 1 (24 semanas; n=283)4
| Insulina Asparte (substância ativa) + insulina NPH | Novolin R + insulina NPH | |
| N | 187 | 96 |
| HbA1c inicial (%)* | 8,3 ± 1,2 | 8,3 ± 1,3 |
| Alteração da HbA1c inicial (%) | 0,1 ± 1,0 | 0,1 ± 1,1 |
| Diferença entre os tratamentos na média da HbA1c (95% intervalo de confiança) | 0,1 (-0,5, -0,1) | |
| Dose de insulina inicial (UI/Kg/24 horas)* | 0,4 ± 0,2 | 0,6 ± 0,2 |
| Dose de insulina no final do estudo (UI/Kg/ 24 horas)* | 0,4 ± 0,2 | 0,7 ± 0,2 |
| Pacientes com hipoglicemia grave (n, %)** | 11 (6%) | 9 (9%) |
| Cetoacidose diabética (n, %) | 10 (5%) | 2 (2%) |
| Peso corporal inicial (Kg)* | 50,6 ± 19,6 | 48,7 ± 15,8 |
| Variação de peso inicial (Kg)* | 2,7 ± 3,5 | 2,4 ± 2,6 |
Gravidez
Um estudo de segurança e eficácia, aberto e randomizado comparou Insulina Asparte (substância ativa) (n = 157) versus insulina humana regular (n =165) em 322 mulheres grávidas com diabetes tipo 1.
Dois terços das pacientes incluídas já estavam grávidas quando entraram no estudo.
A taxa de malformações congênitas foi de 5,7% com Insulina Asparte (substância ativa) versus 7,3% com insulina humana. A diferença não foi estatisticamente significativa.
80% das pacientes em ambos os grupos alcançou HbA1c média abaixo de 6,5% durante a gravidez, e não houve diferença significativa na incidência de hipoglicemia materna.
A Insulina Asparte (substância ativa)e reduz de maneira eficiente a glicemia e as excursões glicêmicas com menos eventos hipoglicêmicos noturnos.
Estudos clínicos controlados foram conduzidos em aproximadamente 2.000 pacientes, comparando Insulina Asparte (substância ativa)e (Insulina Asparte (substância ativa)) com insulina humana.
A terapia intensificada com Insulina Asparte (substância ativa)e resultou em um controle metabólico superior quando comparado à insulina humana em portador de diabetes tipo 1, quando avaliada a HbA1c após 6 meses de tratamento.
Características farmacológicas
Propriedades Farmacodinâmicas
Mecanismo de Ação
Insulina Asparte (substância ativa) apresenta um início de ação mais rápido comparado à insulina humana regular, juntamente com uma concentração de glicose reduzida, como avaliado dentro das primeiras quatro horas após uma refeição.
Insulina Asparte (substância ativa) tem uma menor duração de ação comparado à insulina humana regular após injeção subcutânea.
Quando Insulina Asparte (substância ativa) é injetado subcutaneamente, o início de ação ocorre de 10 a 20 minutos da injeção.
O efeito máximo é exercido entre 1 e 3 horas após a injeção.
A duração de ação é de 3 a 5 horas.
A Insulina Asparte (substância ativa)e é equipotente à insulina humana regular em base molar.
Adultos
Estudos clínicos com pacientes com diabetes Tipo 1 demonstraram uma glicemia pós-prandial inferior com Insulina Asparte (substância ativa) quando comparado com insulina humana regular.
Em dois estudos abertos de longa duração com pacientes com diabetes Tipo 1, compreendendo 1070 e 884 pacientes, respectivamente, Insulina Asparte (substância ativa) reduziu a hemoglobina glicada em 0,12 pontos percentuais [95% I.C. 0,03;0,22] e 0,15 pontos percentuais [95% I.C. 0,05;0,26] quando comparado à insulina humana regular; sem diferença significativa.
Idosos
Um estudo farmacocinético/farmacodinâmico duplo-cego cruzado, randomizado comparando Insulina Asparte (substância ativa)e com insulina humana regular foi realizado com pacientes idosos com diabetes tipo 2 (19 pacientes com idade de 65 a 83 anos, idade média 70 anos).
As diferenças relativas nas propriedades farmacodinâmicas (GIRmáx, AUCGIR, 0-120 min) entre Insulina Asparte (substância ativa)e e insulina humana regular em idosos foram similares àquelas observadas em voluntários sadios e em pacientes mais jovens com diabetes.
Crianças e adolescentes
Quando administrado em crianças, Insulina Asparte (substância ativa) demonstrou controle similar da glicose a longo prazo quando comparado à insulina humana regular.
Um estudo clínico comparando insulina humana regular pré-prandial com Insulina Asparte (substância ativa)e pós-prandial foi realizado com crianças pequenas (26 pacientes com idade de 2 a 6 anos) e um estudo farmacocinético/farmacodinâmico de dose única foi realizado em crianças (6-12 anos) e adolescentes (13-17 anos).
O perfil farmacodinâmico da Insulina Asparte (substância ativa)e nas crianças foi similar ao observado em adultos.
Estudos clínicos em pacientes com diabetes Tipo 1 demonstraram um risco reduzido de hipoglicemia noturna com Insulina Asparte (substância ativa)e quando comparado com insulina humana regular.
O risco de hipoglicemia durante o dia não foi significativamente aumentado.
Gravidez
Um estudo clínico comparando a segurança e eficácia da Insulina Asparte (substância ativa)e versus insulina humana regular no tratamento de mulheres grávidas com diabetes Tipo 1 (322 grávidas expostas (Insulina Asparte (substância ativa): 157; insulina humana regular: 165)) não indicou nenhum efeito adverso da Insulina Asparte (substância ativa)e na gravidez ou na saúde do feto/recém-nascido.
Adicionalmente, os dados de um estudo clínico incluindo 27 mulheres com diabetes gestacional, randomizadas para tratamento com Insulina Asparte (substância ativa)e versus insulina humana (Insulina Asparte (substância ativa): 14; insulina humana regular: 13) demonstraram perfis de segurança similares entre os tratamentos assim como aumento significativo no controle da glicemia pós-prandial no grupo tratado com Insulina Asparte (substância ativa).
Propriedades Farmacocinéticas
Na molécula de Insulina Asparte (substância ativa), a substituição do aminoácido prolina pelo ácido aspártico na posição B28 reduz a tendência à formação de hexâmeros, conforme observado com a insulina humana regular.
Insulina Asparte (substância ativa) é, portanto, mais rapidamente absorvido da camada subcutânea em comparação à insulina humana regular.
O tempo para atingir a concentração máxima é, em média, metade daquele para a insulina humana regular.
Uma concentração plasmática máxima média de 492 pmol/L foi atingida em 40 minutos após uma dose subcutânea de 0,15 U/Kg de peso corporal em pacientes com diabetes tipo 1.
As concentrações de insulina retornam ao nível basal em aproximadamente 4 a 6 horas após a aplicação.
A taxa de absorção foi relativamente mais lenta em portadores de diabetes tipo 2, resultando em uma Cmáx menor (352 ± ) e um tmax mais tardio (60 minutos).
A variabilidade intraindividual no tempo para a concentração máxima é significativamente menor para Insulina Asparte (substância ativa) do que para a insulina humana regular, enquanto a variabilidade intraindividual no Cmáx para Insulina Asparte (substância ativa) é maior.
Crianças e adolescentes
As propriedades farmacocinéticas e farmacodinâmicas de Insulina Asparte (substância ativa) foram investigadas em crianças (6-12 anos) e adolescentes (13-17 anos) com diabetes Tipo 1.
A Insulina Asparte (substância ativa)e foi rapidamente absorvida em ambos os grupos de idade, com tmáx similares aos dos adultos. Entretanto, a Cmáx diferiu entre os grupos de idade, enfatizando a importância da titulação individual de Insulina Asparte (substância ativa).
Idosos
As diferenças relativas nas propriedades farmacocinéticas entre Insulina Asparte (substância ativa)e e insulina humana regular em pacientes idosos (65-83 anos, idade média 70 anos) com diabetes tipo 2 foram similares àquelas observadas em voluntários sadios e em pacientes mais jovens com diabetes.
Uma taxa de absorção diminuída foi observada em idosos, resultando em um tmáx posterior (82 minutos (faixa interquartil: 60-120)), enquanto o Cmáx foi similar ao observado em pacientes mais jovens com diabetes tipo 2 e levemente menor do que em pacientes com diabetes tipo 1.
Disfunção hepática
Um estudo farmacocinético de dose única de Insulina Asparte (substância ativa)e foi realizado com 24 voluntários com função hepática variando de normal a severamente alterada.
Em pacientes com disfunção hepática a taxa de absorção foi reduzida e mais variável, resultando em tmáx atrasado de 50 min, aproximadamente, em pacientes com função hepática normal à 85 min em pacientes com disfunção hepática moderada e severa.
AUC, Cmáx e CL/F foram similares em pacientes com função hepática reduzida comparado com pacientes com função hepática normal.
Disfunção renal
Um estudo farmacocinético de dose única de Insulina Asparte (substância ativa)e foi realizado com 18 voluntários com função renal variando de normal a severamente alterada.
Nenhum efeito aparente dos valores de clearance da creatinina na AUC, CL/F e Cmáx de Insulina Asparte (substância ativa)e foi encontrado.
Os dados foram limitados em pacientes com disfunção renal moderada e severa.
Pacientes com disfunção renal que necessitam de tratamento com diálise não foram investigados.
Dados de segurança pré-clínicos
Dados não clínicos não revelam perigo especial para humanos, tendo como base os estudos convencionais de farmacologia de segurança, toxicidade de dose repetida, genotoxicidade e toxicidade para reprodução.
Em testes in vitro, incluindo a ligação aos receptores de insulina e de IGF-1 e efeitos no crescimento celular, a Insulina Asparte (substância ativa)e se comportou de maneira extremamente similar à insulina humana. Estudos também demonstraram que a dissociação da ligação com o receptor de insulina da Insulina Asparte (substância ativa)e é equivalente à da insulina humana.
Cuidados de Armazenamento
NovoMix 30 Penfill que não está sendo utilizado deve ser conservado em refrigerador (temperatura entre 2 ºC e 8 ºC), distante do compartimento do congelador. Não congelar.
NovoMix 30 Penfill que está sendo utilizado ou carregado como reserva não deve ser conservado em refrigerador.
Após retirar NovoMix 30 Penfill do refrigerador, você deve ressuspender a insulina de acordo com as instruções para a primeira utilização.
Você pode carregar NovoMix 30 Penfill com você e mantê-lo à temperatura ambiente (entre 15 °C e 30 °C) por até 4 semanas.
Após aberto, válido por 4 semanas, sendo armazenado entre 15 ºC e 30 ºC.
Sempre mantenha os carpules na embalagem original quando não estiver em uso, para protegê-lo da luz.
NovoMix 30 Penfill deve ser protegido do calor excessivo e da luz solar.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Número de lote e datas de fabricação e validade: vide embalagem.
O prazo de validade corresponde ao último dia do mês indicado.
Medicamentos não devem ser descartados pelo encanamento ou no lixo doméstico. Pergunte ao seu farmacêutico como eliminar os medicamentos que já não são necessários. Estas medidas ajudarão a proteger o meio ambiente.
Características Físicas
NovoMix 30 é uma suspensão injetável branca. No interior do carpule, há uma esfera de vidro para facilitar a ressuspensão. Após a ressuspensão o líquido deve se apresentar uniformemente branco e leitoso.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
Dizeres Legais
Registro MS 1.1766.0017
Farmacêutico responsável
Luciane M. H. Fernandes – CRF/PR n°6002
Fabricado por
Novo Nordisk A/S
DK-2880 Bagsvaerd, Dinamarca
Importado por
Novo Nordisk Farmacêutica do Brasil Ltda.
Rua Prof. Francisco Ribeiro, 683
CEP: 83707-660 - Araucária/PR
CNPJ: 82.277.955/0001-55
Disk Novo Nordisk: 0800 144488
Venda sob prescrição médica.