Comparamos o preço de Venzer 16 Mg 30 Comprimidos, veja o menor preço

R$ 69,09
RReferência
18
ofertasMelhores preços a partir de R$ 62,03 até R$ 84,51
Oferta patrocinada
vendido por Drogaria Nova Esperança
economize
18.25%
R$ 69,09
Mais de 47 anos de tradição, loja RA1000 e Ebit Diamante!
Oferta patrocinada
vendido por Drogarias Pacheco
economize
17.56%
R$ 69,67
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
Oferta patrocinada
vendido por Drogaria São Paulo
economize
8.95%
R$ 76,95
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Farmácia Preço Popular
economize
26.60%
R$ 62,03
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogaria Araújo
economize
25.46%
R$ 62,99
vendido por Drogaria Vera Cruz
economize
24.65%
R$ 63,68
Entregas para todo o Brasil. Clique e confira!
vendido por Pague Menos
economize
23.69%
R$ 64,49
vendido por Drogaria Catarinense
economize
17.34%
R$ 69,86
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Farmácia.
vendido por Farmácia Indiana
economize
16.94%
R$ 70,19
vendido por Farmácia Online Farmagora
economize
16.66%
R$ 70,43
Pagamento em até 6X sem juros. Frete Grátis! Regras no Site.
vendido por Drogaria Primus
economize
11.84%
R$ 74,50
vendido por Drogaria Soares
economize
10.77%
R$ 75,41
Enviamos para todo o Brasil. Clique e confira!
vendido por Farmácia Super Droga 10
economize
10.76%
R$ 75,42
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
vendido por Drogão Net
economize
8.33%
R$ 77,47
vendido por Agille Medicamentos
economize
6.14%
R$ 79,32
Preço Válido para compra em Boleto
vendido por Drogaria Campeã
economize
0.85%
R$ 83,79
vendido por Promofarma
economize
0.85%
R$ 83,79
vendido por Panvel Farmácias
R$ 84,51
Dúvidas quanto ao Preço ou Frete? Clique e vá direto ao site da Drogaria.
Para que serve
Venzer é indicado para o tratamento de insuficiência cardíaca (coração fraco) e hipertensão arterial (pressão alta) leve, moderada e grave.
O tratamento com Venzer reduz a mortalidade, reduz a hospitalização devido à insuficiência cardíaca e melhora os sintomas.
Como Venzer funciona?
Venzer faz parte de uma classe de medicamentos chamada de bloqueadores dos receptores de angiotensina II, que relaxa e alarga os vasos sanguíneos para reduzir a pressão arterial, fazendo que seu coração bombeie sangue para todas as partes de seu corpo mais facilmente.
Após a administração de uma única dose de Venzer, a pressão arterial começa a reduzir geralmente dentro de 2 horas.
O efeito anti-hipertensivo máximo é atingido dentro de 4 semanas após o início do tratamento.
Contraindicação
Você não deve utilizar Venzer se
- Tiver alergia à candesartana cilexetila ou a qualquer um dos componentes da fórmula;
- Estiver grávida ou amamentando;
- Tiver alterações graves no fígado e/ou colestase (redução do fluxo biliar, no qual surge uma cor amarelada na pele);
- Tiver diabetes mellitus (tipo I ou II);
- Tiver insuficiência renal moderada a grave (TGF < 60 mL/min/1,73 m2);
- Fizer uso de medicamento contendo alisquireno.
Como usar
Os comprimidos de Venzer devem ser administrados 1 vez ao dia, por via oral, com ou sem a ingestão de alimentos.
Posologia
Hipertensão
Dose inicial
8 mg, 1 vez ao dia.
Dose de manutenção
8 mg, 1 vez ao dia, podendo ser aumentada para 16 mg, 1 vez ao dia.
Para pacientes que requerem uma maior redução da pressão sanguínea, a dose pode ser aumentada para 32 mg, 1 vez ao dia.
O efeito anti-hipertensivo máximo é atingido dentro de 4 semanas após o início do tratamento.
Em pacientes com uma redução da pressão arterial inferior à considerada ótima com Venzer, recomendasse associação com um diurético tiazídico.
Posologia para populações especias no tratamento de hipertensão
Idosos
Não é necessário ajuste de dose inicial em idosos.
Pacientes com alterações renais
Não é necessário ajuste de dose inicial em pacientes com alterações renais de leve a moderada (depuração de creatinina 30-80 mL/min/1,73 m2 de área corpórea).
Em pacientes com alterações renais graves (depuração de creatinina <30 mL/min/1,73 m2 de área corpórea), a experiência clínica é limitada, devendo-se considerar uma dose inicial de 4 mg.
Pacientes com alterações hepáticas
Titulação de dose é recomendada em pacientes com doença hepática crônica de leve a moderada e, uma dose inicial de 4 mg deve ser considerada.
Venzer não deve ser usado em pacientes com alterações hepáticas graves e/ou colestase.
Terapia concomitante
Venzer pode ser administrado com outros agentes anti-hipertensivos.
Insuficiência Cardíaca
A dose inicial usual recomendada de Venzer é de 4 mg uma vez ao dia.
A titulação para a dose alvo de 32 mg uma vez ao dia ou para a maior dose tolerada é realizada dobrando-se a dose em intervalos de pelo menos 2 semanas.
Posologia para populações especias no tratamento de insuficiência cardíaca
Não é necessário ajuste de dose inicial para pacientes idosos ou pacientes com alterações nos rins ou fígado.
Terapia concomitante
Venzer pode ser administrado com outro tratamento para insuficiência cardíaca, incluindo inibidores da ECA, betabloqueadores, diuréticos e digitálicos ou uma associação desses medicamentos.
Posologia para crianças
Não foram estabelecidas a segurança e a eficácia do uso de Venzer em crianças.
Este medicamento não deve ser partido, aberto ou mastigado.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
O que devo fazer quando eu me esquecer de usar Venzer?
Se você se esquecer de tomar uma dose de Venzer, não é necessário tomar a dose esquecida, deve-se apenas tomar a próxima dose, no horário habitual.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
Precauções
Venzer deve ser utilizado com cuidado nas seguintes situações:
- Pacientes com pressão arterial baixa (hipotensão) devido à insuficiência cardíaca ou com redução do volume de sangue dentro dos vasos sanguíneos;
- O uso combinado de bloqueadores dos receptores de angiotensina II (BRAs), como Venzer, não é recomendado com medicamentos como inibidores da ECA (enzima conversora de angiotensina) ou alisquirenos, pois pode haver queda da pressão arterial (hipotensão), aumento da concentração de potássio no sangue (hipercalemia) e alterações na função dos rins (incluindo falência renal aguda);
- Em pacientes com insuficiência cardíaca também não é recomendada a combinação tripla de Venzer com um inibidor da ECA (enzima conversora de angiotensina) e um antagonista de receptor de mineralocorticoide;
- Em pacientes com estenose da artéria renal (estreitamento das artérias que nutrem os rins) pode ocorrer um aumento nos níveis sanguíneos de ureia e creatinina (substâncias que se acumulam no sangue e que podem ser usadas para avaliar a função renal);
- Pode ocorrer uma piora da função dos rins em pacientes predispostos a problemas renais. Quando Venzer for utilizado em pacientes com insuficiência dos rins e insuficiência do coração deve-se avaliar periodicamente os níveis de potássio e creatinina;
- Não se tem muita experiência do uso de Venzer em pacientes com transplante de rim e insuficiência do fígado;
- Pacientes com estenose das válvulas mitral e aórtica do coração (estreitamento de estruturas internas cuja função é garantir o sentido correto do fluxo de sangue dentro do coração) e cardiomiopatia hipertrófica obstrutiva (tipo de doença do músculo do coração que causa obstrução do fluxo sanguíneo);
- Pacientes hipertensos em uso associado de Venzer e inibidores da enzima conversora da angiotensina - ECA (por exemplo, captopril, enalapril, ramipril, etc), suplementos contendo potássio, substitutos do sal que contém potássio, diuréticos poupadores de potássio (como por exemplo, espironolactona) ou outros medicamentos que podem aumentar os níveis de potássio no sangue (como heparina, cotrimoxazol) podem ter aumento dos níveis de potássio no sangue;
- Deve-se ter cuidado durante a cirurgia e anestesia, pois pode ocorrer hipotensão (redução da pressão arterial);
- Em pacientes com insuficiência cardíaca e/ou renal grave, o uso de Venzer pode levar a hipotensão (pressão baixa), oligúria (redução importante da eliminação de urina pelos rins), azotemia (aumento dos níveis de ureia e creatinina) e insuficiência renal aguda;
- Deve-se ter cuidado em pacientes com doenças graves nas artérias do cérebro e coração para que não ocorra redução acentuada da pressão arterial.
Dados de estudos clínicos têm demonstrado que o uso combinado de inibidores da ECA (enzima conversora de angiotensina), bloqueadores de receptores de angiotensina II ou alisquirenos está associado com uma frequência maior de eventos adversos como queda da pressão arterial (hipotensão), aumento da concentração de potássio no sangue (hipercalemia) e alterações na função dos rins (incluindo falência renal aguda) comparado ao uso isolado de um dos agentes citados.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Reações Adversas
Estudos clínicos
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento)
Pressão baixa, hipercalemia e alterações nos rins.
Podem ocorrer alterações nos resultados de exames laboratoriais referentes aos níveis de: hemoglobina, creatinina, ureia, potássio, sódio ou TGP (uma enzima do fígado).
Pós-comercialização
Reação muito rara (ocorre em 0,01% dos pacientes que utilizam este medicamento)
Diminuição dos glóbulos brancos do sangue (leucopenia), diminuição do número de neutrófilos no sangue (neutropenia), ausência ou número insuficiente de glóbulos brancos granulócitos no sangue (agranulocit ose), concentração superior ao normal de íons de potássio no sangue (hipercalemia), concentração anormalmente baixa de íons de sódio no sangue (hiponatremia), tontura, tosse, função do fígado alterada, inflamação do fígado (hepatite), inchaço de membros inferiores (nas pernas, tornozelos e pés), lesões na pele com vermelhidão (exantema), coceira na pele com vermelhidão (urticária), coceira na pele (prurido), dor nas costas e alterações nos rins (incluindo insuficiência em pacientes suscetíveis).
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
População Especial
Crianças
A segurança e a eficácia de candesartana cilexetila em crianças não foram estabelecidas.
Gravidez
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez.
Efeitos sobre a capacidade de dirigir veículos e operar máquinas
Verifique a sua reação ao medicamento antes de dirigir veículos ou operar máquinas, porque pode ocorrer tontura ou cansaço durante o tratamento com Venzer.
Pacientes com intolerância a lactose
Este medicamento contém lactose monoidratada (178,122 mg/comprimidos de 8 mg; 169,732 mg/comprimidos de 16 mg; 155,942 mg/comprimido de 32 mg), portanto, deve ser usado com cautela por pacientes com intolerância à lactose.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Composição
Cada comprimido de 8 mg contém:
8 mg de candesartana cilexetila.
Excipientes: hiprolose, macrogol, corante laca amarelo crepúsculo, amido, lactose monoidratada, carmelose cálcica e estearato de magnésio.
Cada comprimido de 16 mg contém:
16 de candesartana cilexetila.
Excipientes: hiprolose, macrogol, corante laca amarelo crepúsculo, amido, lactose monoidratada, carmelose cálcica e estearato de magnésio.
Cada comprimido de 32 mg contém:
32 mg de candesartana cilexetila.
Excipientes: hiprolose, macrogol, corante laca amarelo crepúsculo, amido, lactose monoidratada, carmelose cálcica e estearato de magnésio.
Superdosagem
Sintomas
Podem ocorrer: hipotensão sintomática (sintomas de pressão baixa) e tontura.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
Interação Medicamentosa
Dados de ensaios clínicos têm demonstrado que o bloqueio duplo do sistema reninaangiotensina-aldosterona através do uso combinado de inibidores da ECA, bloqueadores de receptores de angiotensina II ou alsquireno está associado com uma frequência mais alta de eventos adversos como hipotensão, hipercalemia e função renal diminuída (incluindo falência renal aguda) comparado ao uso de um agente isolado que atue no sistema renina-angiotensina-aldosterona.
As seguintes substâncias foram investigadas em estudos de farmacocinética clínica:
Hidroclorotiazida, varfarina, digoxina, contraceptivos orais (etinilestradiol/levonorgestrel), glibenclamida, nifedipino e enalapril.
Não foi identificada interação farmacocinética de relevância clínica com candersartana cilexetila.
Durante a administração concomitante de lítio com inibidores da ECA, foram relatados aumentos reversíveis das concentrações séricas de lítio e toxicidade.
Um efeito similar pode ocorrer com antagonistas dos receptores de angiotensina II, e recomenda-se monitoração cuidadosa dos níveis séricos de lítio durante uso concomitante com lítio.
O efeito anti-hipertensivo de antagonistas dos receptores de angiotensina II, incluindo o Candesartana Cilexetila (substância ativa), pode ser atenuado por anti-inflamatórios não esteroidais (AINEs) como os inibidores seletivos de COX-2 e ácido acetilsalicílico.
Assim como acontece com os inibidores da ECA, o uso concomitante de antagonistas dos receptores de angiotensina II e AINEs pode levar a um risco aumentado de agravamento da função renal, incluindo possível insuficiência renal aguda, e um aumento no potássio sérico, especialmente em pacientes com problemas pré-existente na função renal.
A associação deve ser administrada com precaução, especialmente em pacientes idosos e em pacientes com depleção de volume.
Os pacientes devem ser adequadamente hidratados e deve-se considerar a monitoração periódica da função renal após o início e depois da terapia concomitante.
O efeito anti-hipertensivo de Candesartana Cilexetila (substância ativa) pode ser aumentado por outros anti-hipertensivos.
Interação Alimentícia
A biodisponibilidade da candesartana não é afetada por alimentos.
Ação da Substância
Resultados de eficácia
Hipertensão
Na hipertensão, Candesartana Cilexetila (substância ativa) causa uma redução prolongada da pressão arterial, dose-dependente. A ação anti-hipertensiva é devida à diminuição da resistência periférica sistêmica, embora a frequência cardíaca, o volume de ejeção e o débito cardíaco não sejam afetados.
Não há indícios de hipotensão grave ou exagerada com a primeira dose ou de efeito rebote após a interrupção do tratamento.
Em dois estudos randomizados, duplo-cegos, de 8 semanas de duração, os efeitos de redução da pressão arterial de Candesartana Cilexetila (substância ativa) e losartana foram avaliados em um total de 1.268 pacientes com hipertensão leve a moderada.
Em ambos os estudos, a redução na pressão arterial sistólica e diastólica foi significativamente maior com Candesartana Cilexetila (substância ativa) (32 mg, uma vez ao dia).
Em uma análise agrupada, a redução mínima da pressão arterial (sistólica/diastólica) foi 13,1/10,5 mmHg com Candesartana Cilexetila (substância ativa) e 10,0/8,7 mmHg com losartana potássica (100 mg, uma vez ao dia).
A diferença média na redução da pressão arterial foi 3,1/1,8 mmHg (p<0,0001/p<0,0001).
Candesartana Cilexetila (substância ativa) pode ser usado como monoterapia ou em combinação com outras substâncias antihipertensivas, como os diuréticos tiazídicos e os antagonistas de cálcio diidropiridínicos para melhorar a eficácia.
Candesartana Cilexetila (substância ativa) é igualmente eficaz nos pacientes, independentemente da idade e do sexo.
Candesartana Cilexetila (substância ativa) é eficaz na redução da pressão sanguínea independentemente da raça, embora o efeito seja um pouco menor em pacientes negros (população usualmente com baixa renina). Isso é geralmente comum para substâncias que bloqueiam o sistema renina-angiotensina-aldosterona.
Candesartana Cilexetila (substância ativa) aumenta o fluxo sanguíneo renal e mantém ou aumenta a taxa de filtração glomerular, enquanto a resistência vascular renal e a fração de filtração são reduzidas.
Candesartana Cilexetila (substância ativa) também reduz a excreção de albumina na urina em pacientes com diabetes mellitus tipo II, hipertensão e microalbuminúria.
Em pacientes hipertensos com diabetes mellitus tipo II, o tratamento de 12 semanas com Candesartana Cilexetila (substância ativa) 8 mg a 16 mg não teve efeitos adversos na glicemia ou no perfil lipídico.
No estudo SCOPE - Study on Cognition and Prognosis in the Elderly (Estudo em Cognição e Prognóstico em Idosos), os efeitos do tratamento anti-hipertensivo com Candesartana Cilexetila (substância ativa) na morbidade e na mortalidade cardiovascular, na função cognitiva e na qualidade de vida foram avaliados em 4.937 pacientes idosos (70-89 anos) com hipertensão (Pressão Arterial Sistólica (PAS) 160-179 mmHg e/ou Pressão Arterial Diastólica (PAD) 90-99 mmHg).
A tabela a seguir mostra os resultados do estudo para o desfecho primário (eventos cardiovasculares (CV) importantes) e seus componentes.
Ambos os regimes de tratamento reduziram efetivamente a pressão arterial sistólica e diastólica e foram geralmente bem tolerados. A função cognitiva e a qualidade de vida foram mantidas de maneira apropriada em ambos os grupos do tratamento.
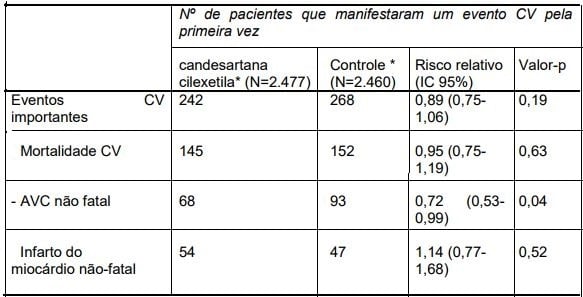
*Qualquer tratamento anti-hipertensivo prévio foi padronizado para hidroclorotiazida 12,5 mg, uma vez ao dia, antes da randomização. Outro tratamento anti-hipertensivo foi adicionado à medicação do estudo duplo-cego (Candesartana Cilexetila (substância ativa) 8-16 mg ou placebo correspondente, uma vez ao dia) se mantida PAS ? 160 mmHg e/ou PAD ? 90 mmHg. Tal tratamento adicional foi administrado em 49% e 66% dos pacientes nos grupos de Candesartana Cilexetila (substância ativa) e no grupo controle, respectivamente.
Insuficiência Cardíaca
Nos pacientes com insuficiência cardíaca crônica (ICC) e função ventricular sistólica esquerda deprimida (fração da ejeção ventricular esquerda, FEVE ? 40%), Candesartana Cilexetila (substância ativa) diminui a resistência vascular sistêmica e a pressão capilar pulmonar, aumenta a atividade da renina plasmática e a concentração de angiotensina II, e diminui os níveis de aldosterona.
O tratamento com Candesartana Cilexetila (substância ativa) reduz a mortalidade e a hospitalização devido a ICC e melhora os sintomas como mostrado no estudo CHARM (Candesartan in Heart Failure – Assessment of Reduction in Mortality and Morbidity / Candesartana em Insuficiência Cardíaca – Avaliação da redução da mortalidade e da morbidade).
Este estudo multinacional, controlado por placebo, duplocego, em pacientes com ICC com classe funcional da New York Heart Association (NYHA) II a IV, consistiu em três estudos separados:
CHARM-Alternativo (n=2.028) em pacientes com FEVE ?40% não tratados com um inibidor da ECA devido à intolerância, CHARM-Adicionado (n=2.548) em pacientes com FEVE ?40% e tratados com um inibidor da ECA, e CHARM - Preservado (n=3.023) em pacientes com FEVE > 40%.
Pacientes com terapia convencional foram randomizados para o placebo ou Candesartana Cilexetila (substância ativa) (titulado de 4 mg ou 8 mg uma vez ao dia para 32 mg, uma vez ao dia, ou a maior dose tolerada, dose média de 24 mg) e acompanhados por uma mediana de 37,7 meses.
O desfecho composto de mortalidade cardiovascular ou primeira hospitalização por ICC foi reduzido significativamente com o Candesartana Cilexetila (substância ativa) em comparação com o placebo no CHARM-Alternativo (razão de risco (RR) 0,77, IC 95% 0,67-0,89, p<0,001) e no CHARM-Adicionado (RR 0,85, IC 95% 0,75-0,96, p=0,011). Isto corresponde a uma redução de risco relativo de 23% e de 15%, respectivamente.
Uma redução numérica, embora estatisticamente não significativa, também foi alcançada no CHARM-Preservado (RR 0,89, IC 95% 0,77-1,03, p=0,118).
O desfecho composto de mortalidade por todas as causas ou primeira hospitalização por ICC também foi reduzido significativamente com o Candesartana Cilexetila (substância ativa) no CHARM-Alternativo (RR 0,80, IC 95% 0,70 - 0,92, p=0,001) e CHARM - Adicionado (RR 0,87, IC 95% 0,78-0,98, p=0,021), e uma tendência similar foi observada no CHARM-Preservado (RR 0,92, IC 95% 0,80-1,05, p=0,221).
Ambos os componentes de mortalidade e de morbidade (hospitalização por ICC) destes desfechos compostos contribuíram para os efeitos favoráveis de Candesartana Cilexetila (substância ativa) no CHARM-Alternativo e CHARM-Adicionado.
Os efeitos favoráveis indicados no CHARM-Preservado foram devidos à redução da hospitalização por ICC.
Mortalidade por todas as causas também foi avaliada nas populações agrupadas do CHARMAlternativo e CHARM–Adicionado (RR 0,88, IC 95% 0,79-0,98, p=0,018) e em todos os três estudos (RR 0,91, IC 95% 0,83-1,00, p=0,055).
O tratamento com Candesartana Cilexetila (substância ativa) resultou em uma melhora da classe funcional NYHA no CHARM-Alternativo e CHARM–Adicionado (p=0,008 e p=0,020 respectivamente).
Os efeitos benéficos de Candesartana Cilexetila (substância ativa) na mortalidade cardiovascular e hospitalização por ICC foram consistentes, independentemente da idade, sexo e medicação concomitante.
Candesartana Cilexetila (substância ativa) também foi eficaz em pacientes tomando concomitantemente betabloqueadores e inibidores da ECA, e os benefícios foram obtidos mesmo se os pacientes estavam ou não tomando inibidores da ECA na dose recomendada pelas diretrizes de tratamento.
Características farmacológicas
Propriedades Farmacodinâmicas
A angiotensina II é o hormônio vasoativo primário do sistema renina-angiotensina-aldosterona e exerce um significativo papel na fisiopatologia da hipertensão, insuficiência cardíaca e outros transtornos cardiovasculares.
Também exerce um importante papel na patogênese da hipertrofia e lesões de órgãos alvo.
Os principais efeitos fisiológicos da angiotensina II, como a vasoconstrição, estimulação da aldosterona, regulação da homeostase do sal e da água e a estimulação do crescimento celular, são mediados via receptor do tipo 1 (AT1).
Candesartana Cilexetila (substância ativa) é um pró-fármaco adequado para o uso oral, sendo rapidamente convertido ao fármaco ativo candesartana, por hidrólise de éster durante a absorção no trato gastrointestinal.
A candesartana é um antagonista do receptor da angiotensina II, seletivo para receptores AT1, com forte ligação e lenta dissociação dos mesmos, não tendo atividade agonista.
A candesartana não inibe a enzima conversora de angiotensina (ECA), que converte a angiotensina I para angiotensina II e degrada a bradicinina.
Como não há efeito na degradação da bradicinina, é improvável que os antagonistas dos receptores de angiotensina II sejam associados com tosse.
Em estudos clínicos controlados que compararam Candesartana Cilexetila (substância ativa) com inibidores da ECA, a incidência de tosse foi menor nos pacientes que receberam Candesartana Cilexetila (substância ativa).
A candesartana não se liga ou bloqueia outros receptores hormonais ou canais de íons conhecidos por serem importantes na regulação cardiovascular.
O antagonismo dos receptores AT1 da angiotensina II resulta em aumento dose relacionada da atividade da renina plasmática, das concentrações de angiotensina I e angiotensina II e em uma diminuição da concentração plasmática de aldosterona.
Propriedades Farmacocinéticas
Absorção e distribuição
Após a administração oral, a Candesartana Cilexetila (substância ativa) é convertida para substância ativa candesartana.
A biodisponibilidade absoluta da candesartana é de aproximadamente 40% após uma solução oral de Candesartana Cilexetila (substância ativa).
A biodisponibilidade relativa dos comprimidos em comparação com a solução oral é de aproximadamente 34%, com variabilidade muito pequena.
O pico médio de concentração plasmática (Cmáx) ocorre entre 3-4 horas após a ingestão do comprimido.
As concentrações séricas da candesartana aumentam linearmente com o aumento das doses na faixa de dose terapêutica.
Não foram observadas diferenças relacionadas ao sexo na farmacocinética da candesartana.
A área sob a curva de concentração plasmática versus tempo (AUC) não é significativamente afetada por alimentos.
A candesartana liga-se extensivamente às proteínas plasmáticas (>99%). O volume aparente de distribuição da candesartana é de 0,1 L/kg.
Metabolismo e eliminação
A candesartana é principalmente eliminada inalterada pelas vias urinária e biliar e apenas uma pequena parte é eliminada pelo metabolismo hepático (CYP2C9).
Os estudos de interação disponíveis não indicam efeito em CYP2C9 e CYP3A4.
Com base em dados in vitro, não seria esperada qualquer interação in vivo com fármacos cujo metabolismo é dependente das isoenzimas do citocromo P450: CYP1A2, CYP2A6, CYP2C9, CYP2C19, CYP2D6, CYP2E1 ou CYP3A4.
A meia-vida de eliminação da candesartana é de aproximadamente 9 horas.
Não há acúmulo após a administração de doses múltiplas.
A depuração plasmática total da candesartana é cerca de 0,37 mL/min/kg, com uma depuração renal de cerca de 0,19 mL/min/kg.
A eliminação renal da candesartana ocorre tanto por filtração glomerular como por secreção tubular ativa.
Seguindo uma dose oral de Candesartana Cilexetila (substância ativa) marcada com 14C, cerca de 26% da dose é excretada na urina como candesartana, e 7% como metabólito inativo, enquanto aproximadamente 56% da dose é recuperada nas fezes como candesartana e 10% como metabólito inativo.
Populações especiais
Em idosos (acima de 65 anos), tanto a Cmáx quanto a AUC da candesartana são aumentadas em aproximadamente 50% e 80%, respectivamente, em comparação com indivíduos jovens.
Entretanto, a resposta da pressão sanguínea e a incidência de eventos adversos são semelhantes após a administração de candesartana cilexetila em pacientes jovens e idosos.
Em pacientes com alterações renais de leve a moderada, a Cmáx e a AUC da candesartana aumentaram com doses repetidas em aproximadamente 50% e 70%, respectivamente, mas a meia-vida (t½) não foi alterada em comparação com pacientes com a função renal normal.
As alterações correspondentes nos pacientes com alterações renais graves foram cerca de 50% e 110%, respectivamente.
A t½ de eliminação da candesartana foi aproximadamente o dobro nos pacientes com alterações renais graves.
A farmacocinética em pacientes que fazem hemodiálise foi similar àquela dos pacientes com alterações renais graves.
Em pacientes com alterações hepáticas de leve a moderada, houve um aumento na AUC da candesartana de aproximadamente 20%.
Em pacientes com alterações hepáticas de moderada a grave o aumento na AUC da candesartana foi de aproximadamente 80%.
Há apenas experiência limitada do uso em pacientes com alterações hepáticas graves e/ou colestase.
Dados de segurança pré-clínica
Em diversos estudos de segurança pré-clínica conduzidos em várias espécies, foram observados efeitos farmacológicos exagerados esperados devido à modificação da homeostase do sistema reninaangiotensina-aldosterona.
A incidência e a gravidade dos efeitos induzidos foram relacionadas à dose e ao tempo e mostraram-se reversíveis em animais adultos.
Estudos com Candesartana Cilexetila (substância ativa), em animais, demonstraram atraso fetal e lesões renais em neonatos.
Acredita-se que o mecanismo seja farmacologicamente mediado por efeitos no sistema renina-angiotensina-aldosterona.
Não houve evidência de mutagenicidade, clastogenicidade ou carcinogenicidade.
Tempo estimado para início da ação terapêutica
Após a administração de uma única dose de Candesartana Cilexetila (substância ativa), o início do efeito anti-hipertensivo geralmente ocorre dentro de 2 horas.
Com o tratamento contínuo, a redução máxima da pressão sanguínea com qualquer dose geralmente é atingida dentro de 4 semanas e é mantida durante o tratamento prolongado.
Candesartana Cilexetila (substância ativa) administrado uma vez ao dia promove uma efetiva e suave redução da pressão sanguínea ao longo de 24 horas com pequena diferença entre os efeitos máximo e mínimo no intervalo de dose.
Cuidados de Armazenamento
Este medicamento deve ser mantido em temperatura ambiente (entre 15°C e 30°C), protegido da luz e da umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Todo medicamento deve ser mantido fora do alcance das crianças.
Características organolépticas
Os comprimidos de Venzer 8 mg, 16 mg e 32 mg são de cor salmão, biconvexo, circular.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observar alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Dizeres Legais
MS nº. 1.0033.0197.
Farmacêutica responsável:
Cintia Delphino de Andrade
CRF-SP nº: 25.125.
Registrado por:
Libbs Farmacêutica LTDA.
Rua Josef Kryss, 250
São Paulo – SP
CNPJ 61.230.314/0001-75.
Fabricado por:
Libbs Farmacêutica LTDA.
Rua Alberto Correia Francfort, 88
Embu das Artes – SP.
Indústria brasileira.
Venda sob prescrição médica.?